"CNL"의 두 판 사이의 차이
Uosche2526 (토론 | 기여) (→개발 과제의 개요) |
Uosche2526 (토론 | 기여) (→Boundary thickness) |
||
| (같은 사용자의 중간 판 16개는 보이지 않습니다) | |||
| 3번째 줄: | 3번째 줄: | ||
==프로젝트 개요== | ==프로젝트 개요== | ||
=== 기술개발 과제 === | === 기술개발 과제 === | ||
| − | + | 국문 : 전기화학적 CO2 환원반응에 대한 전기화학적 측정 방법에 대한 고찰 | |
| − | + | 영문 : A Review on Electrochemical Measurement Methods for CO2RR | |
| − | |||
===과제 팀명=== | ===과제 팀명=== | ||
| − | CNL | + | CNL |
===지도교수=== | ===지도교수=== | ||
| − | 이두환 교수님 | + | 이두환 교수님 |
===개발기간=== | ===개발기간=== | ||
| − | 2025년 9월 ~ 2025년 12월 (총 4개월) | + | 2025년 9월 ~ 2025년 12월 (총 4개월) |
===구성원 소개=== | ===구성원 소개=== | ||
| − | 서울시립대학교 화학공학과 20228710** 정*은(팀장) | + | 서울시립대학교 화학공학과 20228710** 정*은(팀장) |
| − | + | 서울시립대학교 화학공학과 20203400** 남*재 | |
| − | 서울시립대학교 화학공학과 20203400** 남*재 | ||
==서론== | ==서론== | ||
| 44번째 줄: | 42번째 줄: | ||
===관련 기술의 현황=== | ===관련 기술의 현황=== | ||
====관련 기술의 현황 및 분석(State of art)==== | ====관련 기술의 현황 및 분석(State of art)==== | ||
| − | * | + | * 나노 구조 및 결정면 제어 촉매 |
| − | + | 대다수의 CO2 RR 관련 특허는 특정 생성물에 대한 패러데이 효율과 활성을 높이는 새로운 촉매 구조 또는 조성 개발에 집중되어 있다. C2 이상의 고부가 탄화수소 생성에 특화된 나노 구조 또는 산화물 유래 Cu를 개발한다. 이는 표면에 CO Dimerization에 유리한 특정 격자 변형이나 원자 틈을 유도하여 선택성을 향상시킨다. CO 선택성이 높은 Ag 촉매의 경우, 나노입자의 곡선형 표면이나 edge 부위의 비율을 조절하여 CO 생성에 대한 활성 부위를 극대화하는 기술이 주를 이룬다. 나노 구조 촉매는 제조 공정이 복잡하고, 촉매 표면의 결정면이 불균일하여 성능 평가의 재현성이 낮다는 근본적인 문제가 있다. | |
| − | |||
| − | 대다수의 CO2 RR 관련 특허는 특정 생성물에 대한 패러데이 효율과 활성을 높이는 새로운 촉매 구조 또는 조성 개발에 집중되어 있다. C2 이상의 고부가 탄화수소 생성에 특화된 나노 구조 또는 산화물 유래 Cu를 개발한다. 이는 표면에 CO Dimerization에 유리한 특정 격자 변형이나 원자 틈을 유도하여 선택성을 향상시킨다. CO 선택성이 높은 Ag 촉매의 경우, 나노입자의 곡선형 표면이나 edge 부위의 비율을 조절하여 CO 생성에 대한 활성 부위를 극대화하는 기술이 주를 이룬다. 나노 구조 촉매는 제조 공정이 복잡하고, 촉매 표면의 결정면이 불균일하여 성능 평가의 재현성이 낮다는 근본적인 문제가 있다. | ||
| − | |||
| − | |||
| − | |||
| − | |||
| − | |||
| − | |||
| − | |||
| − | |||
| − | + | * 고압 CO2를 직접 활용하는 반응기 설계 동향 | |
| − | + | 포집된 고압 CO2를 별도 감압 없이 직접 전해반응기로 주입하여 formate 등으로 전환하는 고압 전해 시스템을 제시한다. 본 특허는 상용 Cu 기반의 나노구조 전극을 PPy 등으로 기능화하여 H+ 흡착을 억제하고 CO2 환원 선택도를 향상시키는 전극 설계를 포함하며 고압에서의 CO2 표면 coverage 증대와 중간체 에너지장벽 변화가 전환 효율 및 제품 분포에 유리하게 작용함을 제시하고 있다. 질량전달 제어를 통한 선택도 변화와 밀접히 연관되어 본 연구에서 H-cell 교반속도, CO2 유량을 통해 조절하는 boundary thickness 결과를 비교함으로써 작동조건과 전극 표면 특성이 CO2 RR 선택도에 미치는 상대적인 기여를 규명할 수 있다. | |
| − | + | =====특허조사===== | |
| − | + | * CO2RR 연구에서 변수 및 주의사항 | |
| + | CO₂공급 방식에 따라 셀 내부의 기체-액체 접촉 메커니즘이 근본적으로 달라지며, 버블링(기포 주입) 방식과 GDE(가스 확산 전극)를 이용한 공급 방식은 기포 크기·기포 상승 속도 등의 다른 유체역학적 변수를 필요로 한다는 점을 여러 특허에서 다룬다. 특히 일부 문서는 기포 주입 방식에서 교반속도, 기포 유량 및 기포 크기 제어가 제품 분포에 직접 영향을 준다고 명시하고 있다. | ||
| + | CO₂ 공급 방식은 측정 결과, 특히 FE와 부분 전류밀도에 큰 영향을 주므로, 실험 프로토콜에 가스 유량, 공급 방식, 교반 속도/흐름 조건을 반드시 기재해야 한다. 또한 동일한 전극·전해질이라도 공급 방식 차이로 결과가 달라질 수 있으므로 비교 연구 시 공급 방식 일치를 권장한다. | ||
| − | + | =====특허 전략 분석===== | |
| + | 지구 대기 중 이산화탄소 농도는 산업화 이전 대비 52% 증가한 423.9 ppm(2023년 기준) 으로 역대 최고치를 기록했으며, 증가 속도 또한 관측 이래 가장 가파른 수준인 연간 3.5 ppm 에 달하고 있다. 이러한 급격한 상승은 단순한 일시적 현상이 아니라 2010년대 이후 꾸준히 가속되고 있는 장기적 추세로, 화석연료 사용 지속과 산불 증가, 그리고 기후 변화로 인한 해양·삼림의 CO₂ 흡수 능력 저하가 복합적으로 작용한 결과다. 이로 인해 지구 온난화가 심화되고 극단적인 기후 현상이 빈번해지며, 인류의 경제적 안보와 생태계의 안정성에도 직접적인 위협을 가하고 있다. 따라서 대기 중 온실가스, 특히 CO₂ 농도를 근본적으로 줄이는 기술적·정책적 노력이 시급히 요구된다. | ||
| + | 그래프에 따르면 이산화탄소 전환(CO₂RR) 관련 특허는 2000년대 초반부터 꾸준히 증가하는 추세를 보이고 있다. 출원년도, 공개년도, 등록년도 모두 전반적으로 상승세를 나타내며, 특히 2020년 이후 급격한 증가가 확인된다. 이는 최근 기후변화 대응과 탄소중립 기술 개발에 대한 관심이 높아지면서 관련 연구개발 및 특허 활동이 활발해졌음을 보여준다. | ||
[[파일:CNL특허.png]] | [[파일:CNL특허.png]] | ||
| − | + | 현재 전 세계적으로 이산화탄소를 유용한 화학 원료로 전환하기 위한 촉매 기술 개발이 활발히 이루어지고 있다. 특히, 최근 한국에너지기술연구원에서는 구리–마그네슘–철 혼합 산화물 기반의 역수성가스전환반응(Reverse Water Gas Shift Reaction) 촉매를 개발하여 400 °C 저온에서도 일산화탄소를 고효율로 생산하는 기술을 보고하였다. 해당 촉매는 상용 구리 촉매 대비 약 1.7배 빠른 생성 속도와 1.5배 높은 수율을 달성하였으며, 메탄 등의 불필요한 부산물 생성 없이 안정적인 전환이 가능하다. | |
| − | 이러한 연구는 구리 기반 비귀금속 촉매를 활용한 저온 CO₂ 전환 기술의 경쟁이 빠르게 심화되고 있음을 의미한다. 따라서 관련 촉매 조성, 층상 구조 제어, 반응 메커니즘 개선에 관한 조기 특허 확보가 기술적 우위를 선점하기 위한 핵심 전략이 될 것으로 판단된다. | + | 이러한 연구는 구리 기반 비귀금속 촉매를 활용한 저온 CO₂ 전환 기술의 경쟁이 빠르게 심화되고 있음을 의미한다. 따라서 관련 촉매 조성, 층상 구조 제어, 반응 메커니즘 개선에 관한 조기 특허 확보가 기술적 우위를 선점하기 위한 핵심 전략이 될 것으로 판단된다. |
| − | + | 이처럼 최근 이산화탄소 전환 촉매 기술이 빠르게 발전함에 따라, 전기화학적 CO₂ 환원반응(CO₂RR)의 성능을 정밀하게 평가하기 위한 전기화학적 측정 기술의 중요성도 함께 부각되고 있다. 전극 소재의 활성, 선택성, 안정성을 체계적으로 비교·분석하기 위해서는 전류-전압 특성, 파라데이 효율, 전하 전달 저항 등 다양한 전기화학적 지표를 정밀하게 측정하고 해석할 수 있는 방법론이 필요하다. 특히, 반응 중계면의 전하 이동과 반응 생성물의 변화를 실시간으로 추적할 수 있는 전기화학 임피던스 분광법(EIS), 선형 스위프 전압법(LSV), 가변 전위 전해(chronoamperometry/chronopotentiometry) 등의 기법이 핵심 분석 도구로 활용되고 있다. | |
| − | + | 이러한 측정 기술의 고도화는 촉매의 실제 반응 거동을 이해하고, 고효율·고선택적 전극 설계를 위한 과학적 근거를 제공함으로써 차세대 CO₂ 전환 기술 개발의 방향성을 제시할 수 있다. | |
| − | 이러한 측정 기술의 고도화는 촉매의 실제 반응 거동을 이해하고, 고효율·고선택적 전극 설계를 위한 과학적 근거를 제공함으로써 차세대 CO₂ 전환 기술 개발의 방향성을 제시할 수 있다. | ||
===개발과제의 기대효과=== | ===개발과제의 기대효과=== | ||
====기술적 기대효과==== | ====기술적 기대효과==== | ||
| − | ◇ 기존 CO₂RR 연구는 촉매 조성, 전해질 종류, 가스 공급 방식, 전극 구조 등 실험 조건의 다양성으로 인해 데이터 비교가 어렵다. 본 연구를 통해 CV, LSV, GC 등의 전기화학적 분석을 통합하여 반응 특성과 선택도에 영향을 미치는 주요 인자를 정량적으로 규명함으로써 반응 표준화 및 객관적 성능 평가 기준을 제시할 수 있다. 표준화된 실험 프로토콜 확립을 통해 데이터 재현성을 확보하며 CO₂RR 연구 간 객관적 비교 및 기술 평가가 가능할 것이다. | + | ◇ 기존 CO₂RR 연구는 촉매 조성, 전해질 종류, 가스 공급 방식, 전극 구조 등 실험 조건의 다양성으로 인해 데이터 비교가 어렵다. 본 연구를 통해 CV, LSV, GC 등의 전기화학적 분석을 통합하여 반응 특성과 선택도에 영향을 미치는 주요 인자를 정량적으로 규명함으로써 반응 표준화 및 객관적 성능 평가 기준을 제시할 수 있다. 표준화된 실험 프로토콜 확립을 통해 데이터 재현성을 확보하며 CO₂RR 연구 간 객관적 비교 및 기술 평가가 가능할 것이다. |
| − | + | ◇ H-Cell 내 교반 속도 및 CO₂ 유량 조절을 통해 전극 주변 Boundary thickness를 제어함으로써, 질량 전달 특성과 반응 속도 간의 상관관계를 규명하여 전달 현상 해석 기술을 확보할 수 있다. 향후 CO₂RR 반응에서의 전극 구조 및 셀 설계 최적화 기술 개발에 기여할 것으로 기대된다. 전해질 내 불순물 농도 변화가 반응 효율 및 생성물 분포에 미치는 영향을 정량적으로 분석함으로써, 전해질 순도 및 반응 환경 최적화의 중요성을 입증할 수 있다. 이를 통해 CO₂를 유용한 화학물질 및 연료로 전환하는 기술의 효율 향상에 기여할 수 있을 것이다. | |
| − | ◇ H-Cell 내 교반 속도 및 CO₂ 유량 조절을 통해 전극 주변 Boundary thickness를 제어함으로써, 질량 전달 특성과 반응 속도 간의 상관관계를 규명하여 전달 현상 해석 기술을 확보할 수 있다. 향후 CO₂RR 반응에서의 전극 구조 및 셀 설계 최적화 기술 개발에 기여할 것으로 기대된다. 전해질 내 불순물 농도 변화가 반응 효율 및 생성물 분포에 미치는 영향을 정량적으로 분석함으로써, 전해질 순도 및 반응 환경 최적화의 중요성을 입증할 수 있다. 이를 통해 CO₂를 유용한 화학물질 및 연료로 전환하는 기술의 효율 향상에 기여할 수 있을 것이다. | ||
====경제적, 사회적 기대 및 파급효과==== | ====경제적, 사회적 기대 및 파급효과==== | ||
| − | ◇ 현재 전 세계적으로 탄소 포집 및 전환(CCU) 기술 시장은 급성장 중이며, 그 중에서도 CO₂RR 기술은 화석연료 기반 공정의 탄소 배출 저감뿐 아니라 고부가가치 화학제품의 생산을 가능하게 한다. 본 연구를 통해 촉매 성능 평가의 신뢰성을 확보하고 반응 조건의 표준화가 이루어진다면, 연구 결과의 재현성이 향상되어 기업 및 연구기관의 기술개발 비용이 절감되고, 상업화에 기여할 수 있을 것이다. 또한 CO₂RR 공정을 통해 탄소배출권 거래제 시장에서 경제적인 이익을 창출할 수 있다. 특히 CO₂를 원료로 하는 연료 및 화학제품 생산 기술은 탄소 순환형 산업구조를 구축함으로써 에너지, 화학 산업 전반의 경쟁력을 강화할 것이다. | + | ◇ 현재 전 세계적으로 탄소 포집 및 전환(CCU) 기술 시장은 급성장 중이며, 그 중에서도 CO₂RR 기술은 화석연료 기반 공정의 탄소 배출 저감뿐 아니라 고부가가치 화학제품의 생산을 가능하게 한다. 본 연구를 통해 촉매 성능 평가의 신뢰성을 확보하고 반응 조건의 표준화가 이루어진다면, 연구 결과의 재현성이 향상되어 기업 및 연구기관의 기술개발 비용이 절감되고, 상업화에 기여할 수 있을 것이다. 또한 CO₂RR 공정을 통해 탄소배출권 거래제 시장에서 경제적인 이익을 창출할 수 있다. 특히 CO₂를 원료로 하는 연료 및 화학제품 생산 기술은 탄소 순환형 산업구조를 구축함으로써 에너지, 화학 산업 전반의 경쟁력을 강화할 것이다. |
| − | + | ◇ CO₂RR 기술은 온실가스인 CO₂를 유용한 자원으로 전환함으로써 탄소 포집·활용 효율을 높이고, 산업계의 친환경 전환과 ESG 경영 강화에 기여할 수 있다. 또한 표준화된 분석 프로토콜 확립을 통해 연구 재현성과 협력 연구를 촉진하여 탄소중립 실현에 중요한 역할을 할 것으로 기대된다. | |
| − | ◇ CO₂RR 기술은 온실가스인 CO₂를 유용한 자원으로 전환함으로써 탄소 포집·활용 효율을 높이고, 산업계의 친환경 전환과 ESG 경영 강화에 기여할 수 있다. 또한 표준화된 분석 프로토콜 확립을 통해 연구 재현성과 협력 연구를 촉진하여 탄소중립 실현에 중요한 역할을 할 것으로 기대된다. | ||
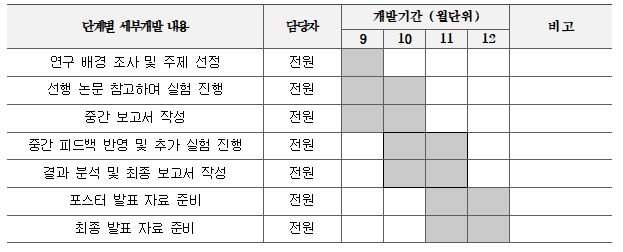
===기술개발 일정 및 추진체계=== | ===기술개발 일정 및 추진체계=== | ||
| 92번째 줄: | 81번째 줄: | ||
[[파일:CNL 개발일정.png]] | [[파일:CNL 개발일정.png]] | ||
====구성원 및 추진체계==== | ====구성원 및 추진체계==== | ||
| − | + | ◇ CO2RR 관련 논문 조사 및 원리 파악(전원) | |
| − | ◇ CO2RR 관련 논문 조사 및 원리 파악(전원) | + | ◇ CO2RR 전극 분석 및 cell 유사성 파악(전원) |
| − | + | ◇ 선행 논문와 현재 cell의 차이점 파악(전원) | |
| − | + | ◇ 선행 논문 참고하여 전류 밀도, FE, ECSA 계산 및 분석(전원) | |
| − | + | ◇ 분석 결과 선행 논문과 일치하는지 확인(전원) | |
| − | ◇ CO2RR 전극 분석 및 cell 유사성 파악(전원) | ||
| − | |||
| − | |||
| − | |||
| − | ◇ 선행 논문와 현재 cell의 차이점 파악(전원) | ||
| − | |||
| − | |||
| − | ◇ 선행 논문 참고하여 전류 밀도, FE, ECSA 계산 및 분석(전원) | ||
| − | |||
| − | |||
| − | |||
| − | ◇ 분석 결과 선행 논문과 일치하는지 확인(전원) | ||
| − | |||
==실험 방법== | ==실험 방법== | ||
| 198번째 줄: | 174번째 줄: | ||
1) H2=50%, CO=50% 인 경우 | 1) H2=50%, CO=50% 인 경우 | ||
| − | [[파일:FL50.png]] | + | [[파일:FL50.png]] |
| − | |||
| − | |||
2) CO=100% 인 경우 | 2) CO=100% 인 경우 | ||
| − | [[파일:FL100.png]] | + | [[파일:FL100.png]] |
| − | |||
| 233번째 줄: | 206번째 줄: | ||
Figure 6. 0, 200, 400, 600 rpm partial Current density of CO vs stirring speed | Figure 6. 0, 200, 400, 600 rpm partial Current density of CO vs stirring speed | ||
| + | |||
[[파일:CNLFE.png]] | [[파일:CNLFE.png]] | ||
| + | |||
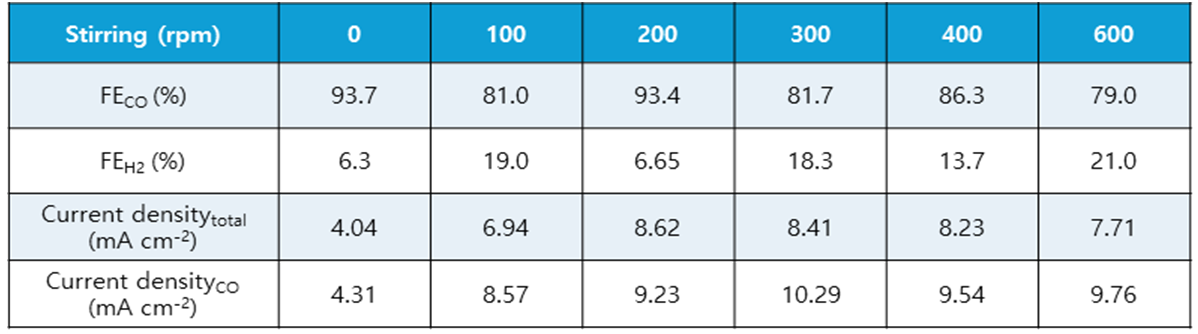
Table 2. Faradaic efficiency of CO and H2, total current density, partial current density of CO vs stirring speed | Table 2. Faradaic efficiency of CO and H2, total current density, partial current density of CO vs stirring speed | ||
| − | |||
Figure 5.는 stirring speed에 따른 CO에 대한 partial current density를 나타낸 그래프이다. Figure 4.를 보면, 600 rpm에서 전극 주변에 소용돌이가 형성되는 것을 확인할 수 있다. 또한, 600 rpm을 초과할 경우 소용돌이가 더욱 커져 전극 표면까지 확장되는 현상이 관찰되었기 때문에, 최대 교반 속도는 600 rpm으로 설정하였다. 이에 따라 0 rpm에서 600 rpm까지 교반 속도를 변화시키며 CO의 부분전류밀도를 측정하였다. | Figure 5.는 stirring speed에 따른 CO에 대한 partial current density를 나타낸 그래프이다. Figure 4.를 보면, 600 rpm에서 전극 주변에 소용돌이가 형성되는 것을 확인할 수 있다. 또한, 600 rpm을 초과할 경우 소용돌이가 더욱 커져 전극 표면까지 확장되는 현상이 관찰되었기 때문에, 최대 교반 속도는 600 rpm으로 설정하였다. 이에 따라 0 rpm에서 600 rpm까지 교반 속도를 변화시키며 CO의 부분전류밀도를 측정하였다. | ||
| − | |||
초기에는 200 rpm 간격으로, 즉 0, 200, 400, 600 rpm에서 측정을 진행하였다. 그 결과, 0–200 rpm 구간에서는 교반 속도가 증가할수록 CO 부분전류밀도가 증가하였지만, 200–600 rpm 구간에서는 교반 속도가 증가할수록 CO 부분전류밀도가 감소하였다. 이는 0–200 rpm에서는 교반 속도 증가에 따라 mass transport가 촉진되고 boundary layer 두께가 감소하여 CO₂RR이 활발해지고, 그 결과 CO 부분전류밀도가 증가하기 때문이다. 반면 200–600 rpm 구간에서는 boundary layer 두께가 계속 감소하더라도 과도한 교반으로 인해 CO₂가 전극 표면에 도달하기 전에 주변으로 제거되어, 결과적으로 CO 부분전류밀도가 감소하게 된다. | 초기에는 200 rpm 간격으로, 즉 0, 200, 400, 600 rpm에서 측정을 진행하였다. 그 결과, 0–200 rpm 구간에서는 교반 속도가 증가할수록 CO 부분전류밀도가 증가하였지만, 200–600 rpm 구간에서는 교반 속도가 증가할수록 CO 부분전류밀도가 감소하였다. 이는 0–200 rpm에서는 교반 속도 증가에 따라 mass transport가 촉진되고 boundary layer 두께가 감소하여 CO₂RR이 활발해지고, 그 결과 CO 부분전류밀도가 증가하기 때문이다. 반면 200–600 rpm 구간에서는 boundary layer 두께가 계속 감소하더라도 과도한 교반으로 인해 CO₂가 전극 표면에 도달하기 전에 주변으로 제거되어, 결과적으로 CO 부분전류밀도가 감소하게 된다. | ||
이러한 분석을 바탕으로, CO에 대한 부분전류밀도가 최대가 되는 교반 속도가 실제로 200 rpm인지 검증하기 위해 추가로 100 rpm과 300 rpm 조건에서 실험을 수행하였다. Figure 6.의 결과에서 확인할 수 있듯이, CO 부분전류밀도는 200 rpm에서 가장 높은 값을 보였다. | 이러한 분석을 바탕으로, CO에 대한 부분전류밀도가 최대가 되는 교반 속도가 실제로 200 rpm인지 검증하기 위해 추가로 100 rpm과 300 rpm 조건에서 실험을 수행하였다. Figure 6.의 결과에서 확인할 수 있듯이, CO 부분전류밀도는 200 rpm에서 가장 높은 값을 보였다. | ||
| − | + | ===Electrocatalytic activity=== | |
- 표면 거칠기 조절 | - 표면 거칠기 조절 | ||
| + | |||
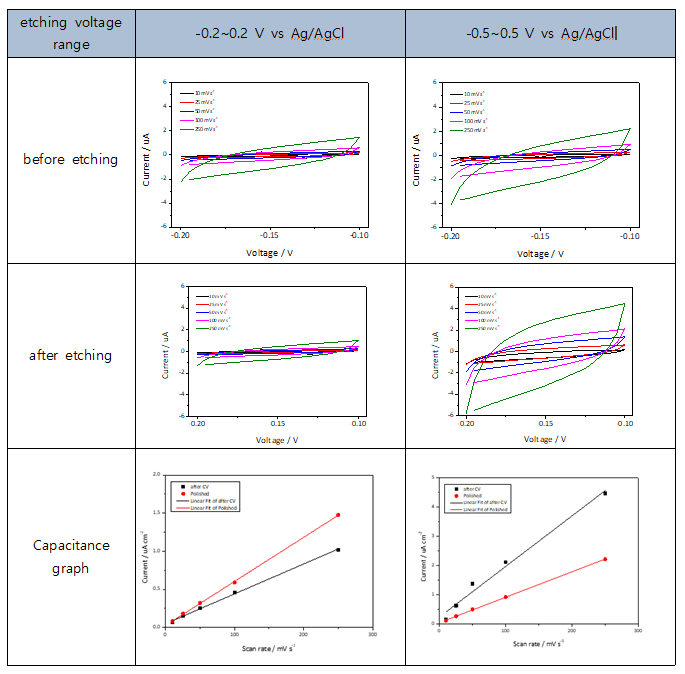
| + | [[파일:ETCH11.png]] | ||
CV 사이클링 방법을 통해 –0.2V ~ +0.2V vs Ag/AgCl 와 -0.5~0.5 V vs Ag/AgCl의 전위로 표면 거칠기를 조절하였다. –0.2V ~ +0.2V vs Ag/AgCl의 전위로 CV 사이클링하여 etching 했을 때, Etching 후의 CV 그래프의 전류 범위가 줄어든 것을 확인할 수 있었다. 또한 Scan rate 별 Polished Ag foil과 CV etched Ag foil의 Capacitance 그래프를 통해 Polished Ag foil이 CV etched Ag foil보다 capacitance가 큰 것을 보아 해당 전압 범위에서는 Ag foil 표면이 잘 깎이지 않은 것을 확인할 수 있다. -0.5~0.5 V vs Ag/AgCl의 전위로 CV 사이클링하여 etching한 경우, Etching 후의 CV 그래프의 전류 범위가 늘어난 것을 확인할 수 있으며 Scan rate 별 Polished Ag foil과 CV etched Ag foil의 Capacitance 그래프를 통해 CV etched Ag foil이 polished Ag foil보다 capacitance가 큰 것을 확인할 수 있다. 이를 통해 -0.5~0.5 V vs Ag/AgCl의 전위로 CV 사이클링하였을 때 Ag foil의 표면이 잘 깎인 것을 알 수 있다. | CV 사이클링 방법을 통해 –0.2V ~ +0.2V vs Ag/AgCl 와 -0.5~0.5 V vs Ag/AgCl의 전위로 표면 거칠기를 조절하였다. –0.2V ~ +0.2V vs Ag/AgCl의 전위로 CV 사이클링하여 etching 했을 때, Etching 후의 CV 그래프의 전류 범위가 줄어든 것을 확인할 수 있었다. 또한 Scan rate 별 Polished Ag foil과 CV etched Ag foil의 Capacitance 그래프를 통해 Polished Ag foil이 CV etched Ag foil보다 capacitance가 큰 것을 보아 해당 전압 범위에서는 Ag foil 표면이 잘 깎이지 않은 것을 확인할 수 있다. -0.5~0.5 V vs Ag/AgCl의 전위로 CV 사이클링하여 etching한 경우, Etching 후의 CV 그래프의 전류 범위가 늘어난 것을 확인할 수 있으며 Scan rate 별 Polished Ag foil과 CV etched Ag foil의 Capacitance 그래프를 통해 CV etched Ag foil이 polished Ag foil보다 capacitance가 큰 것을 확인할 수 있다. 이를 통해 -0.5~0.5 V vs Ag/AgCl의 전위로 CV 사이클링하였을 때 Ag foil의 표면이 잘 깎인 것을 알 수 있다. | ||
| 251번째 줄: | 226번째 줄: | ||
- Electrocatalytic test | - Electrocatalytic test | ||
| + | |||
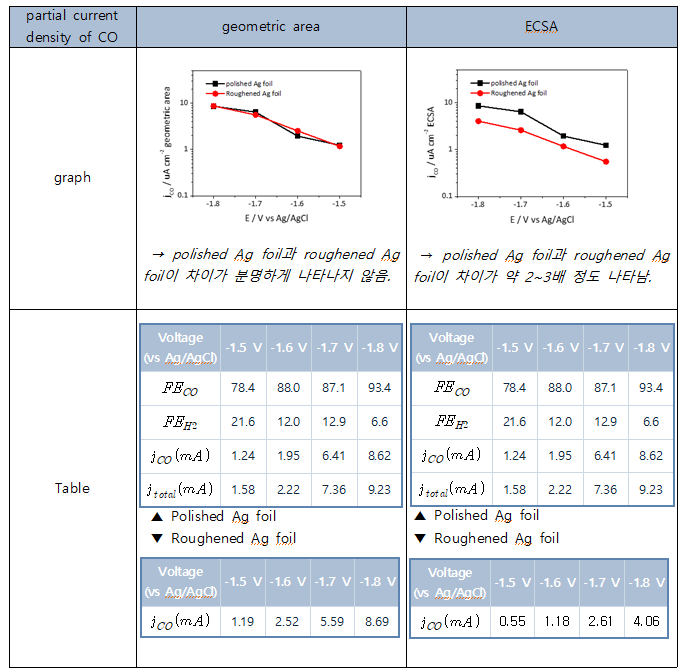
| + | [[파일:ET11.png]] | ||
그래프와 표의 결과를 종합하면, geometric area 기준 CO 부분전류밀도는 polished Ag foil과 roughened Ag foil 간의 차이가 거의 없는 반면, ECSA 기준 CO 부분전류밀도는 roughened Ag foil이 polished Ag foil 대비 약 2–3배 낮은 값을 나타내었다. 이에 대해 다음 두 가지 원인을 고려할 수 있다. | 그래프와 표의 결과를 종합하면, geometric area 기준 CO 부분전류밀도는 polished Ag foil과 roughened Ag foil 간의 차이가 거의 없는 반면, ECSA 기준 CO 부분전류밀도는 roughened Ag foil이 polished Ag foil 대비 약 2–3배 낮은 값을 나타내었다. 이에 대해 다음 두 가지 원인을 고려할 수 있다. | ||
2025년 12월 4일 (목) 01:51 기준 최신판
프로젝트 개요
기술개발 과제
국문 : 전기화학적 CO2 환원반응에 대한 전기화학적 측정 방법에 대한 고찰 영문 : A Review on Electrochemical Measurement Methods for CO2RR
과제 팀명
CNL
지도교수
이두환 교수님
개발기간
2025년 9월 ~ 2025년 12월 (총 4개월)
구성원 소개
서울시립대학교 화학공학과 20228710** 정*은(팀장) 서울시립대학교 화학공학과 20203400** 남*재
서론
개발 과제의 개요
개발 과제 요약
◇ CO2 전기화학적 환원반응(CO2RR)의 반응 특성과 선택도에 영향을 미치는 주요 인자를 규명한다. ◇ 작동전극의 boundary thickness가 CO2RR에 미치는 영향을 분석한다. ◇ CV, LSV, GC 등 다양한 전기화학적 분석 기법을 활용하여 CO2RR 반응 메커니즘을 정량적으로 해석한다. ◇ 전해질 내 불순물의 존재가 CO2RR 효율과 생성물 분포에 미치는 영향을 규명한다. ◇ Ag foil의 ECSA 변화를 정량화하여 CO2RR 활성 및 선택성과의 상관관계를 규명한다.
개발 과제의 배경
◇ CO2 전기화학적 환원 반응은 CO2를 일산화탄소, 메탄, 에틸렌 등과 같은 유용한 화학물질이나 연료로 전환하는 기술로 많은 연구가 이루어졌지만 표준화된 연구의 프로토콜 부재로 인해 촉매 성능을 객관적으로 비교하고 평가하는 데 어려움이 있다. ◇ 촉매의 활성과 선택성은 촉매 자체의 조성과 형태뿐만 아니라 전해질, 전기화학 셀의 유체역학, 촉매 및 전해질의 순도 등 다양한 변수에 의해 영향을 받기 때문에, 재현 가능한 데이터를 얻기 위한 표준화된 절차의 필요성이 대두되고 있다. ◇ 표준화된 촉매 준비 및 셀 작동 조건을 적용하면 객관적인 성능 평가, 데이터 재현성 확보, 연구 효율 증대가 가능할 것이다.
개발 과제의 목표 및 내용
◇ CO2RR working electrode의 boundary thickness를 H-cell 내 stirring 속도 및 CO2 유량 변화를 통해 조절하고, 이에 따른 반응 특성 변화를 규명한다. ◇ CV, LSV, GC 분석 등 다양한 전기화학적 분석 기법을 활용하여 CO2RR 반응 특성 및 생성물 분포를 정밀하게 평가한다. ◇ 전해질 내 불순물의 존재가 CO2RR 반응 효율과 선택도에 미치는 영향을 규명한다. ◇ Ag foil의 ECSA 변화를 정량화하여 CO2RR 활성 및 선택성과의 상관관계를 규명한다.
관련 기술의 현황
관련 기술의 현황 및 분석(State of art)
- 나노 구조 및 결정면 제어 촉매
대다수의 CO2 RR 관련 특허는 특정 생성물에 대한 패러데이 효율과 활성을 높이는 새로운 촉매 구조 또는 조성 개발에 집중되어 있다. C2 이상의 고부가 탄화수소 생성에 특화된 나노 구조 또는 산화물 유래 Cu를 개발한다. 이는 표면에 CO Dimerization에 유리한 특정 격자 변형이나 원자 틈을 유도하여 선택성을 향상시킨다. CO 선택성이 높은 Ag 촉매의 경우, 나노입자의 곡선형 표면이나 edge 부위의 비율을 조절하여 CO 생성에 대한 활성 부위를 극대화하는 기술이 주를 이룬다. 나노 구조 촉매는 제조 공정이 복잡하고, 촉매 표면의 결정면이 불균일하여 성능 평가의 재현성이 낮다는 근본적인 문제가 있다.
- 고압 CO2를 직접 활용하는 반응기 설계 동향
포집된 고압 CO2를 별도 감압 없이 직접 전해반응기로 주입하여 formate 등으로 전환하는 고압 전해 시스템을 제시한다. 본 특허는 상용 Cu 기반의 나노구조 전극을 PPy 등으로 기능화하여 H+ 흡착을 억제하고 CO2 환원 선택도를 향상시키는 전극 설계를 포함하며 고압에서의 CO2 표면 coverage 증대와 중간체 에너지장벽 변화가 전환 효율 및 제품 분포에 유리하게 작용함을 제시하고 있다. 질량전달 제어를 통한 선택도 변화와 밀접히 연관되어 본 연구에서 H-cell 교반속도, CO2 유량을 통해 조절하는 boundary thickness 결과를 비교함으로써 작동조건과 전극 표면 특성이 CO2 RR 선택도에 미치는 상대적인 기여를 규명할 수 있다.
특허조사
- CO2RR 연구에서 변수 및 주의사항
CO₂공급 방식에 따라 셀 내부의 기체-액체 접촉 메커니즘이 근본적으로 달라지며, 버블링(기포 주입) 방식과 GDE(가스 확산 전극)를 이용한 공급 방식은 기포 크기·기포 상승 속도 등의 다른 유체역학적 변수를 필요로 한다는 점을 여러 특허에서 다룬다. 특히 일부 문서는 기포 주입 방식에서 교반속도, 기포 유량 및 기포 크기 제어가 제품 분포에 직접 영향을 준다고 명시하고 있다. CO₂ 공급 방식은 측정 결과, 특히 FE와 부분 전류밀도에 큰 영향을 주므로, 실험 프로토콜에 가스 유량, 공급 방식, 교반 속도/흐름 조건을 반드시 기재해야 한다. 또한 동일한 전극·전해질이라도 공급 방식 차이로 결과가 달라질 수 있으므로 비교 연구 시 공급 방식 일치를 권장한다.
특허 전략 분석
지구 대기 중 이산화탄소 농도는 산업화 이전 대비 52% 증가한 423.9 ppm(2023년 기준) 으로 역대 최고치를 기록했으며, 증가 속도 또한 관측 이래 가장 가파른 수준인 연간 3.5 ppm 에 달하고 있다. 이러한 급격한 상승은 단순한 일시적 현상이 아니라 2010년대 이후 꾸준히 가속되고 있는 장기적 추세로, 화석연료 사용 지속과 산불 증가, 그리고 기후 변화로 인한 해양·삼림의 CO₂ 흡수 능력 저하가 복합적으로 작용한 결과다. 이로 인해 지구 온난화가 심화되고 극단적인 기후 현상이 빈번해지며, 인류의 경제적 안보와 생태계의 안정성에도 직접적인 위협을 가하고 있다. 따라서 대기 중 온실가스, 특히 CO₂ 농도를 근본적으로 줄이는 기술적·정책적 노력이 시급히 요구된다. 그래프에 따르면 이산화탄소 전환(CO₂RR) 관련 특허는 2000년대 초반부터 꾸준히 증가하는 추세를 보이고 있다. 출원년도, 공개년도, 등록년도 모두 전반적으로 상승세를 나타내며, 특히 2020년 이후 급격한 증가가 확인된다. 이는 최근 기후변화 대응과 탄소중립 기술 개발에 대한 관심이 높아지면서 관련 연구개발 및 특허 활동이 활발해졌음을 보여준다.
현재 전 세계적으로 이산화탄소를 유용한 화학 원료로 전환하기 위한 촉매 기술 개발이 활발히 이루어지고 있다. 특히, 최근 한국에너지기술연구원에서는 구리–마그네슘–철 혼합 산화물 기반의 역수성가스전환반응(Reverse Water Gas Shift Reaction) 촉매를 개발하여 400 °C 저온에서도 일산화탄소를 고효율로 생산하는 기술을 보고하였다. 해당 촉매는 상용 구리 촉매 대비 약 1.7배 빠른 생성 속도와 1.5배 높은 수율을 달성하였으며, 메탄 등의 불필요한 부산물 생성 없이 안정적인 전환이 가능하다. 이러한 연구는 구리 기반 비귀금속 촉매를 활용한 저온 CO₂ 전환 기술의 경쟁이 빠르게 심화되고 있음을 의미한다. 따라서 관련 촉매 조성, 층상 구조 제어, 반응 메커니즘 개선에 관한 조기 특허 확보가 기술적 우위를 선점하기 위한 핵심 전략이 될 것으로 판단된다.
이처럼 최근 이산화탄소 전환 촉매 기술이 빠르게 발전함에 따라, 전기화학적 CO₂ 환원반응(CO₂RR)의 성능을 정밀하게 평가하기 위한 전기화학적 측정 기술의 중요성도 함께 부각되고 있다. 전극 소재의 활성, 선택성, 안정성을 체계적으로 비교·분석하기 위해서는 전류-전압 특성, 파라데이 효율, 전하 전달 저항 등 다양한 전기화학적 지표를 정밀하게 측정하고 해석할 수 있는 방법론이 필요하다. 특히, 반응 중계면의 전하 이동과 반응 생성물의 변화를 실시간으로 추적할 수 있는 전기화학 임피던스 분광법(EIS), 선형 스위프 전압법(LSV), 가변 전위 전해(chronoamperometry/chronopotentiometry) 등의 기법이 핵심 분석 도구로 활용되고 있다. 이러한 측정 기술의 고도화는 촉매의 실제 반응 거동을 이해하고, 고효율·고선택적 전극 설계를 위한 과학적 근거를 제공함으로써 차세대 CO₂ 전환 기술 개발의 방향성을 제시할 수 있다.
개발과제의 기대효과
기술적 기대효과
◇ 기존 CO₂RR 연구는 촉매 조성, 전해질 종류, 가스 공급 방식, 전극 구조 등 실험 조건의 다양성으로 인해 데이터 비교가 어렵다. 본 연구를 통해 CV, LSV, GC 등의 전기화학적 분석을 통합하여 반응 특성과 선택도에 영향을 미치는 주요 인자를 정량적으로 규명함으로써 반응 표준화 및 객관적 성능 평가 기준을 제시할 수 있다. 표준화된 실험 프로토콜 확립을 통해 데이터 재현성을 확보하며 CO₂RR 연구 간 객관적 비교 및 기술 평가가 가능할 것이다. ◇ H-Cell 내 교반 속도 및 CO₂ 유량 조절을 통해 전극 주변 Boundary thickness를 제어함으로써, 질량 전달 특성과 반응 속도 간의 상관관계를 규명하여 전달 현상 해석 기술을 확보할 수 있다. 향후 CO₂RR 반응에서의 전극 구조 및 셀 설계 최적화 기술 개발에 기여할 것으로 기대된다. 전해질 내 불순물 농도 변화가 반응 효율 및 생성물 분포에 미치는 영향을 정량적으로 분석함으로써, 전해질 순도 및 반응 환경 최적화의 중요성을 입증할 수 있다. 이를 통해 CO₂를 유용한 화학물질 및 연료로 전환하는 기술의 효율 향상에 기여할 수 있을 것이다.
경제적, 사회적 기대 및 파급효과
◇ 현재 전 세계적으로 탄소 포집 및 전환(CCU) 기술 시장은 급성장 중이며, 그 중에서도 CO₂RR 기술은 화석연료 기반 공정의 탄소 배출 저감뿐 아니라 고부가가치 화학제품의 생산을 가능하게 한다. 본 연구를 통해 촉매 성능 평가의 신뢰성을 확보하고 반응 조건의 표준화가 이루어진다면, 연구 결과의 재현성이 향상되어 기업 및 연구기관의 기술개발 비용이 절감되고, 상업화에 기여할 수 있을 것이다. 또한 CO₂RR 공정을 통해 탄소배출권 거래제 시장에서 경제적인 이익을 창출할 수 있다. 특히 CO₂를 원료로 하는 연료 및 화학제품 생산 기술은 탄소 순환형 산업구조를 구축함으로써 에너지, 화학 산업 전반의 경쟁력을 강화할 것이다. ◇ CO₂RR 기술은 온실가스인 CO₂를 유용한 자원으로 전환함으로써 탄소 포집·활용 효율을 높이고, 산업계의 친환경 전환과 ESG 경영 강화에 기여할 수 있다. 또한 표준화된 분석 프로토콜 확립을 통해 연구 재현성과 협력 연구를 촉진하여 탄소중립 실현에 중요한 역할을 할 것으로 기대된다.
기술개발 일정 및 추진체계
구성원 및 추진체계
◇ CO2RR 관련 논문 조사 및 원리 파악(전원) ◇ CO2RR 전극 분석 및 cell 유사성 파악(전원) ◇ 선행 논문와 현재 cell의 차이점 파악(전원) ◇ 선행 논문 참고하여 전류 밀도, FE, ECSA 계산 및 분석(전원) ◇ 분석 결과 선행 논문과 일치하는지 확인(전원)
실험 방법
전해질 불순물 제거
① 0.1M KHCO3 (aq)를 1000 mL 비커에 stirring 하여 준비한다. ② working electrode, counter electrode 각각에 carbon rod를 꽂고, 전해질에 담가서 고정한다. ③ 24 h 동안 0.1 mA의 전류를 흘려주어 전해질 속 불순물을 제거한다.
CO2RR 실험
① 전해질 sacrificing 과정 이후에 working electrode를 측정하고자 하는 Ag foil로 연결한다. ② H-cell 양쪽에 CO2를 50 cc/min으로 30분간 purging 한다. ③ CO2 유량을 10 cc/min으로 줄이고, potentiostat 장치에 연결하여 LSV를 5번 측정한다. ➃ 측정된 LSV를 바탕으로 원하는 전압을 설정하여 Chronoamperometry를 1시간동안 걸어주면서 GC 장치를 4번 반복하여 실행한다.
boundary thickness 조절
Boundary thickness란 전극 표면과 bulk 전해질 사이에서 농도 구배(concentration gradient)가 형성되는 영역의 두께를 의미한다. 전해질과 전극 사이의 질량 전달이 원활하여 CO₂가 충분히 공급되는 경우 boundary thickness는 얇아지며, 이때 전극 표면의 CO₂ 농도가 높게 유지되어 반응 속도와 전류밀도가 증가한다. 반대로 boundary thickness가 두꺼워지면 CO₂ 공급이 제한되고 전극 표면의 CO₂ 농도가 감소하여 전체 전류밀도가 저하되거나 수소 발생 등 부반응의 비율이 증가할 수 있다. 따라서 CO₂RR에서 boundary thickness를 얇게 유지하는 것은 높은 선택도와 반응 효율을 확보하는 데 매우 중요하다. Boundary thickness에 영향을 미치는 주요 요인으로는 CO₂ flow rate, stirring speed, 확산계수(diffusion coefficient), CO₂ 용해도(solubility) 등이 있으며, 이러한 인자들을 적절히 제어함으로써 CO₂ 공급 거동을 최적화하고 반응 성능을 향상시킬 수 있다.
CO2 flow rate
선행 연구에 따르면, CO2 유량을 10–20 sccm 범위에서 공급했을 때 가장 우수한 CO₂RR 성능을 보였다고 보고되어 있으므로, CO2 유량을 10-20 sccm 범위 내에서 조절하여 실험을 진행할 예정이다.
stirrring speed
H-cell 내의 stirring speed를 조절함으로써 boundary thickness를 조절할 수 있다. stirring speed를 너무 약하게 할 경우, boundary thickness가 두꺼워져 CO2 공급이 원활하지 않아지고, stirring speed를 너무 강하게 할 경우, boundary thickness는 얇아지지만, CO2가 반응하기도 전에 떨어져 오히려 효율을 낮출 수 있는 문제점이 있다. 따라서 적당한 stirring speed를 갖는 것이 중요하다.
CO2 solubility
전해질 속에 CO2를 충분히 녹이기 위해 CO2RR 전, CO2를 30분간 purging한다.
전기화학촉매 TEST
전기화학 촉매의 성능을 평가할 때 가장 흔히 사용되는 지표는 Faradaic efficiency(FE)와 partial current density이다. 그러나 이러한 값들은 촉매의 고유한 활성뿐만 아니라 working electrode로 사용된 촉매의 표면적, 분산도 등등 물리적 요인에 의해서도 크게 영향을 받을 수 있다. 따라서 geometric area 기준의 FE 또는 partial current density만으로 촉매 우수성을 판단할 경우, 실제로는 촉매가 뛰어난 것이 아니라 촉매 표면적이 넓거나 분산이 잘 이루어져 있었기 때문일 가능성도 존재한다. 이러한 이유로 촉매 자체의 고유 성능을 비교 및 평가하기 위해서는 ECSA를 산정하여 정규화하는 과정이 반드시 필요하다.
Ag foil
- Polished Ag foil
전처리를 하지 않은 Ag foil은 불순물이 있으므로, 이를 제거하기 위하여 사포로 표면을 polished 한다. 이때, 선행논문을 참고하여 500~600 grit 사포를 이용하여 전처리를 진행하였다.
- Roughened Ag foil
Roughened Ag foil은 평탄한 Ag foil에 전기화학적 산화–환원 사이클을 반복적으로 적용하여 표면을 거칠게 만든 전극을 의미한다. 반복적인 산화·환원 반응을 통해 Ag 표면의 미세 구조가 변화하여 거칠기가 증가하게 된다.
Roughened Ag foil은 다음과 같은 과정으로 제작하였다.
① 전해질 sacrificing 과정을 마친 후, working electrode를 planar Ag foil로 연결한다. ② H-cell 양쪽 챔버에 Ar을 50 cc/min으로 30분간 purging한다. ③ Ar 유량을 10 cc/min으로 조정하고, potentiostat에 연결하여 –0.5 ~ 0.5 V vs. Ag/AgCl 범위의 전위를 10회 반복 인가하여 표면 거칠기를 유도한다.
Capacitive Current vs Scan rate
전기화학적으로 사이클링된 Ag 전극의 표면 거칠기(surface roughness)는 polished Ag foil과 비교하여, 두 전극의 이중층 전하용량(double layer capacitance) 비를 통해 산정하였다.
- Scan rate에 따른 CV test
이중층 전하용량은 Faradaic 반응이 일어나지 않는 전위 범위에서, scan rate을 점차 증가시키며 측정한 충전 전류(charging current)를 기반으로 결정하였다.
실험 방법은 다음과 같다.
① 전해질 sacrificing 과정을 마친 후, working electrode를 polsihed/roughened Ag foil로 연결한다.
② H-cell 양쪽 챔버에 Ar을 50 cc/min으로 30분간 purging한다.
③ Ar 유량을 10 cc/min으로 감소시킨 뒤, potentiostat에 연결하여 –0.2 ~ 0.1 V vs. Ag/AgCl 범위의 전위를 안정화될 때까지 충분히 반복한 후, CV를 측정한다.
④ scan rate을 10, 25, 50, 100, 250 mV/sec로 변화시키며 반복하여 CV test를 진행한다.
- Cdl, Cs
CV 측정에서 –0.1 V vs. Ag/AgCl에서의 전류를 각 scan rate별로 기록하고, 이를 일차 함수로 나타낸다. 이때의 기울기가 바로 이중층 정전용량(Cdl)과 비정전용량(Cs)이다. 이때, Cs는 polished Ag foil에서 측정한 값이며, Cdl은 CV로 electrochemically etched Ag foil에서 얻어진 값이다.
- ECSA 계산
위의 Cs, Cdl을 바탕으로 다음과 같은 식을 이용하여 ECSA를 계산할 수 있다.
계산한 ECSA과 아래의 식을 바탕으로 geometric area에 대한 partial current density를 ECSA에 대한 partial current density of CO로 환산할 수 있다.

계산한 ECSA과 아래의 식을 바탕으로 geometric area에 대한 partial current density를 ECSA에 대한 partial current density로 환산할 수 있다.
결과 및 평가
전해질 불순물 제거
Boundary thickness
CO2 flow rate
1) H2=50%, CO=50% 인 경우
2) CO=100% 인 경우
3) CO2 flow rate이 10 sccm일 때, 흐르는 전류
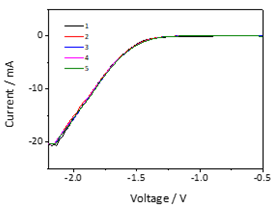
Figure 3. LSV graph
Figure 3에서 확인할 수 있듯이, CO₂를 10 sccm으로 공급할 때 –0.5 ~ –2.2 V vs Ag/AgCl 구간에서 측정된 환원 전류는 최대 약 20 mA에 불과하다. 반면, 동일 조건에서 공급된 CO₂가 모두 소모되기 위해 필요한 최소 전류는 1435 mA로 계산된다. 따라서 CO₂RR 동안 CO₂는 완전히 소모되지 않으며 충분히 공급되고 있어, 질량전달 한계가 발생하지 않는다는 것을 확인할 수 있다. 또한 CO₂ 유량을 10 sccm 이상으로 증가시키는 것은 불필요할 뿐만 아니라, 과도한 CO₂ 공급은 GC 분석 시 생성된 CO 또는 H₂의 농도를 상대적으로 희석시켜 생성량이 실제보다 적게 측정되는 문제를 초래할 수 있다. 이러한 이유로 CO₂ 유량을 10 sccm 이상으로는 증가시키지 않았다. 더 나아가, 선행 연구에서도 CO₂ 유량을 10–20 sccm 범위에서 공급했을 때 가장 우수한 CO₂RR 성능을 보인다고 보고되어 있으므로, 본 연구에서도 CO₂ 유량을 10 sccm 이하로 낮추지 않았다.
Stirring speed
Figure 4. H-cell of 600 rpm stirring
Figure 5. 0, 200, 400, 600 rpm partial Current density of CO vs stirring speed
Figure 6. 0, 200, 400, 600 rpm partial Current density of CO vs stirring speed
Table 2. Faradaic efficiency of CO and H2, total current density, partial current density of CO vs stirring speed
Figure 5.는 stirring speed에 따른 CO에 대한 partial current density를 나타낸 그래프이다. Figure 4.를 보면, 600 rpm에서 전극 주변에 소용돌이가 형성되는 것을 확인할 수 있다. 또한, 600 rpm을 초과할 경우 소용돌이가 더욱 커져 전극 표면까지 확장되는 현상이 관찰되었기 때문에, 최대 교반 속도는 600 rpm으로 설정하였다. 이에 따라 0 rpm에서 600 rpm까지 교반 속도를 변화시키며 CO의 부분전류밀도를 측정하였다. 초기에는 200 rpm 간격으로, 즉 0, 200, 400, 600 rpm에서 측정을 진행하였다. 그 결과, 0–200 rpm 구간에서는 교반 속도가 증가할수록 CO 부분전류밀도가 증가하였지만, 200–600 rpm 구간에서는 교반 속도가 증가할수록 CO 부분전류밀도가 감소하였다. 이는 0–200 rpm에서는 교반 속도 증가에 따라 mass transport가 촉진되고 boundary layer 두께가 감소하여 CO₂RR이 활발해지고, 그 결과 CO 부분전류밀도가 증가하기 때문이다. 반면 200–600 rpm 구간에서는 boundary layer 두께가 계속 감소하더라도 과도한 교반으로 인해 CO₂가 전극 표면에 도달하기 전에 주변으로 제거되어, 결과적으로 CO 부분전류밀도가 감소하게 된다. 이러한 분석을 바탕으로, CO에 대한 부분전류밀도가 최대가 되는 교반 속도가 실제로 200 rpm인지 검증하기 위해 추가로 100 rpm과 300 rpm 조건에서 실험을 수행하였다. Figure 6.의 결과에서 확인할 수 있듯이, CO 부분전류밀도는 200 rpm에서 가장 높은 값을 보였다.
Electrocatalytic activity
- 표면 거칠기 조절
CV 사이클링 방법을 통해 –0.2V ~ +0.2V vs Ag/AgCl 와 -0.5~0.5 V vs Ag/AgCl의 전위로 표면 거칠기를 조절하였다. –0.2V ~ +0.2V vs Ag/AgCl의 전위로 CV 사이클링하여 etching 했을 때, Etching 후의 CV 그래프의 전류 범위가 줄어든 것을 확인할 수 있었다. 또한 Scan rate 별 Polished Ag foil과 CV etched Ag foil의 Capacitance 그래프를 통해 Polished Ag foil이 CV etched Ag foil보다 capacitance가 큰 것을 보아 해당 전압 범위에서는 Ag foil 표면이 잘 깎이지 않은 것을 확인할 수 있다. -0.5~0.5 V vs Ag/AgCl의 전위로 CV 사이클링하여 etching한 경우, Etching 후의 CV 그래프의 전류 범위가 늘어난 것을 확인할 수 있으며 Scan rate 별 Polished Ag foil과 CV etched Ag foil의 Capacitance 그래프를 통해 CV etched Ag foil이 polished Ag foil보다 capacitance가 큰 것을 확인할 수 있다. 이를 통해 -0.5~0.5 V vs Ag/AgCl의 전위로 CV 사이클링하였을 때 Ag foil의 표면이 잘 깎인 것을 알 수 있다. 따라서 –0.5~0.5 V vs Ag/AgCl로 CV etching을 해야 표면이 잘 깎이므로 이후 CO2RR 실험에서 roughened Ag foil은 해당 전압에서 진행하였다.
- Electrocatalytic test
그래프와 표의 결과를 종합하면, geometric area 기준 CO 부분전류밀도는 polished Ag foil과 roughened Ag foil 간의 차이가 거의 없는 반면, ECSA 기준 CO 부분전류밀도는 roughened Ag foil이 polished Ag foil 대비 약 2–3배 낮은 값을 나타내었다. 이에 대해 다음 두 가지 원인을 고려할 수 있다. 첫 번째로, CCV etching 과정에서 사용된 전해질의 영향이다. 본 실험에서는 0.1 M KHCO₃를 전해질로 사용하여 CV etching을 진행하였다. 그러나 일반적으로는 1 M KCl에서 etching을 수행하는 것이 보편적이며, 이에 비해 본 실험 조건은 전해질 농도가 낮았을 가능성이 있다. 또한 KHCO₃에는 탄산이온이 존재하므로, 환원 전위 영역에서 Ag foil 표면에 산소 혹은 탄소 기반 불순물이 환원·도출되었을 가능성도 존재한다. 따라서 전기화학적으로 안정한 KCl을 전해질로 사용하였다면 etching 효율이 상대적으로 더 높았을 가능성이 있다. 두 번째로, CO₂RR을 저전압 영역에서 수행하지 못한 실험 조건의 영향이다. GC 검출 한계 때문에 저전압 영역에서 생성되는 CO의 양이 매우 적어 분석이 어려웠고, 그 결과 가장 낮은 반응 전위가 –1.5 V vs Ag/AgCl로 설정되었다. 즉, 본 실험은 상대적으로 고전압 영역에서 수행되었으며, 이 영역에서는 물질전달 저항이 커져 polished Ag foil과 roughened Ag foil 간 성능 차이가 확대된다. 반면 저전압 영역에서는 반응 속도가 느리므로 물질전달 저항의 영향이 상대적으로 미미하며, 두 전극 간 차이가 작게 나타날 것으로 예상된다. 따라서 –1.5 V vs Ag/AgCl 이하의 더 낮은 전압 영역에서 CO₂RR을 수행할 수 있다면, ECSA 기준 CO 부분전류밀도는 polished Ag foil과 roughened Ag foil 간의 차이가 현재보다 더 작아질 것으로 기대된다.
포스터
관련사업비 내역서
참고문헌
1) Lee, J., et al. “Recent Advances in CO₂ Electroreduction Catalysts and Mechanistic Insights.” Chemical Engineering Research and Design (2024). [1].
2) Zhang, X., et al. “Atomic-Level Insights into CO₂ Reduction on Metal Catalysts.” Nature Communications 13, no. 7124 (2022). [2].
3) World Intellectual Property Organization (WIPO). Catalyst for Electrochemical Reduction of Carbon Dioxide. Patent WO2023042043A1. [3].
4) Clark, E. L., A. T. Bell, J. K. Nørskov, and K. Chan. 2018. “Standards and Protocols for Data Acquisition and Reporting for Studies of the Electrochemical Reduction of Carbon Dioxide.” Catalysis Science & Technology 8 (20): 5881–5893. [4].
5) Clark, E. L., A. T. Bell, J. K. Nørskov, and K. Chan. 2018. “Standards and Protocols for Data Acquisition and Reporting for Studies of the Electrochemical Reduction of Carbon Dioxide.” ACS Catalysis 8: 6560–6570. [5].
6) US Patent Application No. US12/846,002. Electrochemical Production of Synthesis Gas from Carbon Dioxide. Publication No. US20110114504A1. Filed July 29, 2010, and published May 19, 2011.
7) KIPRIS.“특허정보검색서비스.” Korea Intellectual Property Rights Information Service. [6].
8) 통계청. “특허 출원 및 등록 현황.” 국가통계포털 KOSIS. [7].
9) TJB 대전방송. “400℃ 저온에서 CO₂ 전환 가능한 촉매 개발.” TJB 뉴스, 2025년. [8].
10) 동아사이언스. “한국에너지기술연구원, 구리–마그네슘–철 혼합 산화물 기반 CO₂ 전환 촉매 개발.” 동아사이언스, 2025년. [9].
11) 연합뉴스. “탄소 포집·활용 기술 가속화…CO₂ 전환 촉매 연구 활발.” 연합뉴스, 2025년 10월 16일. [10].