"김정현키즈"의 두 판 사이의 차이
Uosche2524 (토론 | 기여) (→수산화 나트륨 당량에 따른 바닐린의 산화 성능 분석) |
Uosche2524 (토론 | 기여) (→수산화 나트륨 당량에 따른 바닐린의 산화 성능 분석) |
||
| 235번째 줄: | 235번째 줄: | ||
[[파일:수나당.jpg|400픽셀|]] | [[파일:수나당.jpg|400픽셀|]] | ||
| − | + | - 위 그래프를 보면 알 수 있듯이, 수산화 나트륨의 당량이 증가할수록, 바닐린의 전환율 및 바닐산 선택성이 동시에 증가하는 것을 알 수 있다. | |
| − | + | ||
| + | - 수산화 나트륨의 양이 증가하면서 알카리성 용액 내 OH 이온의 양이 증가하게 되고, 이 OH 이온은 바닐린을 공격해서 두 개의 수산기가 존재하는 gem-diol 형태로 변환시킨다. | ||
[[파일:수나당2.jpg]] | [[파일:수나당2.jpg]] | ||
- 그리고 이렇게 생성된 gem-diol 형태의 중간체는, 금속 활성점에 의해 형성된 활성 산소종과 반응해서 최종적으로 바닐산으로 산화되며, 형성된 바닐산이 촉매 활성점과 탈착되며 바닐산으로의 전환 반응이 마무리되는 것으로 생각할 수 있었다. | - 그리고 이렇게 생성된 gem-diol 형태의 중간체는, 금속 활성점에 의해 형성된 활성 산소종과 반응해서 최종적으로 바닐산으로 산화되며, 형성된 바닐산이 촉매 활성점과 탈착되며 바닐산으로의 전환 반응이 마무리되는 것으로 생각할 수 있었다. | ||
| + | |||
- 즉, 수산화 나트륨의 당량이 증가하면서 gem-diol 형태로 변환되는 바닐린의 수가 증가하게 되고, 이러한 중간체가 활성 산소종과 반응해서 더 높은 바닐산의 선택성으로 이어진다고 해석이 가능했다. | - 즉, 수산화 나트륨의 당량이 증가하면서 gem-diol 형태로 변환되는 바닐린의 수가 증가하게 되고, 이러한 중간체가 활성 산소종과 반응해서 더 높은 바닐산의 선택성으로 이어진다고 해석이 가능했다. | ||
2025년 12월 3일 (수) 20:31 판
프로젝트 개요
기술개발 과제
국문 : 금 탐지 촉매를 활용한 바닐린 기반 단량체들간의 선택도 조절
영문 : Selectivity Control of Vanillin-Based Monomers Using Gold-Deposition Catalysts
과제 팀명
김정현키즈
지도교수
김정현 교수님
개발기간
2025년 9월 ~ 2025년 12월 (총 4개월)
구성원 소개
서울시립대학교 화학공학과 20203400** 이**(팀장)
서울시립대학교 화학공학과 20203400** 조**
서론
개발 과제의 개요
개발 과제 요약
◇ 현재 국제사회는 화석 자원 의존적 경제구조에서 벗어나 탈탄소 경제체제로의 전환을 추진 중
◇ 산림 바이오매스의 주요 구성성분 중 하나인 리그닌은, 탈탄소 경제 체제로의 전환에 매우 큰 주목을 받고 있음
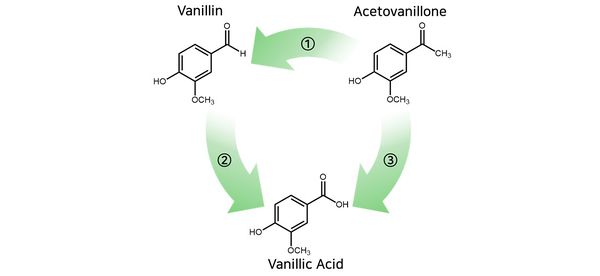
◇ 리그닌으로부터 추출 가능한 바닐린 기반 유도체인 바닐린, 바닐산, 아세토바닐론은 서로 전환 가능하며, 이중 바닐린, 바닐산은 향료, 의료 등의 다양한 산업에서 활용 가능성이 높음
◇ vanillin의 전환을 금을 활용한 촉매를 사용하여 높은 vanillic acid의 선택도를 얻는 것을 목표로 함
개발 과제의 배경
◇ 세계적으로 탄소배출을 줄이려는 정책이 확산되고 있고, 화석 원료를 통한 단량체를 바이오 기반 원료로 대체해야 할 필요성을 느끼고 있음.
◇ 우리나라의 경우, 대통령 직속 탄소중립 녹생성장 위원회를 발족하고, 2023년 4월에는 탄소 중립, 녹색 성장 기본계획을 발표하면서 2030년까지 탄소 배출량을 40% 감축하고자 하는 목표를 설정하며 본격적으로 탈탄소 기반 경제체제 구현을 위한 준비를 진행 중임.
◇ 산림바이오매스의 주요 구성 성분 중 하나인 리그닌은, 산림바이오매스를 활용한 친환경 소재화 기술 개발의 필요성 증가에 매우 적합한 물질로 최근 들어 많은 주목을 받고 있음.
◇ 리그닌으로부터 추출 가능한 단량체인 바닐린, 바닐산은 식품, 향료, 의약용품 등 다양한 분야에서 활용될 수 있으며, 이러한 이유로 인해 높은 수요가 예측되는 고부가가치의 물질임.
◇ 리그닌으로부터 추출가능한 바닐린 기반 단량체로는 아세토바닐론, 바닐린, 바닐산이 있으며, 위 세 가지 물질은 작용기 치환을 통해 서로 전환이 가능하다는 특징이 존재함.
◇ 이번 과제를 통해서, 바닐린 기반 단량체 간의 전환을 위한 최적의 반응 기술을 찾아 고부가가치 물질로의 전환 가능성을 평가하고자 함.
◇ 이를 위해서는 환경적, 정책적, 자원성에서 선택적으로 회수 가능한 공정 최적화를 개선할 필요가 있음.
그림 1. 바닐린 기반 단량체들간의 전환 메커니즘
개발 과제의 목표 및 내용
◇ 바닐린으로부터 바닐산을 얻어내는 반응은 섬세한 반응 조건의 설정 및 반응 적합성이 뛰어난 촉매를 알아내는 것이 중요하다. 이러한 과정을 연구하기 위해 관련된 관련 기술 및 특허들을 확인한다.
◇ Au촉매(Au/TiO2, Au/CuO_TiO2 등)을 이용하여 바닐린으로부터 바닐산을 고수율 및 높은 선택성으로 얻는 것이 가능한지 확인해 본다.
◇ 그렇게 찾은 촉매를 이용하여 온도, 압력 등의 환경에서 최적화를 진행한다.
◇ 침적침전법(Deosition-Precipitation) 방식을 통해 합성한 촉매를 TEM, SEM, XRD, XPS등 다양한 분석기기를 통해 분석해 촉매의 특징을 규명한다.
관련 기술의 현황
관련 기술의 현황 및 분석(State of art)
- 전 세계적인 기술현황
◇ Oxidation of Vanillin with Supported Gold Nanoparticles
- 위의 논문에서는 수용매와 압력 산소(5bar)의 친환경 조건에서 금 나노 입자 촉매를 사용하여 바닐린(vanillin)을 바닐산(vanillic acid)로 선택적으로 산화하는 방법을 연구한 논문이다. 촉매와 지지체로는 Au/Al2O3-DIE, Au/Al2O3-DPU와 Au/TiO2를 사용하였다. NaOH 3 당량, 80 °C, 30분에서 전환율/선택도는 각각 93%/≥99%, 88%/≥99%, 35%/≥99% 이었다. 특히, Au/Al2O3-DIE를 사용하였을 때 높은 전환과 ≥99%의 선택도를 동시에 달성하여 가장 좋은 결과를 얻을 수 있었다. 전환율과 선택도의 향상에는 강염기를 넣어준 것이 결정적이었고, NaOH의 당량을 2에서 3, 4로 늘리면 전환율이 19%에서 90%로 상승하였고, 선택도도 83%에서 ≥99%로 개선되었다. 이러한 NaOH에 대한 설명으로는 다음과 같이 설명한다. 염기가 존재하에 바닐린이 물과 반응하여 중간체를 더 형성하여 바닐산으로의 산화가 수월해지고, 생성된 바닐산과 페놀성 OH는 염기에 의해 탈프론톤화되어 금 촉매 표면에 강하게 달라붙지 않는다. 그렇게 되어 촉매를 보호하고 활성시킨다. 마지막으로 염기가 충분하여 분해되는 라디칼 경로가 줄어들고, 원하는 바닐산으로 만들어지는 반응으로 전환된다.
◇ Synergistic Effect of Au−Cu Alloy Nanoparticles on TiO2 for Efficient Aerobic Catalytic Oxidative Desulfurization
- 위의 논문에서는 TiO2 지지체 위에 금 구리 합금 촉매(AuCu/TiO2)를 제작하여, 공기를 산화제로 사용하는 방식으로 DBT류 황화물을 선택적 산화를 통해 sulfone으로 바꾸는 황을 제거하는 방법을 설명한다. 핵심으로 설명하고 있는 것은 금과 구리를 섞은 합금 효과이다. 두 금속이 붙어 있게 되면 전자가 살짝 이동하게되고, 산소가 잘 붙고 더 활성화 되기 쉬운 표면이 된다. 이를 통해 Au/TiO2나 Cu/TiO2 보다 훨씬 잘 반응하게 된다. 생성물은 surfone(DBTO2) 하나로 깔끔하게 나왔고, 촉매를 여러 번(6회 이상) 다시 사용하여도 90%대 성능을 유지하였다.
◇ Selective oxidation of 5-hydroxymethyl-2-furfural using supported gold–copper nanoparticles
- 위의 논문에서는 HMF(5-hydroxymethyl-2-furfural)을 FDCA(2,5-furandicarboxylic acid)로 산화하는 과정에서 기존 Au 촉매는 비활성화 등의 문제가 존재하여 진행한 연구이다. 그렇게 연구한 촉매 TiO2 지지체 위에 담지한 Au-Cu 합금 나노입자 촉매가 기존의 단일 Au 촉매보다 활성, 선택성, 내구성의 부분에서 모두 우수하다. 이러한 이유로 Au 단일 촉매는 평균 6.6nm에 비해 Au-Cu 합금은 4.4nm로 약 30% 더 작은 입자의 크기를 가져, 활성점 접근성과 선택적 산화를 유리하게 만든다고 설명한다. 5회의 재사용 후에도 활성도와 선택성을 유지하였다.
- 특허조사
◇ 금 입자를 포함하는 산화 촉매(Oxidation catalyst comprising gold particles)
- 본 특허는 망간을 함유하는 티탄산화물 및 상기 망간을 함유하는 티탄산화물에 담지된 입자상의 금을 포함하는 산화 촉매를 활용해서 휘발성 유기화합물(VOC) 및 일산화탄소 군에서 하나 이상 선택되는 대기 오염물질을 효과적으로 제거할 수 있다고 주장했다. 위 특허에서, 합성한 망간_금 산화 촉매에서 금이 직경 1내지 5nm인 나노입자 형태로 포함되어있다고 말하고 있으며, 총 중량 기준으로는 0.1 내지 1.5 중량 %로 담지되어 있음을 확인했다고 한다.
그림 2. 합성한 산화 촉매의 투과전자현미경 이미지
◇ 지지된 금-NP 및 니켈 산화물 촉매 및 이를 이용한 메틸 메타크릴레이트 제조 방법(supported gold-np and nickel oxide catalyst and method for producing methyl methacrylate using such)
- 본 특허는 메타크롤레인의 메틸 메타크릴레이트로의 산화 에스테르화 반응을 위해서 0.8mm의 평균 직경을 가지는 지지체에다가 니켈 산화물과 금 입자를 담지시켜서 만든 산화 촉매를 활용했다. 위 특허에 따르면, 담지된 금 입자의 경우 12nm 미만의 평균 직경과 +/- 4nm의 표준 편차를 갖는 촉매를 합성할 수 있다고 주장하며, 위 촉매의 금 나노입자를 활용해서 99% 이상의 메틸 메타크릴레이트 선택도를 얻을 수 있다고 한다.
◇ 팔라듐-금-구리 촉매를 사용하는 비닐 아세테이트의 제조방법(Vinyl acetate process utilizing apalladium-gold-copper catalyst)
- 본 특허는 반응물인 에틸렌, 산소 및 아세트산과 할로겐 비 함유 구리 화합물을, 촉매 효과량의 팔라듐, 금 및 구리 금속이 다공성 표면에 침착된 다공성 지지체를 포함하는 촉매와 접촉시킴을 포함하는 반응물로서 에틸렌, 산소 및 아세트산을 반응시켜 비닐 아세테이트를 제조하는 방법을 제시해준다. 위 특허에 따르면, 지지체상에 팔라듐, 금 또는 구리를 침윤시키기 위해서 수용성 금속 화합물 용액을 활용해서 팔라듐, 금, 구리 가 침착되도록 처리하는 방식을 선택하였으며, 이 방식은 여러 논문들에서도 채택되는 보편적인 합성 방식이다. 위 특허를 통해서 촉매 내 금 원소의 총량이 최종 촉매에 요구되는 양과 동일하도록 수용성 금 염의 용액을 촉매에 침윤시키는 방법에 대해 참고할 수 있었다.
- 특허전략
◇ 선행 조사 특허들에서는 기상 산화 및 석유화학 공정을 중심으로 금 입자 크기와 담지량, 일반적 침윤 합성 방식 등을 넓게 포섭하고 있다.
◇ 또한 대부분의 특허들에서는 금 나노입자 탐지에 대해 집중적으로 다루고 있으며, 이번 연구 주제인 바닐린의 선택적 산화에 금 나노입자를 활용한 특허는 발견하지 못했다.
◇ 이러한 점을 파고들어, 이번 연구 주제의 특허 전략은 액상에서의 바이오유래 바닐린의 선택적 산화를 주 용도로 특정하고, 추가적으로 금, 구리 이중 접합 촉매 합성에서 우레아 기반 pH 제어 및 광환원과 고온 소성의 후처리 제조 공정을 선택해서 높은 바닐산 선택성 및 재사용성을 확보한 차별화된 촉매 합성법을 제시하는 것을 목표로 하고 있다.
◇ 이렇게 용도, 조성, 합성 방법의 삼중 차별화를 통해서 확실한 분석이 힘든 기상 산화 분야의 혼잡 영역을 피하면서, 구조-성능의 상관관계를 수치 범위 및 분석지표로 뒷받침하여 권리 범위의 실효성을 극대화하고자 한다.
개발과제의 기대효과
기술적 기대효과
◇ 물, 산소 기반 그린 공정의 강화
- 주요 재료는 물(혹은 물-혼합용매) 와 공기, 염기로 유해한 산화제를 사용하지 않는다. 그렇기에 유기 폐용매나 후처리 과정에서 경제적 및 환경적 이점을 챙길 수 있다.
◇ 데이터 기반 최적화
- 합성되는 환경으로는 온도, 압력 등 여러 가지 요소가 존재한다. 이러한 요소들을 최적화하거나 경향성을 분석하여, 비슷한 실험에서 실험의 수를 줄이고 시간을 절약할 수 있다.
경제적, 사회적 기대 및 파급효과
◇ 바이오매스의 고부가가치화
- 바이오매스인 리그인을 고부가가치인 바닐산으로 전환함으로써 폐기물을 감축하고, 탄소배출을 줄일 수 있다. 실제로 바닐산은 식품, 향료, 의약, 헬스케어와 같은 부분에서도 많이 사용되고 있고, 연구와 산업 모두에서 수요가 있는 물질이다.
◇ 귀금속 사용 절감
- 가격이 비싼 금을 구리와 함께 사용함으로 금의 사용량을 줄일 수 있다. 또한 촉매를 재사용할 수 있는 수치가 나온다면 이 또한 경제적으로, 환경적인 측면에서 긍정적인 효과를 기대할 수 있다.
기술개발 일정 및 추진체계
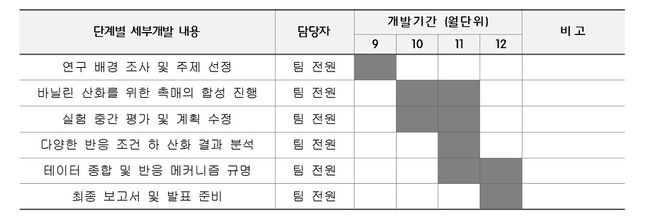
개발 일정
구성원 및 추진체계
◇ 바닐린 산화를 위한 촉매의 합성 진행 (팀 전원)
- Au를 활용한 여러 촉매를 만들고 아세토 바닐론에서 바닐린과 바닐산으로의 전환율이 높은 촉매를 확인한다.
◇ 다양한 반응 조건 하 산화 결과 분석 (팀 전원)
- 높은 전환율을 보인 촉매 및 다른 촉매들을 포함하여 여러 조건(압력, 온도 등)을 바꿔가며 최적의 조건을 찾는다.
◇ SEM, TEM과 같은 분석기기를 활용한 촉매의 구성 원소 분석 (팀 전원)
- 합성한 촉매를 사용 전후 입자 크기, 응집과 같이 촉매의 형태학을 분석한다.
◇ XPS, XRD와 같은 분석기기를 활용한 촉매의 구성 원소 분석 (팀 전원)
- 촉매의 Au 산화 상태, 결정상 크기 등을 분석하여 촉매 구성 상태를 확인한다.
◇ 데이터 종합 및 반응 메커니즘 규명 (팀 전원)
- 분석 결과를 선택도, 전환율, 시간에 따른 데이터를 통해 반응 경로를 정리한다.
설계
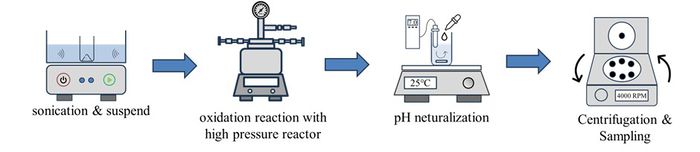
실험 방법
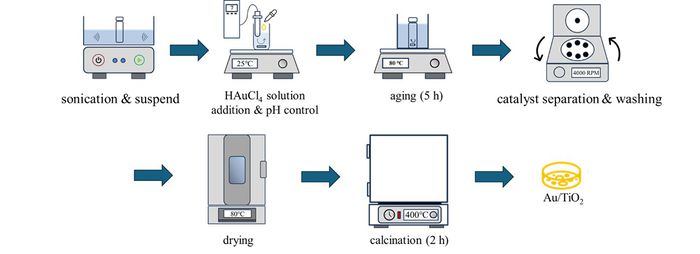
◇Au/TiO2 촉매 합성 방법
- 1. TiO2 1g을 소니케이션을 10분동안 진행해서 DI water에 분산시킨다. TiO2는 사용하기 전에 24시간동안 오븐에서 건조과정을 진행해 잔여수분을 제거해준다.
- 2. 소니케이션을 통해 얻은 TiO2 분산액에다 0.203M 우레아 용액 10mL와 5mg/mL 농도의 염화금산 삼수화물 용액을 dropwise 방식으로 순차적으로 첨가한다.
- 3. 위 용액을 80℃ , 5시간동안 교반을 진행해 금속 담지를 진행한다. 교반을 마친 뒤, 원심분리를 통해 촉매를 분리하고 DI water로 3~4회 세척을 진행한다.
- 4. 세척을 마친 뒤 얻어진 고형물을 진공 오븐에서 80℃에서 2시간동안 가열을 진행하고, 막자사발을 활용해 곱게 갈아주어 최종적으로 Au/TiO2 촉매를 얻을 수 있다.
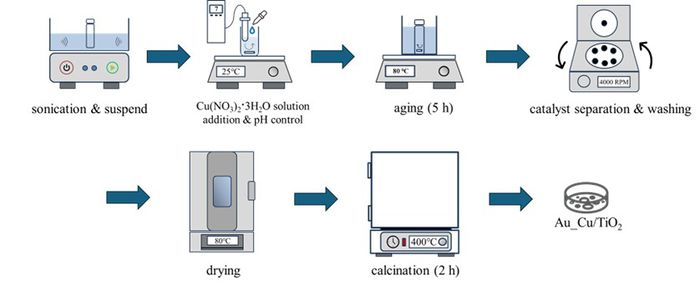
◇Au/TiO2 촉매 합성
금, 구리 이중 접합 촉매의 경우, 먼저 구리를 담지한 뒤 금을 순차적으로 담지시키는 2-STEP 방식을 활용했다. 정확한 합성 방법은 아래와 같다.
- 1. 1.5g의 TiO2를 소니케이션을 15분동안 진행시켜 DI water에 분산시킨다. 이전과 마찬가지로 TiO2를 사용하기전에 24시간 동안 오븐에서 건조하는 과정을 선행해주었다.
- 2. TiO2 분산액에 0.154M 우레아 용액 10mL와 질산구리 삼수화물 27.9mg이 용해돼있는 용액 10mL를 순차적으로 dropwise 방식으로 첨가한다.
- 3. 위 용액을 80℃ , 5시간동안 교반을 진행해 금속 담지를 진행한다. 교반을 마친 뒤, 원심분리를 통해 촉매를 분리하고 DI water로 3~4회 세척을 진행한다.
- 4. 세척을 마친 뒤 얻어진 고형물을 진공오븐에서 상온, 2시간동안 건조과정을 진행주고, 막자사발로 갈아주어 고체 형태의 Cu/TiO2를 얻어낸다.
- 5. 위 과정들을 통해 얻은 Cu/TiO2 1g을 DI water에 분산시킨 뒤, Cu/TiO2 합성과정과 마찬가지로 0.152M 우레아 용액 10mL와 5mg/mL 농도의 염화금산 삼수화물 용액 6mL를 dropwise 방식으로 순차적으로 첨가해준다.
- 6. 금 전구체 용액 및 우레아 용액 첨가를 마무리해준 뒤, 80℃에서 4시간 동안 교반을 진행한다.
- 7. 교반을 마친 뒤 원심분리를 통해 촉매의 분리 및 세척을 진행한다.
- 8. 최종적으로 진공오븐에서 80℃로 2시간동안 가열을 진행해주어 Au_Cu/TiO2 촉매 합성을 완료한다.
◇바닐린 산화 실험
바닐린 산화 실험은 한울엔지니어링의 HR-8200 고압반응기 모델을 활용해서 진행했다. 정확환 실험 순서는 아래와 같다.
- 1. 일정 농도의 수산화나트륨 용액이 들어있는 바이얼 병에 바닐린, 촉매를 첨가해준 뒤 10분간 소니케이션을 통해 촉매가 용액 내 고르게 분산되도록 한다.
- 2. 분산 과정을 마친 뒤 얻어진 용액을 고압반응기 내부에 투입해준 뒤 반응기 입구를 강하게 잠가준다.
- 3. 일정 압력만큼 고순도산소가스를 투입해주고, 설정한 반응 온도 및 반응 시간에서 바닐린의 산화 실험을 진행한다.
- 4. 반응이 끝난 뒤, 상온까지 냉각을 해주고 얻어진 반응 생성물을 묽힌 1M 염산 용액을 통해 pH 적정을 진행한다.
- 5. 최종적으로 원심분리를 통해 반응 생성물 내 촉매를 분리해주고, 순수한 액상의 분석 샘플을 얻고 분석 의뢰를 맡긴다.
결과 측정 방법
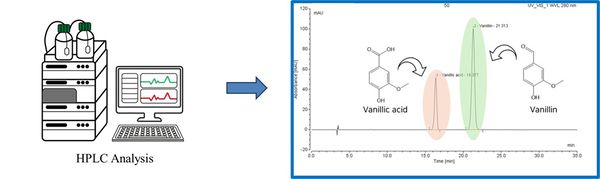
분석 방법은 고속 액체 크로마토그래피(High Performance Liquid Chromatography)를 활용했다. 역상컬럼법(C-18)을 활용했으며, 이동상은 DI water 77 %, methanol 23 %, formic cid 0.1 % 구성을 선택했다. 총 35분동안 측정을 진행했으며, UV/Vis 검출을 통해 280nm에서의 흡광도를 통해 정성 및 정량 분석을 진행했다.
실험 샘플의 분석을 의뢰하기 앞서, 먼저 바닐린과 바닐산 표준품의 샘플 분석을 맡겨서, 위 HPLC 측정 조건에서 바닐린, 바닐산이 몇 분대에서 검출되는지 확인했다.
측정 결과 바닐린은 21 분대, 바닐산은 16 분대에서 검출되었음을 알 수 있었다. 위 표준 샘플의 측정 결과를 바탕으로, 실험 샘플의 측정 결과를 진행했다.
결과 분석 방법
HPLC 측정을 통해 얻을 수 있는 바닐린 및 바닐산 농도를 바탕으로 바닐린의 전환율 및 바닐산의 선택성, 수율을 계산했다. 각 지표의 계산은 아래의 식을 통해 진행했다.
결과 분석
후처리 방식에 따른 바닐린 산화 차이
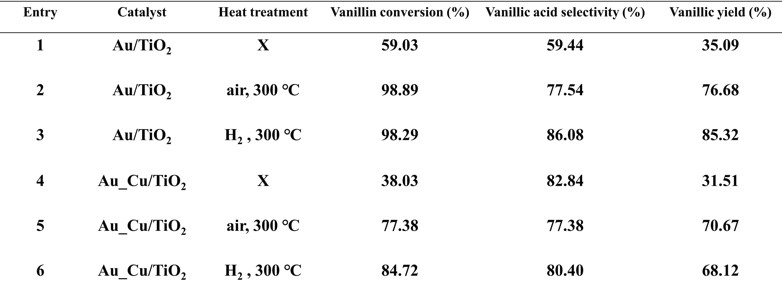
후처리 방식 차이에 따른 바닐린 산화 결과 차이에 대해 분석을 진행해보았다. 2가지의 촉매(Au/TiO2, Au_Cu/TiO2)와 3가지의 후처리 방식(후처리x, 공기 소성, 수소 소성)의 방식으로 총 6가지 샘플의 분석을 진행하였다. 이렇게 진행한 실험의 결과는 다음과 같다.
Au/TiO2를 수소 소성한 샘플의 결과가 85.32%로 가장 좋은 바닐산 수율이 나왔지만 Au만을 사용하는 경우 금의 가격으로 인해 경제적인 이융로 어느정도 비슷한 수율을 보이며 경제적으로 이점을 가진 Au_Cu/TiO2를 사용하기로 결정했다.
촉매량에 따른 바닐린의 산화 성능 분석
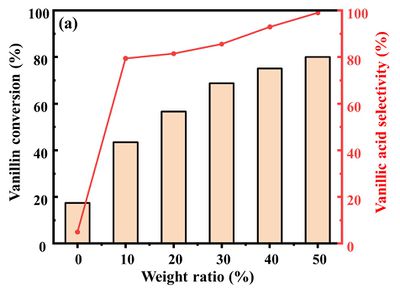
가장 먼저, 촉매량 증가에 따른 바닐린의 산화 성능을 분석해 보았다. 사용한 촉매의 경우, 구리와 금의 이론상 질량비가 1:1로 설정된, 전체 금속 로딩이 지지체 질량 기준 1 wt%인 금, 구리 이중 접합 촉매를 활용했다. 촉매량을 0 wt%부터 50 wt%까지 증가시키면서 바닐린 산화 실험을 진행했으며, 그 측정 결과는 아래와 같이 나왔다.
• 실험 결과를 보면, 촉매량이 증가할수록 바닐린의 전환율 및 바닐산 선택성이 꾸준히 증가하는 것을 확인할 수 있다.
• 특히, 촉매를 투입하지 않았을 때 얻어진 바닐산 선택성 4.971%에 비해서, 촉매를 10wt% 투입하는 순간 바닐산의 선택성이 급격히 증가(79.43%)하는 것을 확인할 수 있었다.
•위 측정 결과를 통해서, 실험 전에 예상했던 촉매량이 증가할수록 바닐린의 산화 효율이 증가할 것이라는 생각과 동일하게 측정되었음이 확인 가능했다.
반응 온도에 따른 바닐린의 산화 성능 분석
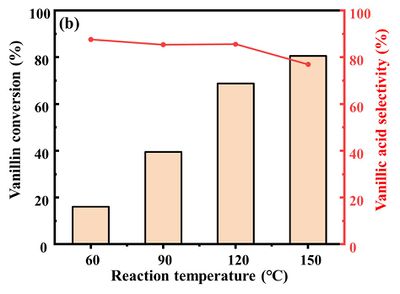
반응 온도에 따라 반응 온도 60℃부터 150℃까지 증가시키며 바닐린 산화 실험을 진행해보았으며, 측정 결과는 다음과 같다.
• 반응 온도가 증가할수록 바닐린의 전환율이 증가하는 것을 확인할 수 있다. 이는 반응 온도가 증가할수록 촉매 표면에 존재하는 금속 활성점과 접촉하는 바닐린 수가 증가하기 때문이라고 해석할 수 있었다.
• 또한 반응 온도가 증가함에 따라 촉매 표면의 금속 활성점과 접촉해서 만들어지는 활성 산소종의 수도 증가하는 점도 높은 바닐린 전환율의 근거로 볼 수 있다.
• 그러나 반응 온도가 120 ℃에서 150 ℃로 증가하면서 바닐산 선택성은 85.57 %에서 76.91 %로 감소하는 결과를 보였다. 이는 150 ℃ 이상의 고온에서는 바닐린의 1차 산화 반응으로 형성된 바닐산의 재흡착으로 인해 추가적인 산화 반응이 진행되어 얻어진 결과라고 보여진다.
• 즉, 바닐린의 전환율과 바닐산 선택성 모두 높은 값을 얻기 위해서는 너무 고온 환경에서 진행하는 것은 적합하지 않다는 것을 확인할 수 있었으며, 120 ℃ 주변의 온도 환경에서 산화 반응을 진행하는 것이 최적 반응 온도임을 알 수 있었다.
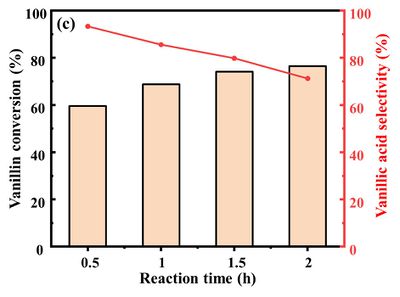
반응 시간에 따른 바닐린의 산화 성능 분석
반응 시간에 따른 바닐린의 산화 효율도 분석해 보았다. 반응 온도를 30분부터 2시간까지 증가시켜가며 바닐린 산화 실험을 진행했으며, 측정 결과는 다음 페이지의 그래프를 통해 확인할 수 있다.
• 반응 시간이 증가할수록, 바닐린의 전환율은 증가하지만 바닐산의 선택성은 감소하는 결과를 얻었다. • 이는 반응 시간이 증가할수록 바닐린에서 바닐산으로 전환되는 반응만 진행되는 것이 아니라, 바닐산에서 추가적인 부반응도 진행되어서 바닐산 선택성이 감소하는 것으로 해석할 수 있다. 이는 HPLC 검출 결과를 통해서도 간접적으로 확인이 가능하다.
• 위 검출 결과를 보면, 반응 시간이 2시간일 때, RT 5분 주변에서 확인되는 피크의 세기가 더 강해지는 것을 확인할 수 있다. 이는 바닐린, 바닐산 이외 물질의 검출 농도가 강해졌다는 정량적 의미로 해석이 가능하며, 이를 통해서 위에서 주장한 부반응 진행의 증가를 간접적으로 뒷받침할 수 있다.
수산화 나트륨 당량에 따른 바닐린의 산화 성능 분석
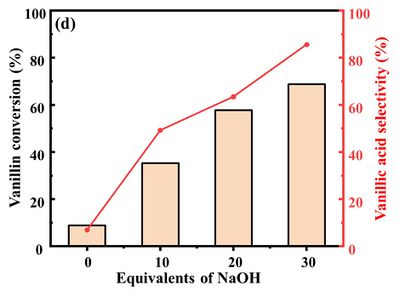
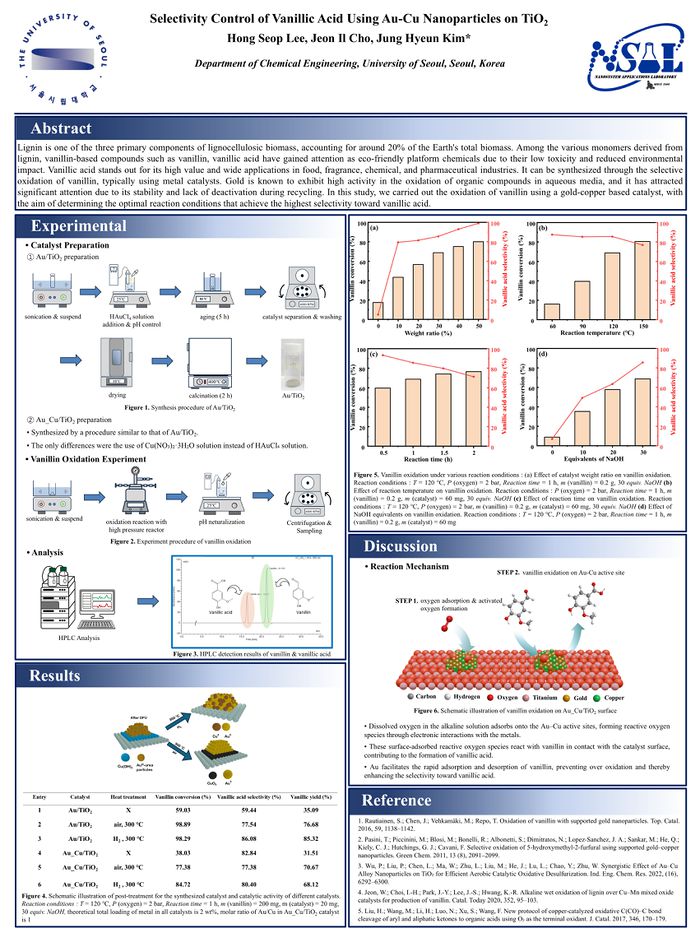
마지막으로, 이번 바닐린 산화 실험에서 염기로 활용하고 있는 수산화 나트륨의 투입 당량을 변화시켜가며 바닐린의 산화 성능을 분석해 보았다. 수산화 나트륨 당량을 0에서부터 최대 30까지 증가시켜가며 실험을 진행시켰으며, 그 측정 결과는 아래와 같다.
- 위 그래프를 보면 알 수 있듯이, 수산화 나트륨의 당량이 증가할수록, 바닐린의 전환율 및 바닐산 선택성이 동시에 증가하는 것을 알 수 있다.
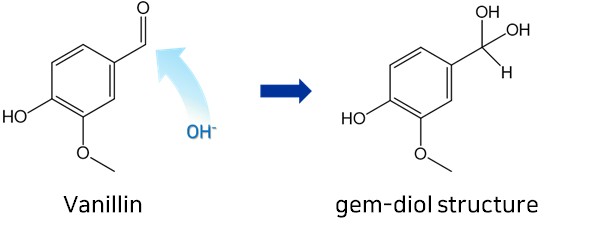
- 수산화 나트륨의 양이 증가하면서 알카리성 용액 내 OH 이온의 양이 증가하게 되고, 이 OH 이온은 바닐린을 공격해서 두 개의 수산기가 존재하는 gem-diol 형태로 변환시킨다.
- 그리고 이렇게 생성된 gem-diol 형태의 중간체는, 금속 활성점에 의해 형성된 활성 산소종과 반응해서 최종적으로 바닐산으로 산화되며, 형성된 바닐산이 촉매 활성점과 탈착되며 바닐산으로의 전환 반응이 마무리되는 것으로 생각할 수 있었다.
- 즉, 수산화 나트륨의 당량이 증가하면서 gem-diol 형태로 변환되는 바닐린의 수가 증가하게 되고, 이러한 중간체가 활성 산소종과 반응해서 더 높은 바닐산의 선택성으로 이어진다고 해석이 가능했다.
결론
◇ 촉매를 후처리 하는 방법은 Au/TiO2 를 수소 소성하는 것이 가장 좋았지만, Au를 너무 많이 사용하여 경제적이지 않아, 수율이 비슷하지만 경제적인 Au_Cu/TiO2 를 선택.
◇ 촉매의 양이 늘어남에 따라, 바닐산 선택도 높아짐.
◇ 반응 온도 높아짐에 따라, 바닐산 선택도 낮아짐.
◇ 반응 시간이 길어짐에 따라, 바닐산 선택도 낮아짐.
◇ Ph 조절을 위한 NaOH의 양이 많아짐에 따라, 바닐산 선택도 높아짐.
결과 및 평가
포스터
개발 과제 관련 향후 전망
◇ 이번 프로젝트종합설계를 통해서, 바닐린으로부터 바닐산을 얻어내는 반응에 대한 많은 정보를 얻을 수 있었다.
◇ 하지만, 금, 구리 이중 접합 촉매가 단일 금 촉매보다 높은 활성을 보일 것이라는 예상은 틀렸다. 따라서 이 부분에 대해서 좀 더 자세하게 알아볼 계획이다.
◇ 금과 구리의 비율에 문제가 있을 수도 있으며, 혹은 촉매 합성 방식이 잘못되었을 수 있다.
◇ 따라서 일차적으로는 구리와 금의 비율을 세세하게 조정해가며, 각 비율마다 바닐린의 산화 결과가 어떻게 측정되는지를 확인해 볼 계획이다.
◇ 만약, 각 비율마다 뚜렷한 결과가 확인되지 않는다면, 촉매의 합성 방식을 침전침적법이 아닌 다른 방식을 활용해서 촉매 합성을 진행해보고 그 결과를 확인해 볼 계획이다.
◇ 위와 같은 수정 과정을 거쳐서 최종적으로 금과 구리의 시너지 효과를 직접 확인하는 것이 이번 연구 주제의 최종 목표이다.
참고 문헌
◇ Rautiainen, S.; Chen, J.; Vehkamäki, M.; Repo, T. Oxidation of vanillin with supported gold nanoparticles. Top. Catal. 2016, 59, 1138–1142.
◇ Pasini, T.; Piccinini, M.; Blosi, M.; Bonelli, R.; Albonetti, S.; Dimitratos, N.; Lopez-Sanchez, J. A.; Sankar, M.; He, Q.; Kiely, C. J.; Hutchings, G. J.; Cavani, F. Selective oxidation of 5-hydroxymethyl-2-furfural using supported gold–copper nanoparticles. Green Chem. 2011, 13 (8), 2091–2099
◇ Wu, P.; Liu, P.; Chen, L.; Ma, W.; Zhu, L.; Liu, M.; He, J.; Lu, L.; Chao, Y.; Zhu, W. Synergistic Effect of Au–Cu Alloy Nanoparticles on TiO₂ for Efficient Aerobic Catalytic Oxidative Desulfurization. Ind. Eng. Chem. Res. 2022, (16), 6292–6300.
◇ Jeon, W.; Choi, I.-H.; Park, J.-Y.; Lee, J.-S.; Hwang, K.-R. Alkaline wet oxidation of lignin over Cu–Mn mixed oxide catalysts for production of vanillin. Catal. Today 2020, 352, 95–103.
◇ Liu, H.; Wang, M.; Li, H.; Luo, N.; Xu, S.; Wang, F. New protocol of copper-catalyzed oxidative C(CO)–C bond cleavage of aryl and aliphatic ketones to organic acids using O₂ as the terminal oxidant. J. Catal. 2017, 346, 170–179.
◇ Timofeev, K. L., & Vodyankina, O. V. (2021). Selective oxidation of bio-based platform molecules and their conversion products over metal nanoparticle catalysts: A review. Reaction Chemistry & Engineering, 6(3), 418–442.
◇ Davis, S. E., Houk, L. R., Tamargo, E. C., Datye, A. K., & Davis, R. J. (2011). Oxidation of 5-hydroxymethylfurfural over supported Pt, Pd and Au catalysts. Catalysis Today, 160(1), 55–60.
◇ Sandoval, A., Louis, C., & Zanella, R. (2013). Improved activity and stability in CO oxidation of bimetallic Au–Cu/TiO₂ catalysts prepared by deposition–precipitation with urea. Applied Catalysis B: Environmental, 140–141, 363–377.