삼종접합
프로젝트 개요
기술개발 과제
국문 : NiZnS 광촉매의 수소생산에 구리 도핑이 미치는 영향
영문 : Effect of Copper Doping on the Hydrogen Production of NiZnS Photocatalyst
과제 팀명
삼종접합
지도교수
김정현 교수님
개발기간
2022년 9월 ~ 2022년 12월 (총 4개월)
구성원 소개
서울시립대학교 화학공학과 2019340014 김주현(팀장)
서울시립대학교 화학공학과 2019340004 권지원
서울시립대학교 화학공학과 2019340009 김수경
서울시립대학교 화학공학과 2016340014 박종현
서론
개발 과제의 개요
개발 과제 요약
◇ 수소 에너지의 수요증가에 따른 기술 연구 개발의 필요성 증가 ◇ 연구를 위한 광촉매 원료와 도핑 재료 선정 ◇ NiZnS 광촉매 합성 및 구리 도핑 ◇ 광촉매의 수소 생산량 측정 및 비교 ◇ 다양한 분석을 통한 원인 조사 ◇ 종합적인 결론 도출
개발 과제의 배경
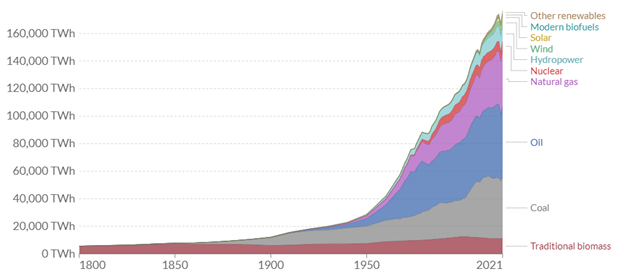
18세기 영국에서 증기기관이 발명되며 세계적으로 에너지에 대한 수요가 폭발적으로 증가하였다. 증기기관이 발명되어 글로벌 운송망이 형성되었고, 각 기업은 앞다퉈 공장을 설립하기 시작하였다. 물자를 운송하고, 공장의 기계를 돌리기 위해서는 많은 에너지가 필요했고, 이 때 주목받은 것이 바로 화석연료였다. 화석연료는 산업혁명 이전부터 사용되었지만, 산업혁명을 기점으로 사용량이 급격히 증가하였다. 아래의 그림 1에서 볼 수 있듯이, 산업혁명 이전에는 500 TWh 부근에서 머물던 화석 연료 사용량이 현재는 160000 TWh를 돌파하였다. 대략 27배 증가한 것이다. 결론적으로 증기기관의 발달은 세계적인 에너지 수요를 끌어올렸고, 이에 따라 화석 연료의 사용량이 증가하였다.
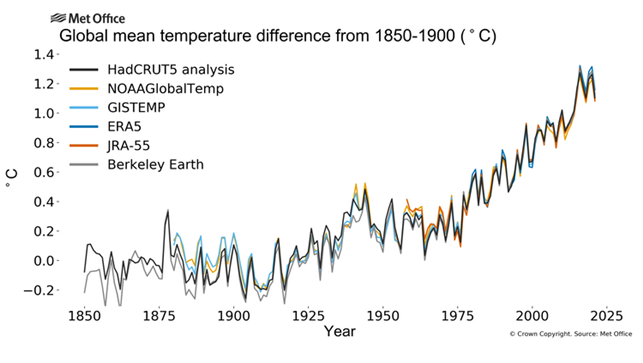
화석연료는 사용이 편리하며 가공이 용이하다는 많은 장점을 갖고 있지만, 하나의 치명적인 단점을 갖고 있어 현재 화석연료 사용에 대한 회의론이 제기되고 있다. 그 단점은 바로 지구온난화이다. 지구 온난화란 특정 요인에 의하여 지구의 복사강제력이 커져 전지구의 평균 기온이 상승하는 현상이다. 화석연료를 사용하기 위해서는 이것을 연소시켜야 하는데, 이때 이산화탄소와 같은 온실가스가 대기 중으로 방출된다. 대기중으로 방출된 온실가스는 지표면에서 우주로 방출되는 적외선 복사열을 흡수 혹은 다시 지표면으로 반사시켜 지구 표면의 온도를 상승시킨다. 이로 인하여 실제로 산업혁명 이후로 지표면의 온도는 1.2도 상승하였다.
인류가 처해있는 지구온난화로부터 벗어날 수 있는 해결책으로 제시되는 것이 바로 대체 에너지이다. 대체 에너지란 석유, 석탄, 천연가스 등 기존의 화석연료를 대체할 수 있는 에너지이다. 대체 에너지는 대체 에너지는 신에너지와 대체에너지로 나뉜다. 신에너지는 화석 연료를 변환시키거나 수소, 산소 등의 화학 반응을 통하여 생산된 에너지이다. 신에너지에는 수소, 연료 전지 등이 속한다. 재생 에너지는 재생 가능한 에너지를 변환시켜 이용하는 에너지로 태양, 풍력, 지력, 조력 등이 속한다. 대한민국에서는 신에너지와 재생에너지를 통틀어 신재생에너지라고도 부른다. 신재생 에너지는 고갈 우려가 없고, 오염물질과 이산화탄소 배출량이 적어 환경친화적이다. 따라서, 세계 각국들이 화석연료 사용을 줄이고, 신재생 에너지의 비중을 높이는 것을 목표로 하고 있다. 2021년 5월엔 유럽연합의 집행위원회가 2050년 탄소중립을 법으로 명시한 기후기본법을 제정하였고, 2022년 8월엔 미국의 바이든 대통령이 2030년까지 탄소배출을 2005년 대비 40%로 감축한다는 내용을 담은 기후변화 대응법을 발효했다.
앞서 말했듯이 신재생 에너지에는 다양한 종류의 에너지가 있다. 하지만, 그 중에서 요즘 특히 각광받는 것이 있다. 바로 수소 에너지이다. 수소에너지는 수소 형태로 에너지를 저장하고 사용하는 에너지원으로 화석 연료를 대체할 청정에너지원으로 꼽힌다. 수소에너지의 원료가 되는 물은 지구상에 풍부하게 존재하여 고갈될 우려가 없고, 수소를 연소시켜도 물이 배출되므로 지구온난화의 우려도 화석연료에 비하면 현저히 낮다. 또한, 에너지 밀도가 높아 수소 1kg으로 3,5000kcal의 에너지를 얻을 수 있다. 다른 신재생 에너지는 날씨 혹은 지형의 영향을 많이 받는 반면, 수소 에너지는 언제 어디서나 사용할 수 있다는 이점 또한 존재한다. 이런 다양한 장점으로 수소 에너지의 사용 비중은 날로 커져가고 있다.
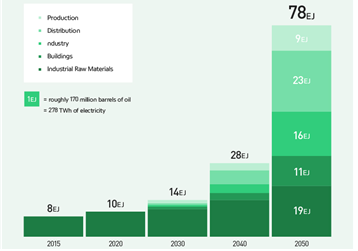
그림 3에서와 같이 2015년 수소 에너지 사용량은 8 EJ이지만, 2050년에는 78 EJ로 증가할 것이라고 예측된다.
광촉매란 빛을 에너지원으로 이용하여 새로운 물질을 합성 혹은 분해시키는 촉매로, 태양에너지를 화학에너지로 변화시켜준다. 이 광촉매는 유기물 분해 혹은 물 분해 측면에서 연구가 많이 되고 있는데, 그 중 물을 분해하여 수소에너지를 친환경적으로 생산하는 물 분해 광촉매가 주목받고 있다. 물 분해 광촉매는 태양광을 사용하여 물이 산소와 수소로 분해되게 도와주는 역할을 한다. 추가로, 지속가능한 에너지인 태양과, 상대적으로 제한 없이 사용할 수 있는 물을 사용한다는 점에서도 친환경적이다. 요즘같이 수소 에너지의 중요성과 수요가 높아지는 만큼, 효율적인 수소 생산에 대한 연구 개발에 더 많은 투자가 이뤄지고 있고, 특히 이 광촉매를 활용한 수소 생산에 귀추가 모이고 있다. 본 연구에서도 태양광을 이용하여 수소를 생산할 때, 수소 생산의 효율을 올려주기 위한 광촉매에 대해 다룰 것이다. 이를 통해 수소를 더욱 효율적으로 생산할 수 있는 촉매를 개발하는 것이 목표이다.
개발 과제의 목표 및 내용
본 개발 과제가 지향하는 최종적인 목표는 효율적인 수소 생산이 가능한 촉매를 합성하는 것이다. 광촉매 활성에 영향을 미치는 인자는 온도, 내부식성, 결정성 등 여러 가지가 있지만, 가장 중요한 요인은 band gap energy이다. band gap은 수소 생산 반응과 밀접한 관계가 있다. 광촉매에 태양광이 들어오면 빛에너지 덕분에 valence band(VB)에 있던 전자가 conduction band(CB)로 올라가게 된다. 이때, VB에 생긴 정공에 의해 물이 산화되며 산소 기체와 수소 이온이 생산되고, CB로 올라간 전자가 수소이온을 환원시키면서 수소가 생산된다. 이때, 만약 band gap이 넓다면 그만큼 많은 에너지가 필요하게 되고, 가시광선에서의 활용성이 떨어진다. 그렇다고 띠 간격을 과하게 좁혀서 물분해반응 에너지인 1.23 eV보다 적어진다면 물분해반응이 일어나지 않는다. 또한, band gap이 1.23 eV에 가까워지면, excited 되어 CB로 올라간 전자가 VB의 정공과 재결합하는 현상이 발생하여 광촉매의 성능이 떨어질 수도 있다. 재결합이 일어나지 않게 하면서, 띠 간격을 줄이는 것이 광촉매의 주요 연구과제이다.
광촉매의 수소 생산성능을 향상시키기 위해서 연구자들은 heterostructure, heterojunction, doping, oxidaton 등 다양한 방법을 접목시키고 있다. 그 중 heterostructure, heterojunction 방법은 여러 물질을 접합시킴으로써 band gap은 좁히면서 band gap 감소의 부작용인 재결합도 줄이는 방법으로, 널리 사용된다. 본 연구는 그 중 니켈, 아연, 황 세 가지 물질을 사용하여 NiZnS라는 heterostructure를 형성하여 새로운 band gap을 가지는 물질을 합성하고자 한다. 합성 과정에서 S(황)의 비율을 변화시켜가며 수소 생산량과 황의 관계에 대해 탐구할 것이다. 이를 통해 수소 생산을 위한 최적의 비율을 찾을 것이다. 더 나아가, doping하여 band gap을 줄어들게 함으로써 더 많은 수소 생산을 얻고자한다.
Doping은 광촉매 분야 뿐만 아니라 다양하게 사용되는 방식으로, 광촉매에서는 band gap을 줄여주는 역할을 한다. 금속물질을 도핑하게 될 경우 conduction band의 에너지를 낮춰주며, 비금속 물질을 도핑할 경우 valence band의 에너지를 높여준다. 즉, 두 가지 경우 모두 band gap을 줄이는데 영향을 미친다. 이는 가시광선 영역의 흡수를 향상시켜주며 결과적으로 수소 생산량을 높여주게 되는 것이다. 어떠한 doping 재료를 사용할 것인지에 대해서는 NiZnS의 band gap을 먼저 측정한 후 결정하고자 한다.
앞으로 수소 사용량이 늘어나게 되면, 촉매의 합성 과정이 얼마나 단순화되어있는지에 대한 것도 중요하게 평가될 것이다. 본 연구에서 진행하는 NiZnS heterostructure의 생성 방법은 다른 Heterojunction 물질 생성에 비해 단순하다. Heterostructure는 일정한 비율의 precursor를 넣고 열을 가해주면 합성이 되지만, Heterojunction은 두 물질을 따로 합성하고 다시 열을 가해주거나, 한 물질을 합성하고 다른 물질을 그 위에 coating 되도록 해야 한다. 그렇기 때문에 Heterostructure 방법을 사용하면 보다 쉬운 방법으로 합성하여 많은 수소 생산량을 얻을 수 있는 것이다.
수소 생산 성능은 광촉매를 물에 균일하게 분포시킨 후 중위도의 태양빛과 동일한 AM 1.5 G의 빛을 사용하여 물분해 반응을 시켰을 때, 생성되는 수소의 양을 gas chromatography(GC)를 사용하여 측정한다. GC를 찍으면 기체양이 Area로 표시되는데, 이 area를 reference를 통해 mol %로 환산한다. 환산된 mol %와 이상기체 방정식 () 이용하여 수소량(µmol/g/h)을 구할 수 있다. 결과적으로 수소량을 확인하여 광촉매의 효율을 평가할 수 있는 것이다.
수소 생산량뿐만 아니라, 동대한 reproducibility도 측정한다. 광촉매는 일회성이 아니기 때문에 계속 좋은 성능을 유지하는 것도 중요하게 평가된다. 특정 시간 간격으로 새로 질소 purging을 해주면서 수소 생산량을 확인한다. 재사용에 의한 수소생산량 감소가 적을수록 좋은 광촉매이다.
관련 기술의 현황
관련 기술의 현황 및 분석(State of art)
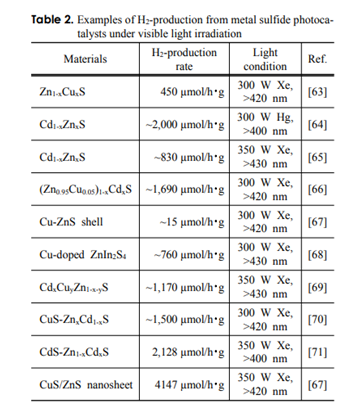
김정현(2013) 연구에서는 태양광을 이용한 물분해 수소생산용 광촉매재료들에 대하여 알아보고, 현재까지 보고된 다양한 광촉매재료의 특성들을 검토하였다. 광촉매 재료로는 이산화티타늄, 텅스턴 계열, 구리 계열, 흑연탄소질화물, 금속황화물 등이 사용된다. 이산화티타늄은 강한 산화활성(oxidation activity)과 수친화력(hydrophilicity)의 특징을 가진다. 하지만대적으로 큰 띠간격 에너지로 인하여 자외선 이상의 가시광선(태양광의 약 45%)을 활용함에 어려움이 있다. 가 가지고 있는 큰 띠간격을 줄이고 가시광선의 흡수를 높이기 위해 금속물질이나 비금속물질의 도핑이 수행되는데, 이를 통해 원자가띠 에너지(hν3)가 높아지게 된다. 수소를 생산하기에 적절한 띠간격을 만족시키기 위해 두 종류의 재료를 결합하여 각각으로부터 수소와 산소를 생산하는 역할을 담당하게 할 수 있다. 그것을 Z-scheme 촉매라고 한다. 이러한 개념을 바탕으로 텅스텐산화물()은 물을 산화시켜 산소를 생산하는데 매우 유리한 전위구조를 가지고 있으며, 다양한 화학반응 용액조건에서 광 및 화학적 안정성을 보여준다. 구리 화합물인 황동(chalcopyrite) 계열(, , )은 좁은 띠간격과 화합물에 따라 비교적 정교한 에너지준위를 가진 물질로 태양광의 특정 파장영역을 흡수하기에 매우 적합한 물질이다. 화합물의 조성을 비교적 쉽게 변화시켜 밴드구조를 1.1~2.5 eV 범위에서 조절 가능하며 우수한 전자이송 특성을 가지고 있다. 또한 전도띠의 전위가수소를 생산하기에 용이한 음전위에 위치하고 있다. 하지만, 원자가띠의 위치에 있어서 물분해로부터 산소를 산하기에는 적합하지 않으며, 따라서 황동광계열 촉매로부터 물분해 수소생산은 혼합구조 광촉매의 사용이 필요하다. 흑연탄소질화물()은 그래파이트와 유사한 고분자형 반도체 소재로서 우수한 화학적, 광화학적 안정성을 가지고 있는 것으로 알려져 있다. 띠간격은 약 2.7 eV이며 이는 가시 광선 파장영역인 400~450 nm의 파장을 흡수할 수 있다. 금속황화물 광촉매는 촉매기능이나 띠간격 측면을 고려하여 최근에 연구가 활발히 진행되고 있다. 특히, 아연황화물(ZnS)은 광여기에 의하여 전자-정공 쌍을 빨리 형성하고 여기된 전자가 높은 음전위를 가지고 있어 물분해 수소생산 반응에서 매우 높은 활성을 보이는 특징이 있는 것으로 잘 알려진 광촉매 물질이다. ZnS의 띠간격은 3.66eV로 비교적 큰 편이며 가시광에 의한 광여기를 용이하게 하기 위하여, 구리(Cu)와 카드뮴(Cd) 등의 금속성 물질을 동시에 도입하는 등 다양한 실험이 이뤄지고 있다. 태양광을 활용한 물분해 수소생산용 광촉매재료
Chi-Jung Chang(2019) 논문에서는 광촉매로서 Ni이 도핑된 ZnS 나노 물질을 사용하였다. 주사전자현미경(SEM), X선회절(XRD), 확산반사분광(DRS), 광발광(PL), 광전류 반응 및 접촉에 의해 Ni 도핑 함량이 광촉매 수소 생성 활성, 형태론, 광특성, 결정특성, 표면 함침성, 광전류 등에 미치는 영향을 연구하였다. 분석에 의하면, NiO/Ni foam에 처리된 Ni-doped ZnS이 표면을 소수성에서 초친수성으로 변화시켰다. 이를 통해 ZnS, NiO, NiO foam 사이의 전자의 전달과 함께 ZnS와 NiO의 band gap 설명하는 메커니즘을 제안했다. Ni이 도핑된 ZnS/NiO/Ni foamd의 광촉매인 NZ5는 band 구조와 Ni foam의 높은 전도성으로 인해 훨씬 더 높은 광촉매 활성을 보였다. 광촉매의 다공성 텍스처 및 초친수성 성질은 광트래핑(light traping), 반응물 분자의 효과적인 질량 전달(mass transfer)에 유리하며, 접촉 면적이 넓다. 따라서 Ni 도핑은 band 갭을 감소시키는 역할을 하게 된다. 가장 높은 광촉매 생성 활성은 2500 µmol/g/h에 달했다. 3 cycle 동안 작동한 후, 3번째 cycle의 활성도는 1째 cycle에서 얻은 활성의 85%였다. Efficient photocatalytic hydrogen production by doped ZnS grown on Ni foam as porous immobilized photocatalysts
chang(2015)등이 발표한 연구에 의하면, graphene 표면 위에 광촉매를 decoration 시키면 광촉매의 hydrogen production performance이 향상된다. chang은 위와 같은 사실을 입증하기 위해 XPS, XRD, FESEM, TEM, DRS등 다양한 분석장비를 활용하여 연구를 진행하였다. chang은 graphene 표면 위에 ZnS를 도포하고 각각 1시간, 2시간, 3시간 동안 ZnS nanoparticle이 성장하도록 기다렸다. 이후에 해당 촉매를 이용하여 water splitting 하여 hydrogen production 하였다. 1시간, 2시간, 3시간 동안 nanoparticle을 성장시킨 촉매의 수소 생산량은 각각 4545, 5700, 1890μmol/h/g이었다. 위와 같은 결과는 촉매의 nanoparticle 성장 시간에 따른 표면적의 변화와 연관되어 있다. BET 분석기기로 분석해본 1시간, 2시간, 3시간의 성장 시간을 가진 촉매의 표면적은 각각 78.70, 97.63, 31.39이다. 그래핀 위에서 ZnS nanoparticle이 성장하면 촉매의 표면적이 증가한다. 하지만, 3시간 동안 nanoparticle이 성장한 촉매는 ZnS에 의한 두꺼운 필름막을 갖게 된다. 이로 인하여 3시간 동안 nanoparticle을 성장시킨 촉매의 표면적이 가장 작아졌다. 따라서, 촉매의 표면적이 가장 작기 떄문에 수소의 발생량도 가장 적어졌다. Ni-doped ZnS decorated graphene composites with enhanced photocatalytic hydrogen-production performance
You(2015)등이 발표한 연구에서는 semiconductor-based photocatalyst를 이용한 물 분해 수소 생성 반응에서 사용되는 solid metallic Ni, Ni based compound와 같은 다양한 Ni- based cocatalyst에 대해 다뤘다. 해당 연구에 의하면 solid inorganic Ni-based cocatalyst에서 수소 생산의 Quantum efficiency는 53%로 447nm에서 가장 최적이었다. 또한, Ni-based molecular cocatalyst에서 최대 600,000톤의 수소 생산이 가능하다는 것을 보여주었다. Nickel-based cocatalysts for photocatalytic hydrogen production
특허조사
가시광 감응 광촉매 구조체, 그 제조방법 및 그를 이용한 물 분해 수소생산방법
- 출원 번호 : 10-2021-0020418
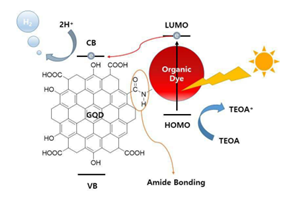
- 요약 : 본 발명은 가시광 감응 광촉매 구조체, 그 제조방법 및 그를 이용한 물 분해 수소생산방법에 관한 것으로서, 그래핀 양자점(Graphene Quantum Dot) 및 아민계 염료 화합물을 포함하고, 상기 그래핀 양자점과 아민계 염료 화합물이 공유결합에 의해 결합된 가시광 감응 광촉매 구조체, 그 제조방법 및 그를 이용한 물 분해 수소생산방법을 제공한다.
- 그림 2는 본 발명의 실시예에 따른 가시광 감응 광촉매 구조체 및 광원에 의한 전자 여기 메커니즘을 개략적으로 나타낸 것이다. 그림 2에서, 가시광 감응 광촉매 구조체는 그래핀 양자점(Graphene Quantum Dot, GQD) 및 아민계 유기 염료 화합물을 포함하고, 그래핀 양자점과 아민계 유기 염료 화합물은 공유결합에 의해 결합된다. 그래핀 양자점은 표면에 히드록실기(-OH) 및 카르복실기(-COOH)와 같은 친수성 작용기를 포함할 수 있다. 그래핀 양자점은 표면에 존재하는 친수성 작용기로 인해 우수한 수용성을 나타내며, 기존의 탄소나노소재가 가지는 용매 분산 안정성에 대한 문제를 해결할 수 있다. 그래핀 양자점(graphene quantum dot, GQD)은 육각형 모양으로 결합되는 탄소 원자들의 이차원적 확장으로 구성된 단층 소재인 그래핀의 층상 구조가 반복되어 쌓여있는 구조체로서, 직경이 수 nm 정도의 판상으로 판의 내부는 단일 그래핀 격자로 이루어져 있다. 그래핀 양자점은 반도체적 성질을 가지며, 이로 인해 여기된 전자를 촉매 반응에 사용할 수 있는 광촉매 특성을 가진다.
- 상기한 바와 같이 이루어진 본 발명의 실시예에 따른 가시광 감응 광촉매 구조체는 광 촉매 반응의 반응속도와 촉매 전환률의 특성을 동시에 향상시킬 수 있다. 또한, 수용액 상에서 높은 용해도를 가지게 되어 수용액 상 광촉매 재료로 적용하기에 적합하다. 또한, 전자의 전이 효율을 높여 물분해 수소 생산 효율을 높일 수 있다. 또한, 조촉매의 적용 없이 낮은 단가로 높은 촉매 활성을 기대할 수 있다. 물론 이러한 효과에 의해 본 발명의 범위가 한정되는 것은 아니다.
가시광 물분해 수소생성용 광촉매 및 이를 이용한 물분해 수소생성방법
- 출원 번호 : 10-1541746
- 요약 : 본 발명은 가시광 물분해 수소생성용 광촉매 및 이를 이용한 가시광 물분해 수소생성방법에 관한 것으로, 보다 구체적으로는 플라티늄이 로딩된 및 상기 표면에 형성된 나피온 층을 포함하되, 상기 나피온 층에는가 함침되어 있는 가시광 물분해 수소생성용 /Nf/Pt- 광촉매 및 이를 이용한 가시광 물분해 수소생성방법에 관한 것이다. 본 발명에 따르면, 염료를 따로 용액에 녹여 사용하지 않으면서도 의 가시광에서의 활성을 개선하여 가시광을 이용하여 효율적으로 물분해를 통한 수소가스의 생산이 가능하다.
- 본 발명에 따른 가시광 수소생성용 광촉매는 의 가시광에서의 활성을 개선하여 가시광을 이용하여 효율적으로 물분해를 통한 수소가스의 생산이 가능하고, 간단한 공정을 통하여 염료와 촉매를 일체화시킴으로써 염료를 따로 용액에 녹이지 않고도 자체적으로 사용이 가능하며, 전 pH 영역에서 수소생성이 가능하여 수소생성효율을 더욱 향상시킬 수 있다. https://patents.google.com/patent/KR101541746B1/ko
효율적인 수소 방출을 위한 테더링된 전이 금속 촉진된 광촉매 시스템
-출원번호 : 10-2016-7008797
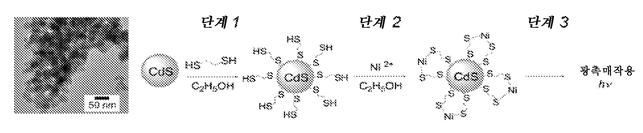
-요약 : 본 발명은 적어도 부분적으로는 유기 리간드를 사용하여 금속 (예를 들어, 후 전이 금속(late transition metal), 예컨대 니켈의 금속 이온)을 반도체 (광촉매) 표면에 테더링(tethering) (침착)시킴으로써 광촉매 (반도체 광촉매)의 효율을 개선시키는 방법에 관한 것이다. 보다 구체적으로, 1,2-에탄디티올 (EDT)이 전이 금속 착물 (예를 들어, 니켈 (Ni2+ 이온))을 반도체 표면에 부착시키기 위한 우수한 분자 연결기(linker) (예를 들어, 유기 리간드)로서 기능하며, 반도체 표면은 황화카드뮴 표면의 형태일 수 있다. 광촉매는 H2S로부터 수소를 생성하는 데 특히 유용하다.
-본 발명은 적어도 부분적으로는 본원에 기술된 바와 같은 유기 리간드를 사용하여 금속 (예를 들어, 후 전이 금속(late transition metal), 예컨대 니켈의 금속 이온)을 반도체 (광촉매) 표면에 테더링 (침착)함으로써 광촉매 (반도체 광촉매)의 효율을 개선시키는 방법에 관한 것이다. 하나 이상의 변형에서, 1,2-에탄디티올 (EDT)이금속 착물 (예를 들어, 니켈 (Ni2+ 이온))을 반도체 표면에 부착시키기 위한 우수한 분자 연결기 (예를 들어, 유기 리간드)로서 기능하며, 반도체 표면은 황화카드뮴 (CdS) 표면의 형태일 수 있다.[0016] 본 발명의 광촉매는 H2S로부터의 수소 생성, 물 분해, CO2 환원 등을 비롯한, 다수의 상이한 응용에서 사용될 수있다.
환원그래핀옥사이드-이산화티타늄 광촉매 복합체의 제조방법 및 그 방법을 이용한 태양연료로서의 과산화수소의 제조방법
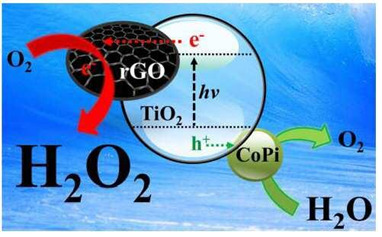
-요약 : 본 발명은 이산화티타늄(TiO2) 및 환원그래핀옥사이드(reduced Graphene Oxide, rGO)를 포함하는 광촉매 복합체이거나, 상기 광촉매 복합체에 포스페이트(phosphate) 또는 코발트포스페이트(Cobalt phosphate, CoPi);를 추가로 포함하는 광촉매 복합체 및 그를 이용한 태양연료로서의 과산화수소의 제조방법을 제공하며, 본 발명에 따른 광촉매 복합체는 귀금속을 대체한 환원그래핀옥사이드가 담지된 이산화티타늄에 의해 과산화수소의 생산 효율이 우수하고, 인산기가 이산화티타늄 표면에 보호막물질로서 생성된 과산화수소의 분해를 저해하여 과산화수소의 생산효율을 높이고, 코발트포스페이트에 의해 in-situ 형성으로 유기 전자 공여체 없이 과산화수소를 생산하므로, 공정상 비용이 낮은 경제적인 과산화수소의 제조방법을 제공할 수 있다.
- 본 발명의 광촉매 복합체는 귀금속을 대신에 환원그래핀옥사이드가 담지된 이산화티타늄이 과산화수소의 생산효율을 높이고, 인산기가 이산화티타늄 표면에서 과산화수소의 분해를 방지하여 과산화수소의 생산효율을 높이고, 코발트포스페이트는 유기 전자 공여체 없이 과산화수소를 생산하는 효과가 있다. 따라서, 본 발명의 광촉매복합체는 공정 비용이 낮은 경제적인 과산화수소의 제조방법을 제공할 수 있다.
특허전략
여러 가지 방법으로 수소를 생산하는 특허가 등록되어 있었다. 기존의 수소생산은 주로 열에너지와 유기물, 태양에너지를 사용하여 이루어지고 있는 것으로 보인다. 이 중 가시광을 이용해 물분해로 수소를 생산하는 방법은 극히 일부이다. 따라서, 촉매 제조방법과 촉매의 수소생산 능력을 입증한다면 충분히 특허를 취득할 수 있을 것으로 보인다.
여러 Heterojunction을 사용한 광촉매가 특허 등록되어 있지만, 황화아연의 경우 특허가 존재하지 않았고, Heterojuction에 도핑된 광촉매의 경우도 특허가 존재하지 않았다. 따라서 새로운 물질을 광촉매에 도입하였다는 신규성을 확보할 수 있을 것으로 보인다. 따라서 이후 실험을 통해 기존 광촉매 대비 높은 효과를 보인다는 점을 입증할 수 있는 데이터를 확보한다면 특허 등록에 유리할 것으로 보인다.
따라서, 촉매의 독창성과 촉매 제조 과정의 독창성을 내세워 신규성을 확보하고, 촉매의 수소생산효율을 내세워 진보성을 확보할 수 있을 것으로 보인다.
대부분 특허가 촉매 제조방법과 수소 생산량까지 자세하게 기술되기 때문에, 상세한 제조 과정과 수소 생산 방법이 명확하게 정리되어야 한다. 따라서 수소생산량 이외에도 촉매생산 효율을 높일 필요가 있다. 또한, 공정에 적용할 수 있는 방안까지 고안한다면 더 고도한 기술이 될 수 있을 것이다.
개발과제의 기대효과
기술적 기대효과
기존에 사용하지 않던 조합의 비금속 도핑을 통하여 수소 생산 반응에 관련된 band gap을 조절하고, 이를 통해 가시광선 영역의 빛 흡수를 증가시켜 수소생산능력을 개선한 광촉매를 개발한다. 전자-홀의 이동을 향상시키고, 재결합 확률을 낮출 것이다. 또한 각종 분석장비를 이용해 매개변수와 수소생산능력의 상관관계 밝힐 것이다. 연구의 매커니즘을 밝힐 것이다.
또한, 광촉매는 오염물질의 분해와 자정작용이 있도록 하는 등의 기능이 있는 기술로서 유해한 화학물질에 대한 강력한 분해력으로 환경분야 뿐 아니라 많은 분야에 널리 사용되고 있다. 따라서, 항균, 살균, 방취작용으로 병원, 화장실 등 세균이 있는 곳과 유기물의 분해작용으로 세정작용이 필요한 터널 전등, 터널 벽, 욕실, 주방용품 및 빗물에 의한 자정이 필요한 유리창, 태양전지 상판유리, 헤드라이트 등에 사용될 수 있다. 따라서, 해당 분야의 개발을 통해 다른 분야에도 적용할 수 있을 것으로 기대된다.
경제적, 사회적 기대 및 파급효과
수소는 우주 질량의 75%를 차지할 정도로 가장 흔한 원소이다. 지구 표면의 70%를 덮고 있는 물에도 수소가 들어 있다. 액체나 고압 기체로 저장이 가능하고, 운송이 쉽다는 이점도 있다. 화석연료와 달리 고갈될 우려나 지역 편중이 없고 자연환경 조건에 따라 전기 생산량이 달라지는 재생에너지의 단점을 보완해줄 수 있는 것도 수소의 장점이다. 따라서 광촉매 개발로 인해 수소생산량을 증가되면 수소경제를 활성화할 수 있다.
전세계적으로 현재 화석연료 중심의 수소 생산 방식에서 CO2를 적게 발생시키는 친환경적 수소 생산 방식으로 전환함에 따라, 탈화석연료에 기여하고 온실가스를 줄이고 관련 산업과 일자리 창출은 물론 첨단 기술 발전으로 세계 경제를 선도할 수 있다.
우리나라는 거의 모든 화석연료를 수입하여, 산업과 경제가 화석연료 가격 변동에 영향을 크게 받는다. 따라서 수소에너지 생산량을 높여, 수입의존도를 낮출 수 있으며, 역수출의 기회를 얻을 수 있다.
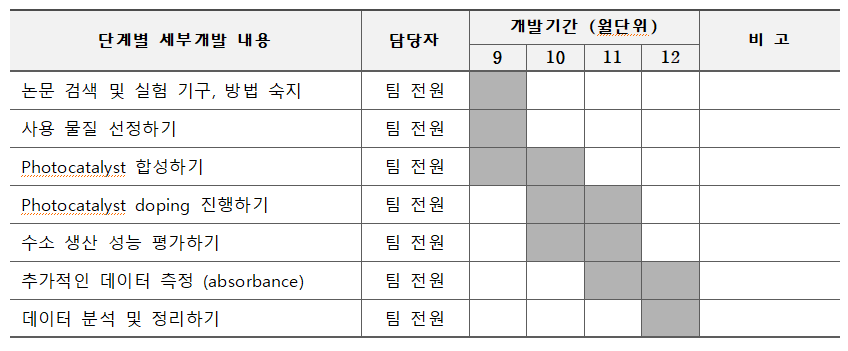
기술개발 일정 및 추진체계
개발 일정
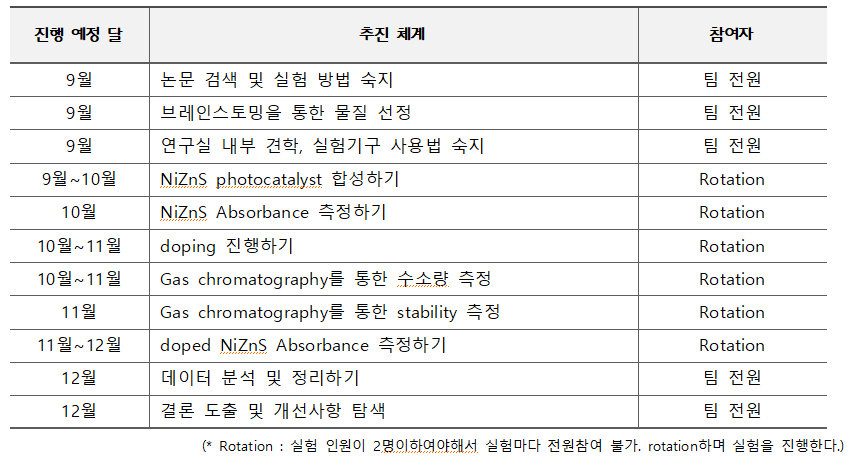
구성원 및 추진체계
설계 및 결과
목표 달성을 위한 실험 방법
NiZnS 광촉매 합성 방법
1. Nickel nitrate hexahydrate 0.1396 g 과 Zinc nitrate hexahydrate 4.6172 g 과 Thiourea 2.4358 g 을 weighing하여 160mL DI water에 넣고 solution을 한 시간동안 stirring 시킨다. 2. Solution을 200mL Teflon-lined autoclave로 옮긴 후 heat rate 10℃/min 으로 200℃ 24시간 동안 hydrothermal method로 합성한다. 3. 실온에서 Teflon-lined autoclave를 식힌 후, Solvent와 Solute를 분리한 후에 Solute를 원심분리기를 사용하여 DI water와 Ethanol로 번갈아가며 두 번씩 세척해준다. 4. 60℃에서 얻은 생성물을 24시간동안 건조시킨 후 수득한다.
NiZnS 구리 도핑 진행
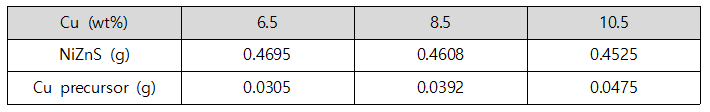
1. 위에서 합성한 NiZnS와 Copper nitrate hexahydrate을 하단의 표에 나온대로 weighing하여 80mL DI water에 넣고 solution을 한 시간동안 stirring 시킨다. 2. Solution을 100mL Teflon-lined autoclave로 옮긴 후 heat rate 10℃/min 으로 160℃ 8시간 동안 hydrothermal method로 합성한다. 3. 실온에서 Teflon-lined autoclave를 식힌 후, Solvent와 Solute를 분리한 후에 Solute를 원심분리기를 사용하여 DI water와 Ethanol로 번갈아가며 두 번씩 세척해준다. 4. 60℃에서 얻은 생성물을 24시간동안 건조시킨 후 수득한다.
수소 생산량 측정
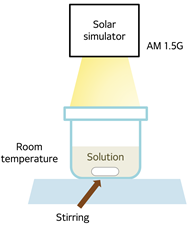
1. 광촉매 0.01g과 DI 40 mL를 바이알 병에 넣고 30분간 sonicating 시킨다. 2. 뚜껑이 수정판으로 된 300 mL의 pyrex 용기에 DI 20mL, Na₂S 5.0438 g, Na₂SO₃ 1.8906 g, 그리고 sonicating 시켰던 용액을 넣고 5분간 질소 퍼징하며 stirring한다. 3. Pyrex 용기를 solar simulator를 사용해 AM 1.5G 조건의 광원 하에 수소 생산을 진행한다. 1시간 간격으로 1 mL 용량의 시린지를 사용하여 수소 생산량을 측정한다.
수소 생산 안정성 측정
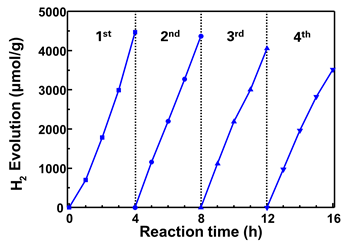
1. 광촉매 0.01g과 DI 40 mL를 바이알 병에 넣고 30분간 sonicating 시킨다. 2. 뚜껑이 수정판으로 된 300 mL의 pyrex 용기에 DI 20mL, Na₂S 5.0438 g, Na₂SO₃ 1.8906 g, 그리고 sonicating 시켰던 용액을 넣고 5분간 질소 퍼징하며 stirring한다. 3. Pyrex 용기를 solar simulator를 사용해 AM 1.5G 조건의 광원 하에 수소 생산을 진행한다. 1시간 간격으로 1 mL 용량의 시린지를 사용하여 수소 생산량을 측정한다. 4. 4시간동안 측정이 끝난 후, 5분간 질소 퍼징을 진행한 후 다시 3번처럼 수소 생산을 진행한다. 5. 4번을 3번 반복하여 총 16시간동안 수소 생산을 진행한다.
개발 과제 핵심 결과
Absorbance and band gap
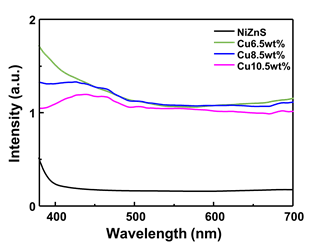
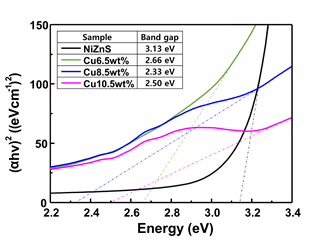
그림 8은 광촉매들의 광학적 특성을 파악하기 위해 가시광선영역을 분광 분석을 한 결과다. 자외선과 가까운 380nm 부터 약 450nm 까지는 구리 함량 증가에 따라 빛을 흡수하는 양이 감소하는 모습을 보인다. 하지만 그 이후의 대부분의 영역에서 구리가 도핑된 세 광촉매 모두 흡수량이 비슷해지며 공통적으로 구리가 도핑되지 않은 NiZnS보다 높은 수치를 보여주고있다. 이것으로 광촉매에 구리를 도핑하면 가시광선 영역의 빛 흡수가 보다 원활히 이루어지지만 구리의 함량에 따른 차이는 크지 않다는 것을 알 수 있다.
그림 9는 Tauc plot을 이용해 띠간격을 계산한 결과다. 구리를 도핑 하게되면 band gap이 큰폭으로 감소하는 것을 볼 수 있다. 구리의 함량을 6.5wt%에서 8.5wt%로 늘리면 band gap이 2.66eV에서 2.33eV까지 감소하지만 10.5wt%까지 늘렸을때의 band gap은 2.5eV로 다시 값이 증가하게 된다. 이를 통해 수소 생산을 위한 구리 도핑의 함량은 8.5wt%가 가장 효율적일 것이라고 예상할 수 있다.
SEM
NiZnS 샘플의 형태와 구조는 FE-SEM (field-emission scanning electron microscopy) 장치로 조사되었다. 그림 10에 나타난 것과 같이 NiZnS에 Cu가 doping된 촉매는 구체 모양으로 응집 정도는 서로 다르고 거친 표면을 갖는다. 그림 10-(a),(b),(c)는 비교적 작은 크기의 입자를 갖는 것으로 보이는 반면, 그림 10-(d)는 동일 배율 대비 비교적 큰 입자를 갖는 것으로 보인다. 이는 촉매의 성능에 중요한 변수이다. 촉매와 반응물이 닿는 계면의 면적은 반응 효율을 결정한다. (a), (b), (c) 의 지름은 약 5μm로, Cu가 10.5 wt% 로 doping된 입자의 지름이 약 8μm인 것에 비하면 작다. 따라서, 동일 무게에서 반응물인 물과 촉매 입자가 접촉하는 표면적이 넓어서 수소 생산량이 적어졌을 것이라고 추측된다.
XPS
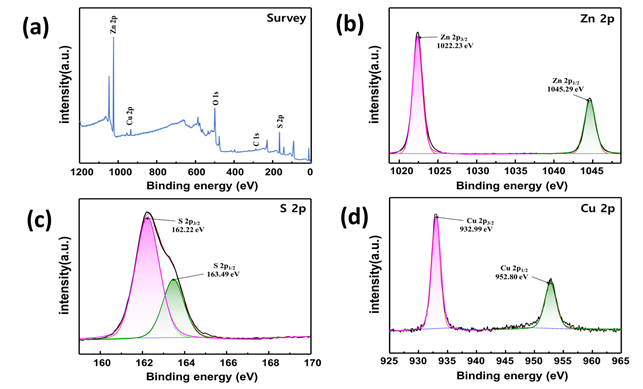
Cu가 doping된 NiZnS 광촉매의 표면에서의 화학적 특성을 알아보기 위해 XPS(X-ray photoelectron spectroscopy)를 통해 분석을 해보았다. 그림 11-(a)는 전체적인 스펙트럼을 보여주며, 아연, 구리, 황의 피크가 나타났다. 니켈은 소량이라 피크를 찾아보기 어려웠으며, C 1s peak인 284.6 eV를 기준으로 calibration 하였다. 그림 11-(b),(c),(d)는 Cu가 doping된 NiZnS 광촉매의 각각 Cu 2p, S 2p, Zn 2p 를 보여준다. Cu 2p 3/2와 Cu 2p 1/2의 binding energy는 각각 932.99eV, 952.8eV이고, S 2p 1/2와 S 2p 3/2의 binding energy는 163.49eV, 162.2 eV이며, Zn 2p 3/2와 Zn 2p 1/2의 binding energy는 각각 1022.23eV, 1045.29eV이다. 위의 결과는 다음과 같이 해석될 수 있다. 먼저, Zn는 Cu를 doping한 후에도 Zn2+의 산화 상태를 갖고 있기 때문에 눈에 띠는 peak shift를 보이지 않았다. 또한, S의 하나의 2p orbital이 나눠진 상태로 발견되었다. 마지막으로 Cu 2p의 peak가 두 개로 분리되어 나타났는데, 각각 metallic 혹은 cationic Cu를 나타낸다. 결론적으로, XPS 측정을 통해 Cu가 효과적으로 ZnS 입자 속으로 doping되었음을 알 수 있다.
수소 생산 결과
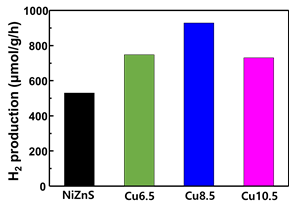
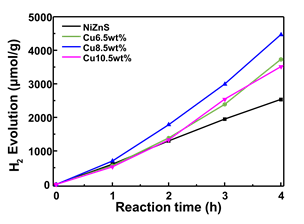
그림 12는 광촉매들의 수소생산을 4시간동안 측정한 값을 그래프로 나타낸 것이고, 그림 13은 광촉매들의 시간당 수소생산량이다. 광촉매에 구리를 도핑하고 그 함유량을 증가함시킬수록 수소 생산량이 증가했지만 구리 함량이 10.5wt%인 광촉매는 수소 생산량이 감소하였다. 구리 함량이 너무 많아 지면 NiZnS로 입사되는 빛을 차단하기 때문이다. 따라서 band gap이 가장 작았던 8.5wt% 의 구리가 도핑된 NiZnS 광촉매가 928.2 µmol/g/h 의 가장 높은 생산량을 보여주어 가장 우수한 촉매임을 확인했다.
광촉매의 안정성 평가
그림 14는 내구성 평가를 위해 4시간 동안의 실험을 4번 반복하여 진행한 결과다. 첫번째 실험에서 수소 생산 총량은 4471.6 µmol/g 이 나왔다. 두번째에서 4371.8 µmol/g 으로 실험을 반복할 수록 점차 감소하였다. 마지막 4번째 실험에서 3517.7 µmol/g 까지 감소해 21% 수준의 감소량을 보였다. 이런 현상은 황화물 광촉매를 오래 사용할 경우 일어나는 광부식이 원인으로 생각된다.
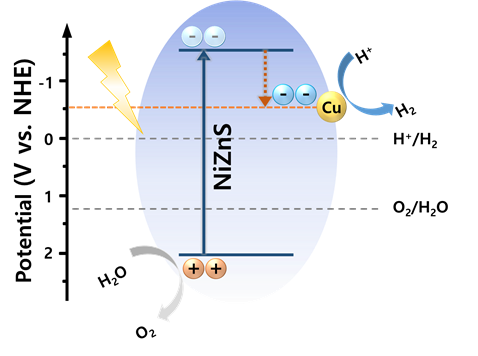
Band gap diagram
그림 15는 Cu-NiZnS의 band gap, 그리고 reference들을 참고하여 그린 schematic diagram이다. NiZnS는, ZnS의 3.54 eV라는 넓은 band gap을 보완하여 3.13 eV를 가진다. Ni은 광부식 억제 효과가 있으며 NiS₂, Ni₃S₂ 등 황과 다양한 결합이 가능해 여러 물질과의 heterojunction을 가능하게 하여 band gap이 줄어들었다고 추측된다. 이에 추가적으로 Cu 도핑을 시도하여 NiZnS의 높은 conduction band energy를 낮춰주며 위와 같은 band gap을 가졌을 것이라 판단된다. 결론적으로 기존보다 낮은 band gap으로 인해 더 낮은 에너지로도 수소 생산이 가능해지며 높은 수소생산 결과에 기인하였다고 사료된다.
평가
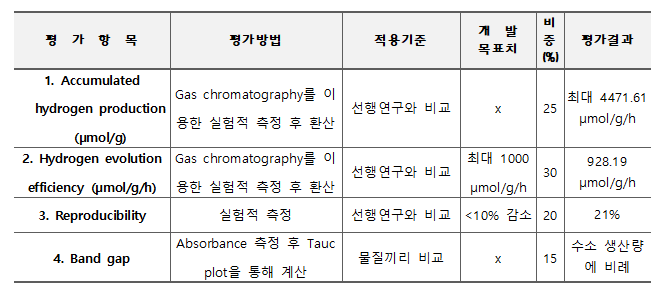
개발 과제 평가
개발 과제 관련 향후 전망
최근 환경문제를 해결하기 위해 세계가 주목하는 에너지 전환의 방안은 크게 두 가지로 재생에너지와 수소에 화학반응을 일으켜 전기를 생산하는 수소에너지를 활용하는 것이다. 그 중 수소에너지가 탄소중립의 핵심으로 꼽힌다. 수소경제 글로벌 CEO 협의체인 ‘수소위원회’는 2050년이면 세계 수소 소비량이 5억4600만t에 이를 것으로 추산했다. 이는 132억6천만배럴의 석유를 대체하는 규모로, 전세계 에너지 수요의 20%에 육박한다. 현재 대부분의 수소는 탄소와 수소로 구성된 천연가스에서 수소를 추출하는 천연가스 ‘개질(Reforming) 방식’으로 생산된다. 천연가스 개질 방식은 생산 비용이 저렴하지만 온실가스가 배출된다. 수소 산업에서 자주 거론되는 ‘부생 수소(석유화학 공정이나 철강 등을 만드는 과정에서 부수적으로 나오는 수소)’ 또한 생산과정에서 온실가스가 배출된다. 따라서 수소를 생산하는 방법도 연구가 필요하다. 생산 과정에서 온실가스 배출이 없는 ‘그린수소’로 가장 하나가 광촉매를 이용한 것이다. 따라서 관련 연구 전망도 밝을 것으로 보인다.
또한, 광촉매는 수처리나, 공기에서의 화학 물질을 분해하여 무해한 물질로 변환시켜 오염물질의 분해와 자정작용이 있도록 하는 등의 기능이 있어 다른 많은 분야에 널리 사용될 수 있다. 현재 광촉매를 사용한 수소발생 방식은 효율이 낮아 상용화 단계의 경제성을 확보하지 못했다. 하지만, 수소에너지원은 중요한 에너지원이며 물분해 광촉매 수소생산은 장래에 꼭 실현시켜야 하는 과제이다.
포스터
파일:프로젝트종합설계 최종과제 포스터 삼종접합(김주현).pdf