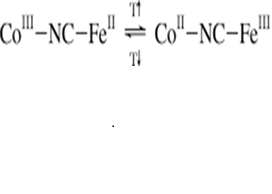Battery Flow
프로젝트 개요
기술개발 과제
국문 : Redox-Target Redox Flow Battery 에 대한 설계 및 성능 향상
영문 : Design and Performance Enhancement of Redox-Target Redox Flow Battery
과제 팀명
Battery Flow
지도교수
이두환 교수님
개발기간
2023년 9월 ~ 2023년 12월 (총 4개월)
구성원 소개
서울시립대학교 화학공학과 2017340044 조재호(팀장)
서울시립대학교 화학공학과 2020340054 이승기
서울시립대학교 화학공학과 2018890046 심형석
서울시립대학교 화학공학과 2018890047 안유현
서울시립대학교 화학공학과 2019340013 김주향
서론
개발 과제의 개요
개발 과제 요약
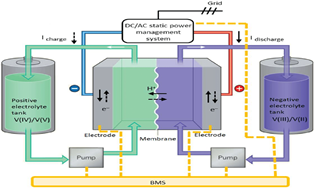
◇ ESS(Energy Storage System)의 종류는 크게 에너지 저장 기술에 따라 화학적 저장, 전자기적 저장, 열역학적 저정, 물리적 저장으로 나뉜다. 이번에는 화학적 저장 중 플로우 배터리인 VRFB(Vanadium Redox Flow Battery)에 대해 연구한다.
◇ VRFB(Vanadium Redox Flow Battery)는 LIB(Lithium Ion Battery)와 비교했을 시, 안전성이 좋고 약 30년으로 긴 수명이 가지고, 낮은 에너지 밀도로 인해 ESS에 적용하기에는 어려움이 있다.
◇ VRFB 탱크에 RT(Redox Target)물질을 넣어 활성물질인 바나듐과 산화환원 반응을 통해 전자를 RT물질에 저장 또는 방출하면서 에너지 저장 밀도를 높여줄 수 있다.
◇ 이번 연구에서는 VRFB 환경에서 사용 가능한 새로운 RT물질을 찾고자 한다.
◇ 새로운 RT물질이 VRFB에 적용 가능한 여부는 1. RT물질이 배터리 재료의 Femi level과 비슷한 값의 표준 전위를 갖는 가역적 환원 종이여야 하고, 2. RT물질의 산화환원 전위 중 하나가 활성물질보다 낮고, 다른 하나는 활성물질보다 높아야 한다.
개발 과제의 배경
◇ 최근 지구온난화로 인해 각국에서는 신재생에너지의 비중을 높이고 있는 추세이다. 하지만 신재생에너지는 시간, 날씨와 같은 주변 환경의 영향을 크게 받으며 이로 인해 출력량을 예측하기 어렵다(재생에너지의 간헐성).
◇ 신재생에너지의 단점들을 보완하기 위해 에너지 저장 기술인 ESS가 도입되었다. ESS는 예비전력 저장을 통한 피크시간대에 전력망의 부담을 줄여주고, 환경에 따라 변동성이 큰 발전량을 보완할 수 있으며 ,마지막으로 전력공급 불안정 시 주파수를 안정시킬 수 있다.
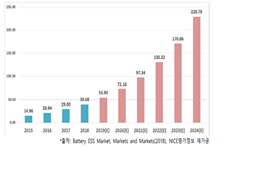
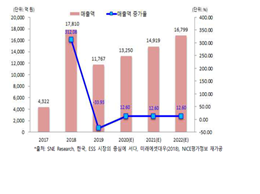
◇ 이러한 ESS의 장점으로 인해 각국에서는 ESS 시장 규모가 급증하고 있다. 이를 통해 ESS는 국내외적으로 성장 가능성이 크고 ESS에 대한 연구의 필요성이 지속적으로 높아질 분야라고 생각하였다.
◇ VRFB는 수계 전해질을 사용함으로써 화재 위험성이 없다. 또, 약 30년이라는 긴 사이클 수명을 가지고 있고 전해질의 부피를 늘려 에너지 저장 용량을 향상시키고 전극의 크기를 늘려 출력 전력을 높임으로써 LIB에 비해 용량 확장과 설계에 유연하다. 이러한 장점으로 인해 VRFB는 현재 ESS 시장에서 주목 받고 있다.
◇ 이러한 장점들에도 불구하고 현재 VRFB는 에너지 밀도가 낮다라는 단점이 있다. 이를 극복하기 위해 탱크에 RT물질을 넣어 활성물질인 바나듐과 서로 반응하여 전자를 RT물질에 저장 또는 방출하면서 에너지 저장밀도를 높여준다.
◇ 따라서, 이번 연구에서는 VRFB에 적용가능한 새로운 RT물질을 찾는 것이 목표이다.
개발 과제의 목표 및 내용
◇ VRFB의 에너지 저장밀도를 높여주는 새로운 RT물질을 찾는다.
◇ 논문 리뷰 결과 이번 연구에 RT물질로 사용가능하다고 판단한 물질은 5가지이며, 경제성, 합성 용이성 등을 근거로 5개 중 2개인 PANI-FeCoPBA, K-V-Fe-PBA를 합성한다.
◇ 합성된 물질이 실제 VRFB에서 RT물질로 적용가능한지 CV를 통해 확인한다.
◇ 이때, 고체 시료만의 전기화학적 성질을 확인하는 RDE(Rotating Disk Electrode)를 사용하여 활성물질과 RT물질의 CV 데이터를 얻는다.
관련 기술의 현황
관련 기술의 현황 및 분석(State of art)
- 전 세계적인 기술현황
◇ Flow battery의 전류 밀도를 증가시키기 위하여 다양한 연구가 진행되고 있다. 이두환 등 4인(2023) 연구에서는 VRFB Carbon electrode 표면의 heteroatom 도핑을 연구하였다. 해당 연구의 경우, VRFB의 전극에 집중하여 Carbon felt 전극 표면에 Boron, Oxygen과 같이 Heteroatom을 도핑하여 전극의 성능 변화를 확인하고, 성능이 변화하는 메커니즘을 연구하였다.
◇ Yuanhang Cheng 등 12인(2019) 연구에서는 Redox targeting을 VRFB에 최초로 적용하였다. 해당 논문에서는, Prussian Blue Analogue, 또는 (VO)6[Fe(CN)6]3을 사용하였다. 해당 물질을 Granule 형태로 만들어 Catholyte tank 안에 삽입한 결과, PBA를 5g만 첨가했음에도 0.6M 바나듐 농도 전지가 5.0M 바나듐 전지와 동일한 전류밀도를 가지게 되었다. RT반응을 통해 특정 전류밀도에 도달하는 데 필요한 바나듐 농도를 줄임에 따라, 전지에 필요한 바나듐 양이 감소하여 경제성이 증가하였을 뿐만 아니라 전지의 온도 안정성 역시 크게 상승하였다.
◇ Sabrian Berling 등 6인(2022) 연구에서는 VRFB의 RT에서 기존의 무기물질 대신 유기물 Lignin을 사용하였다. Lignin은 폐 펄프와 같은 종이 기반 폐기물에서 추출할 수 있어 친환경적일 뿐만 아니라 다양한 활성 작용기의 존재로 redox 반응이 가능해, 친환경 흐름에 맞추어 리그닌을 전기화학적 cell에 응용하는 방안이 여럿 연구되고 있는데, 이 또한 그 일환이다.
- 특허조사
◇ Stable and High-capacity Neutral Aqueous Redox Flow Lithium Battery Based on a Redox-Targeting Reaction
본 발명은 Redox-targeting 반응을 이용한 안정적이고 고용량의 중성 수계 redox flow 리튬 배터리에 관한 것이다. 해당 flow 리튬 배터리는 양극 전해질액 탱크와 음극 전해질액 탱크로 구성되어 있다. 양극 전해질 탱크에는 [Fe(CN)6]4− 또는 [Fe(CN)6]3− 염이 포함된 양극 전해질과 함께, 탱크 내부에 추가적으로 LFP(Lithium Iron Phosphate) 혹은 FP입자가 포함된다. 이 flow 리튬 배터리는 대용량 에너지 저장 분야에서 다양한 활용이 가능할 것으로 기대된다.
◇ A condensed phase aqueous redox flow battery
본 발명은 음극 전해질 탱크와 양극 전해질 탱크로 구성된 응축 상 redox flow 전지(CARB, Condensed phase redox flow battery)를 골자로 한다. 전해질 탱크에는 전기적으로 활성화된 고체물질이 포함되어 있는데, 이때 이 물질들은 PB(Prussian blue), PBA, PB 수화물, 또는 기타 다른 물질이다. - CARB를 통해 기존의 Flow battery의 한계점인 낮은 전지 성능, cycling 안정성을 극복하고 실제 산업에 이용될 수 있는 전지를 생산할 수 있다.
◇ Cobalt ferricyanide solid energy storage material applied to flow battery and preparation method thereof
본 발명은 흐름 전지에 cobalt iron cyanide(CoFe-PBA)를 고체 에너지저장 물질로 사용하는 방법과, 해당 물질의 제작법을 골자로 한다. TEMPO는 기존 Flow 전지의 수계 전해질 활성물질에 비해 산화환원 가역성이 높고 친환경적이라는 장점이 있다. 하지만 산화환원 potential이 높아 RT반응을 이용하여 전지의 에너지밀도를 높일 수 없다는 단점이 있다. 이에 따라 본 발명은 TEMPO와 Redox potential이 일치하는 물질인 cobalt iron cyanide의 합성 방법을 제시하고, 해당 물질이 고체 에너지저장물질로 사용 가능함을 확인하였다.
◇ Flow batteries with insoluble polymer supported redox active materials
본 발명은 불용해성인, 작용기를 부착한 고분자 bead를 전해질 탱크 내부에 포함하여 bead의 산화-환원반응에 활성화된 부분에 전자를 저장하는 redox matched flow battery의 구성과, 해당 Bead의 합성 방법에 관한 것이다. 해당 활성 Bead는 resin bead xPS-Cl에 -viologen group, ferrocene 혹은 cyclopropenium기를 부착하여 만들어진다. 이 bead를 flow 전지에 포함해 기존 Flow 전지에 비해 성능이 향상된 RMFB를 제작할 수 있다.
- 특허전략
◇ 다양한 수계 배터리에 사용된 여러 RT물질을 확인할 수 있었다. 주로 PBA계 금속화합물이 사용되었지만, LFP 또는 고분자계 물질 역시 사용되었다. 하지만 VRFB를 대상으로 한 RT물질의 특허는 1개만 찾아볼 수 있었고, 그 역시 구체적으로 RT물질 및 그 합성법을 제시한 것이 아닌 RT라는 기법에 대한 개념 및 여러 가지 가능한 물질을 포괄적으로 제시한 개념적 특허로 보인다. 따라서 특정 RT물질을 제시하고, 그에 대한 성능향상폭을 구체적으로 제시한다면 특허를 취득할 수 있을 것으로 보인다.
◇ Cobalt가 사용된 PBA가 특허가 존재하긴 하였지만, 우리가 사용한 물질의 경우 Co-Fe-PBA의 경우 PANI를 코팅하여 성능향상을 시도하였고, K-V-Fe PBA의 경우 기존 특허가 없기 때문에 해당 두 물질을 사용하여 특허의 신규성을 확보할 수 있다.
◇ 우리가 선정한 RT물질들에 대하여, 구체적인 합성방법을 제시하여 합성의 용이함을 제시한다. 그에 더하여, 새로운 RT물질을 적용한 전지가 기존 VRFB에 비하여 어떤 점에서 성능이 향상되는지 구체적으로 근거를 제시하여 진보성을 확보할 수 있다.
◇ 그에 더하여, 실제 ESS산업에 이용될 수 있도록 대량 합성방법을 고안하고, 해당 물질이 기존 PBA에 비하여 비용적 이점이 있는지 기반 원소 가격, 합성 재료 가격 등을 이용하여 제시한다면 산업적 이용 가능성을 확보할 수 있다.
개발과제의 기대효과
기술적 기대효과
◇ PBA는 상온에서 수용액상에서의 공침반응을 통해 합성 되기 때문에 경제적이며 친환경적으로 생산된다. 그러나 이러한 PBA중 VRFB에 적합한 물질은 아직까지 발견되지 않았다. 그에 따라서 다른 배터리에 사용하던 Redox Target Material인 Prussian Blue Analogue를 구조적 측면 및 이유들에 따라서 RDE측정을 통해 산화환원 그래프를 확인하여 VRFB에 사용하기 적절한 Redox Target Material을 개발한다.
◇화석연료와 기후 변화에 대한 우려로 태양광, 풍력 등의 신재생에너지의 중요성은 대두되고 있다. 그리고 이러한 에너지원을 안정적으로 만들기 위해서는 에너지 저장 시스템(ESS)가 필수적이며, 가장 각광받는 ESS는 VRFB이다. VRFB는 전해액에 에너지가 저장되지만 낮은 에너지 밀도를 가진다는 단점이 존재한다. 그렇기 때문에 VRFB와 호환이 되는 적절한 Redox Target material을 개발한다면 낮은 에너지 저장밀도를 높일 수 있을 것이다.
◇PBA는 크기 기반 흡착 모델을 가정하면 상당한 암모늄의 흡착능력을 가지게 되어 폐수에 포함되어 있는 암모늄을 제거할 수 있는 기술을 개발할 수 있다. 이러한 PBA는 친환경기술로 활용될 수도 있다. 이 밖에도 PBA는 세슘 등의 방사성 동위원소와 같은 특정 유형의 중금속 중독에 대한 해독제로 사용되는 등 의학적으로도 사용이 가능하다.
경제적, 사회적 기대 및 파급효과
◇VRFB의 에너지 저장 밀도는 LIB(리튬이온 배터리)의 1/10 수준으로 상대적으로 저조한 편에 속한다. 그러나 충반전의 수명이 LIB는 5000cycle이며 VRFB는 15,000~20,000cycle이라는 점에서 전지의 높은 수명을 가지고 있다. 그렇기 때문에 Redox Target Material을 첨가하여 에너지 저장 밀도를 높인다면 안정적인 전력공급 환경을 구축할 수 있을 것이다. 현재 신재생에너지는 환경오염으로 투자가 증가하고 있는 추세이다. 그에 따라 에너지 저장장치의 중요성도 증가하고 있기에 Redox Target Material을 사용하여 VRFB를 상용화하게 되는 것은 환경적으로 강한 이점을 가질 수 있다.
◇Prussian Blue Analogue는 산화환원을 촉진시키는 역할을 하기 때문에 VRFB에 사용 될 경우 높은 이론 용량을 가질 수 있다. 그리고 PBA는 산화환원 매개체가 저렴한 Fe로 이루어져있다. 그렇기 때문에 PBA를 사용한다면 VRFB의 전해액으로 쓰이는 Fe에 비해 상대적으로 고가인 Vanadium양을 줄일 수 있어 경제성에서 다른 RFB에 비해 우위성을 점할 수 있다.
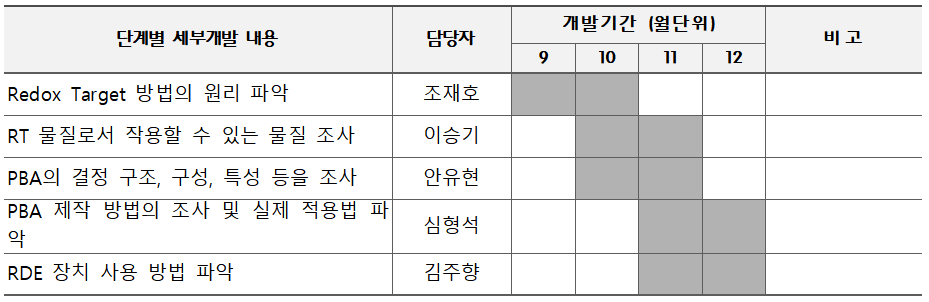
구성원 및 추진체계
◇조재호 : VRFB의 원리와 단점을 파악하고 이를 해결하기 위한 Redox Target 방법의 원리 분석 ◇이승기 : VRFB의 RT 물질로서 작용할 수 있는 물질 조사 및 현상 분석 ◇안유현 : PBA의 결정 구조, 구성, 특성 등을 조사하고 파악하여 RT 물질로서의 가능성 탐구 ◇심형석 : 기존 논문들을 참고하여 PBA 제작 방법의 조사 및 실제 적용법 파악 ◇김주향 : PBA의 RT 반응의 가능성 파악을 위한 RDE 장치 사용 방법 및 해석 파악
설계
사전 조사
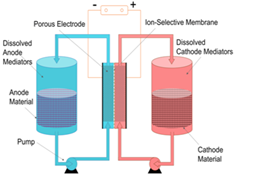
Redox Targeting의 원리
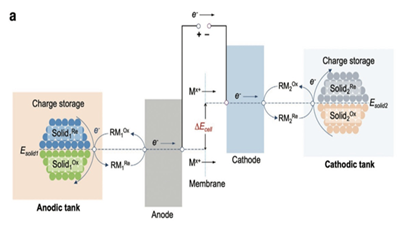
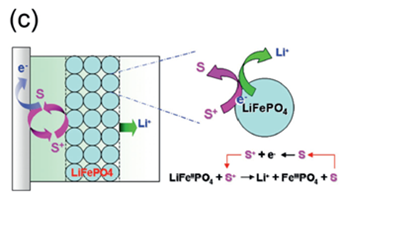
위 그림에서처럼, 충전 프로세스 동안 산화환원 매개체(S로 표시)는 전극에서 S+로 산화된다. 그 후 S+는 배터리 물질(LiFePO4 여기서)로 확산되어 S+의 전위가 높으면 물질을 추가로 산화하여 FePO4로 변한다. 결과적으로 분자는 다시 S로 환원되어 전극으로 확산되어 새로운 반응 라운드를 위해 준비된다. 역으로 방전 프로세스 동안 S의 전위가 FePO4보다 낮으면 S는 LiFePO4로 확산될 때 Li+가 존재하는 상황에서 후자를 환원된다. 결과적으로 매개체 자체는 S+로 산화되어 전극으로 확산되어 또 다른 반응 주기를 위해 돌아간다.
Redox Targeting 물질 선정
- RT물질의 조건
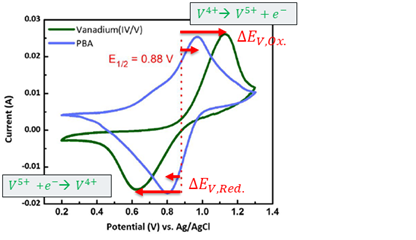
전해질 용액에 투입되어 Redox Target이 진행되는지를 확인하기 위해서는 Redox material 의 산화-환원potential이 바나듐 산화-환원 potential과 그림과 같이 형성되어야 한다. Redox Target 물질의 standard potential(anodic peak potential과 cathodic peak potential의 중간)을 기준으로 바나듐의 산화-환원 포텐셜 peak를 비교하면 된다. 그림과 같이 산화-환원 potential 관계가 형성되면, 전해질 탱크 내에서의 Redox Target 물질과 바나듐 이온(V4+,V5+)간의 자발적인 산화-환원 원동력이 형성되어 탱크 내에서의 산화-환원 반응이 진행된다.
- 후보 물질
◇Na-Mn-Fe PBA
Na와 Mn으로 구성된 PBA다. 구조는 lattice 구조를 가지며, 합성 과정에서 내부에 ferrocyanide defect가 포함될 수도 있다. 해당 PBA는 Zn ion 전지, rechargeable aqueous proton battery(APB)의 양극재 등 기존에 여러 전기화학적 분야에서 사용되어 왔다. 수계 전해질을 사용하고 Na+나 Zn+보다 이온 반지름이 작은 V 이온을 사용하는 VRFB에서도 Na-Mn-Fe PBA를 RT물질로 사용할 수 있다고 판단하여 후보로 선정하였다.
◇PbO2
PbO2는 VRFB의 탄소전극 표면을 전기적으로 활성화시키는 Dopant로도 사용된다. 또한 PbO2의 peak가 V의 peak보다 넓기 때문에 redox targeting 물질로 기능할 수 있다고 추정된다. 이에 따라 PbO2가 RT물질로 가능성을 갖는다고 판단하였다.
◇PANI(Polyaniline) + Fe-Co PB
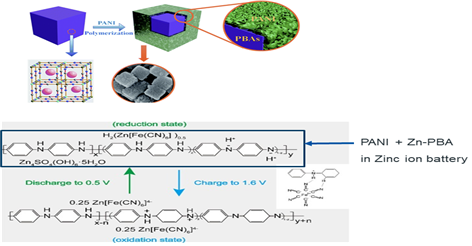
구조는 위 그림과 같다. 보라색 정육면체가 PBA이며 이를 감싸고 있는 초록색 부분이 PANI이고, SEM 이미지와 같이 정육면체 형태를 띠고 있다. 기존 PBA는 V에서 안정적인 포텐셜을 가지면서 RT물질에 적합하지만 낮은 전기전도성 및 산성 또는 염기성 매질에서 구조적 불안정성을 가진다는 단점이 있다. PANI는 높은 전기전도성 및 무독성, 합성 용이의 장점을 가지고 있는 반면, V 전해질에서 열역학적 불안정성을 가지는 경향이 있다. 이를 극복하기 위해 PBA와 PANI를 결합하여 열역학적 및 구조적 안정성을 높여주고, 전기전도성을 향상시켜 많은 에너지를 저장하는 RT물질로 적합하다고 판단하였다.
◇V/Fe PBA
V/Fe PBA의 구조는 위 그림과 같다. 파란색은 V, 초록색은 Fe, 빨간색은 C, 보라색은 N, 노란색은 Na이다. Sodium 배터리에 사용되는 PBA이며 HCl을 첨가하면 C와 N의 단단한 결합으로 결정구조를 만들면서 전기화학적 능력이 향상된다. V/Fe PBA를 구성하는 V 이온은 2가에서 5가 범위의 다양한 산화 상태를 가지며, 수성 전해질이 안정적으로 유지되는 전위 창 내에서 용이한 전기화학적 가용성을 나타낸다. Fe 이온은 수성 전해질 시스템에서 전기화학적으로 활성화 되며 2개의 서로 다른 Fe 원자가 전자 이동 반응을 견딜 수 있어 2전자 산화 환원 반응을 완전히 활용 가능하다. 따라서 두 원소의 특징이 RT 물질에 적합하다고 판정하였다.
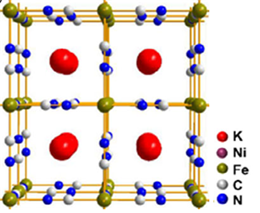
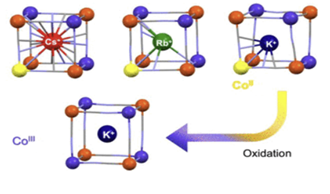
◇K-V-Fe PBA Nanocubes
K-V-Fe PBA는 K14V4O9[Fe(CN)6]3·21.4H2O와 유사한 구조를 가진다. V 원자가 VO2+ 이온의 상태로 PBAs framework 안에 있는 형태이다. 수성 전해질에서 V 이온이 산화-환원 반응 동안 공기 중의 O 이온과 결합해 생성된 중간체 VO2+는 수성 전해질에 쉽게 용해되어 용량 손실과 구조 파괴를 유발한다. 따라서 안정성이 높은 PBAs framework와 결합하여 복합재료를 형성한 K-V-Fe PBA Nanocubes는 용량이 높고 비용이 합리적이며 우수한 사이클링 안정성을 보이므로 RT 물질로 적합하다고 판단하였다.
- 최종 선정 물질 및 선정 기준
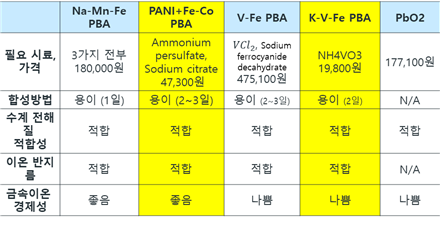
후보로 선정한 5가지 물질 모두 합성에 소요되는 시간이 3일 이내로 합성이 매우 용이하였다. 또한 모두 수계 전해질에서 사용이 적합하며 Framework 구조가 바나듐 이온을 통과시킬 수 있다. 따라서 경제성을 중점으로 판단하였다. 각각의 PBA에 포함된 금속 이온의 경제성을 따져보았을 때 V를 포함한 PBA와 PbO2는 비교적 경제성이 좋지 못하다고 판단하였다. 상단의 기준에 더하여, 실험 시의 환경과 재실험의 가능성까지 고려하였다. 따라서 우리는 필요 시료의 가격이 낮고 합성 방법이 용이한 후보들 중 V가 포함되지 않은 PANI+Fe-Co PBA와 V를 포함하고 있는 K-V-Fe PBA를 선정하여 실험을 진행하였다.
실험 방법
K-V-Fe PBA 합성
1. 비커에 70mL DI water, 3.6mmol NH3VO4 , 2.4mmol K3(Fe(CN)6] , 9.0mmol oxalic acid를 넣고 상온에서 혼합이 완료될 때까지 electromagnetic stirring 실시
2. Solution을 autoclave로 옮겨 180°C, 8h 유지
3. 상온까지 냉각
4. 원심분리 후 침전물을 3회 증류수와 알코올로 세척
5. 세척한 침전물을 오븐에 60°C, 8h 건조
PANI-Co-Fe-PBA 합성
◇ Fe-Co PBA 합성
1. 염화코발트(CoCl2*6H2O, 2.5mmol)와 구연산나트륨(Na3C6H5O7*H2O, 6mmo)을 80mL의 증류수에 용해시켜 투명한 생성물 형성 -> 용액 A
2. (1.5 mmol)을 증류수 80ml에 용해 -> 용액 B
3. 용액 A와 B를 magnetic stirring을 통해 24h stirring
4. 원심분리기로 어두운 보라색 침전물을 증류수와 에탄올로 세척
5. 24h, 60 °C로 진공 건조
◇ PANI + Fe-Co PBA 합성
1. Fe-Co PBA을 HCl(0.01M, 50ml)에 넣어 1시간 동안 sonication -> 용액 C
2. aniline(C6H7N, 0.5mmol)을 용액 C에 천천히 첨가하고 1시간 동안 stirring
3. Ammonium persulfate ((NH4)2S2O8, 0.5 mmol)을 HCl(0.01M, 50ml)에 용해 -> 용액 D
4. 얼음조에 용액 C를 강렬하게 교반하면서 용액 D를 2ml/min로 주입
5. 얼음조에서 혼합된 용액(C+D)를 12시간 동안 강렬하게 stirring
6. 원심분리기를 통해 침전된 PANI+Fe-Co PBA를 증류수와 에탄올을 통해 세척
7. 12h, 150 °C로 진공 건조
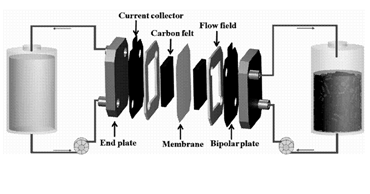
RDE 측정
RDE란 Rotating Disk Electrode로 3전극 중 working electrode가 일정한 rpm으로 회전시킬 수 있는 전기화학 측정용 전극이다. RDE를 사용하면 회전으로 convection에 의해 diffusion layer가 감소하고 전극 표면에 반응물의 전달이 빨라져 steady state에 도달한 상태의 값을 얻을 수 있다. 또한 다른 종류의 전극과 달리, 외부적인 요소에 영향을 받지 않고 전극 위에 올리는 고체 시료만의 전기화학적 성능을 확인할 수 있다. 따라서 합성한 시료만의 CV를 측정하기 위해 RDE를 사용한다. 그러나 우리 실험의 경우, 회전을 주고 CV를 측정하면 GC(Glassy carbon) 위의 고체시료가 떨어지는 현상을 보였으므로 RPM은 없이 측정하였다.
결과 및 평가
실험 결과
K-V-Fe PBA
- 합성 및 CV 측정
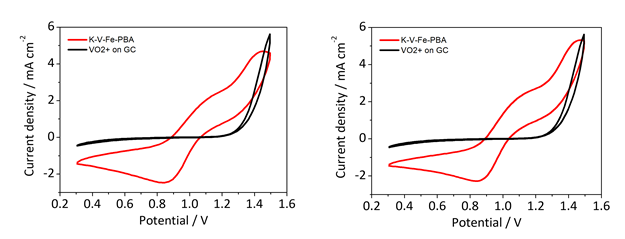
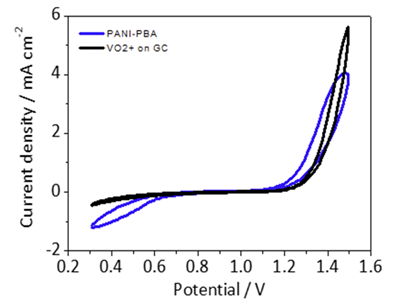
Scan rate 50mV, 전해질 용액 조성 0.1M VOSO4 + 3.0M H2SO4 조건 하에서, 전극 회전속도 0으로 하여 RDE CV 측정을 진행하였다.
- CV 결과 데이터 분석
해당 그래프들은 CV 각 사이클의 데이터를 평균화하여, Prisitine GC와 K-V PBA Coated GC 2개의 CV 그래프를 비교한 것이다. 공통적으로 1.17V에서 Anodic peak current, 0.83V에서 cathodic peak current가 관찰된다. 그 외에도 1.3V, 1.45V 가량에서 추가적인 peak가 관찰되는데 이는 부반응의 산화환원 peak가 관측된 것으로 예상한다. Pristine 상황에서 V4+/V5+ 산화환원 반응의 Potential은 각각 1.4V, 0.45V로 측정되었다. 이를 K-V-Fe-PBA의 산화환원 반응과 비교하면, 산화 potential은 V4+/5+>K-V-Fe PBA, 환원 Potential은 V4+/5+<K-V-Fe PBA이다. 이를 통해, K-V-Fe PBA는 VRFB의 Redox Targeting 물질로 사용될 수 있음을 확인하였다.
- 반응 메커니즘 분석
◇ PBA 주 반응
환원: 전해질 상 V4+->V5+ +e-, 해당 전자를 받아 Framework 내부(VO2)+ +e- ->(VO)2+ 로 환원
산화: Framework 내부 (VO)2+->(VO2)+ +e-로 산화
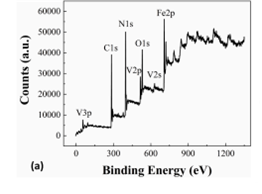
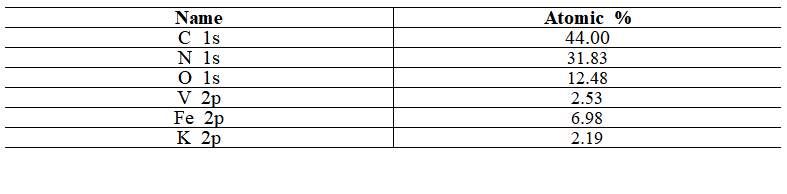
◇ PBA 부 반응
PBA의 XPS 데이터에 따르면, vanadium과 potassium의 원자 비율이 비슷하다. (2.53:2.19) 이를 통해 Framework 내부에 들어가는 전이금속이 기존 포타슘에서 모두 바나듐으로 전환되지는 않았다는 것을 알 수 있다. 이에 따라 포타슘 이온의 산화환원이 부반응으로 나타날 수 있다. K+는 PBA framework에 대해 강한 선호도를 가진다. 그래서 PBA framework에 접근하여 격자 변형을 낮추고 빠른 이온 확산을 가능하게 한다. 또한 K+는 그 반경이 작아서 수용성, 비수용성 전해질에서 높은 이온 전도도와 이온 전달 수에 기여한다. 측정한 CV 그래프에서 부반응에 해당하는 peak를 보면 높은 전위값을 가지는데, 이는 PBA와 K+사이 좋은 상호 호환성이 더 낮은 깁스 프리 에너지로 이어져 따라서 더 높은 산화 환원 전위로 이어진 결과라고 추론하였다.
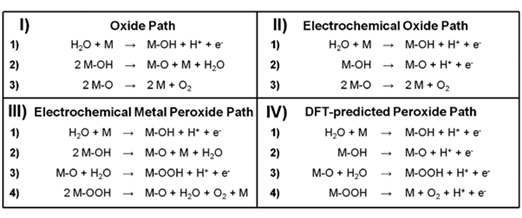
또 다른 부반응으로는, 물의 전기분해로 산소가 발생하는 OER(Oxygen Evolution Reaction)을 예상한다. OER의 메커니즘은 현재까지도 정확히 규명되지 않았지만, 그림과 같이 진행될 것으로 추측된다. 4가지 경우 모두에 대해, Gibbs free energy에 의한 kinetic barrier를 넘고 반응이 진행되는 standard reaction potential E0=1.23V (1.60V vs SHE)이다. 분자단위 구성 조작이 가능한 pba 특성상, 단일 고분자 framework 단위체에 다량의 catalytic 전이금속 원자가 존재하며, 이들 원자는 framework에 강하게 결합되어 있기에 해당 OER을 촉진하기 적합하다. 또한 PBA의 개방형 Framework 구조로 mass transfer 역시 활발하게 일어나 OER의 catalyst로 작용한다. 해당 OER반응의 standard reaction potential보다 높은 전류를 흘려주었고, PBA의 촉매작용으로 OER의 kinetic barrier 역시 낮아져 RDE 전극 표면에서도 OER이 진행되었을 것으로 보인다. 그에 따라, 물분자가 분해되어 PBA 표면에 부착되는 과정에서의 Reaction potential이 관측된다.
PANI-Co-Fe-PBA
- CV 결과 데이터 분석
CV 각 사이클의 데이터를 평균화하여, Prisitine GC와 비교한 결과 산화, 환원 피크가 없는 것이라고 확인되었다. 실제 RDE를 할 당시, PANI-CoFePBA을 올린 GC 전극을 바나듐 전해질에 넣자마자 PANI-CoFePBA가 GC전극에서 떨어져 가라앉게 되었다. 이로 인해, RDE측정시 PANI-CoFePBA의 영향보다 GC전극의 영향이 우세하여 피크가 없거나 매우 작고 Pristine 데이터와 유사하게 나온 것이라고 예상한다.
- 오류 원인 분석
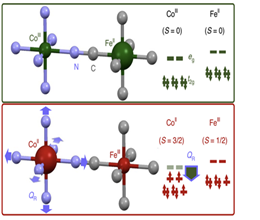
◇ CoFePBA 합성 당시 또는 RDE 측정 과정에서 발생할 수 있는 구조적 불안정성이 존재한다. CoFePBA는 PBA 격자구조를 유지하는 Cobalt의 산화수(2+ or 3+)에 따라 그리고 PBA 격자구조 내부에 들어오는 양이온의 이온반지름의 크기에 따라 PBA 격자의 구조적 불안정성이 생긴다. 구체적으로 Co3+일 경우에는 어떤 양이온이 들어와도 격자구조의 왜곡은 발생하지 않는다. 하지만 Co2+이고 양이온의 이온반지름 크기가 작을수록 격자 구조 왜곡이 커진다. K+의 이온 반지름은 138pm임에 반해 이번 연구에서 사용한 바나듐 전해질은 V4+, V5+이며 이온 반지름은 72pm, 68pm로 약 2배 가까이 작다. 이로 인해 V5+가 Co2+와 결합하면서 PBA의 격자구조가 불안정해져서 다른 부분의 결합이 깨질 수 있다.
추가로 CoFePBA 합성 과정에서 발생할 수 있는 오차를 확인해 보자. CoFePBA는 200K 부근에서 Cobalt의 산화수가 결정된다. 200K이하에서 합성이 진행될 경우, Co3+가 격자 구조 내부에 우세하고 200K 이상일 경우, Co2+가 격자 구조 내부에 우세하다. 이번 연구에서 CoFePBA을 합성할 때, 얼음조 조건에서 단순히 얼음을 주위에 감싸 스터링을 진행했다. 이로 인해 합성 당시 CoFePBA의 온도는 273K부근으로 예상되고 이로 인해 Co2+가 격자구조 내부에 주로 이루어질 것이라고 예상할 수 있다.
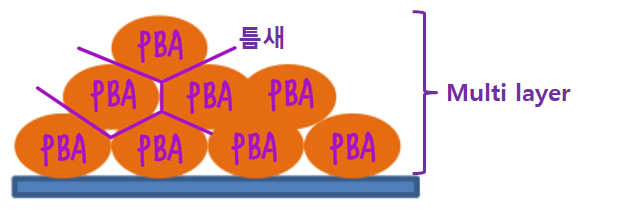
◇ Prussian Blue Analogue의 주요 원소인 Co,Fe,Ni과 같은 전이금속 산화물은 매우 높은 활성을 가지고 낮은 pH에서 부식을 겪게 된다. RDE 측정시에 PBA와 에탄올 혼합물을 전극위에 여러번 적층시키며 Multi Layer가 생성됐을 것이며, layer사이사이에 틈새가 발생하며 접착력이 강하게 발생되지는 않았을 것으로 추측된다. 이로 인해 PANI-CoFePBA의 Multi Layer사이로 바나듐 전해질이 스며들어 전극 위 PANI-CoFePBA가 떨어진 것이라고 예상할 수 있다. 이를 극복하기 위해 RDE측정시에 전극에 Binder역할을 할 수 있는 Nafion과 같은 물질을 첨가하면 더 정확한 측정을 할 수 있을 것이라 기대된다.
개발 과제 평가
향후 전망
현재 지구촌은 과도한 탄소배출로 심각한 환경오염과, 그에 따른 기후변화로 고통받고 있다. 그에 따라 세계는 탄소배출이 없는 신재생에너지에 많은 투자를 하고 있고 2030년에는 태양광과 풍력의 생산비용이 각각 50%,20% 하락을 예상되고 있다. 그러나 태양광 및 풍력과 같은 발전으로 발생하는 신재생에너지는 발전의 특성상 전력공급이 불안정하다. 그렇기 때문에 신재생에너지의 필요성이 증가하는 만큼 에너지 저장장치의 필요성 또한 증가하고, 에너지 저장장치로써 가장 각광받는 Vanadium Redox Flow Battery의 필요성 역시 증대될 것이다. 낮은 에너지 저장밀도라는 단점은 Redox Target Material인 Prussian Blue Analogue를 사용하여 개선될 것이며, 또한 경제적으로 부담이었던 고가의 Vanadium은 PBA의 산화환원 매개체인 저렴한 Fe에 의해 그 양이 이전보다 줄어들어 경제적 부담을 절감할 수 있을 것이다. 따라서 관련 연구 전망도 밝을 것으로 여겨진다.
또한 PBA는 에너지 저장장치의 산화환원 촉진제로 쓰일 뿐만 아니라, 폐수에 포함되어 있는 암모늄을 제거하는 친환경기술로 쓰이거나, 세슘등의 중금속 중독을 해독하는 용도로 사용되는 의학적 활용도 쓰일 수 있기 때문에 다른 분야에 널리 사용될 수 있다.
현재 Redox Target Material인 PBA의 산화환원 메커니즘은 아직 명확히 밝혀지지 않았다. 하지만, 미래에 신재생에너지 공급의 핵심인 에너지 저장장치의 효율성을 높일 수 있는 중요한 기술이라는 점에서 향후 반드시 기술확보가 이루어져야 하는 과제이다.