Yoo group조
프로젝트 개요
기술개발 과제
국문 : OER을 이용한 수소 생산 페로브스카이트 촉매 디자인
영문 : Designing high performance perovskite for hydrogen production with OER
과제 팀명
Yoo group
지도교수
유종석 교수님
개발기간
2019년 9월 ~ 2019년 12월 (총 4개월)
구성원 소개
서울시립대학교 화학공학과 20143400** 이**(팀장)
서울시립대학교 환경공학부 20148900** 박**
서울시립대학교 화학공학과 20143400** 박**
서울시립대학교 화학공학과 20143400** 이**
서론
개발 과제의 개요
개발 과제 요약
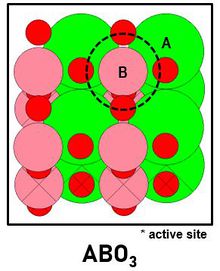
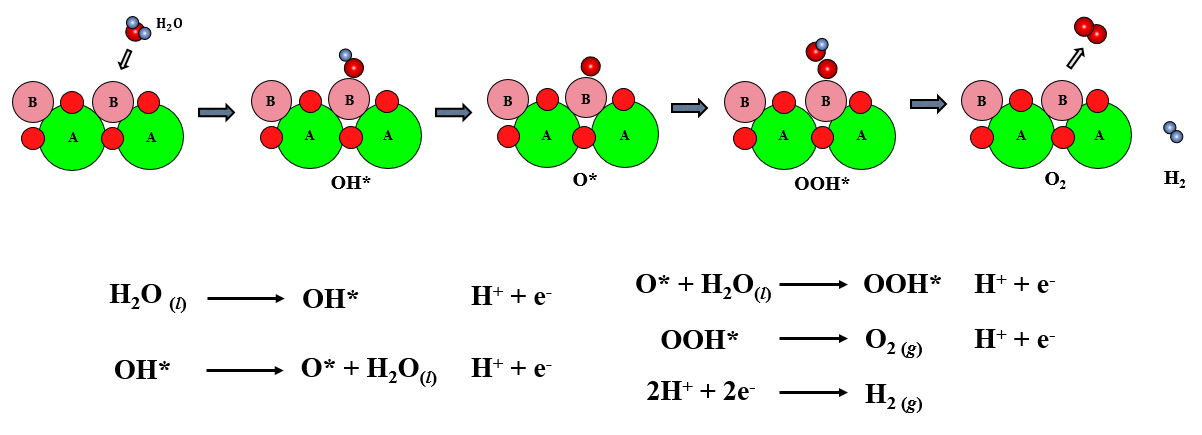
◇ 신에너지로서 수소 에너지가 각광받고 있으며, 물의 전기분해 방법을 통해 수소를 얻는 것이 친환경적이며 수소의 순도가 높은 방법이다. ◇ Perovskite( 구조) 촉매를 이용하여 OER(Oxygen Evolving Reaction)반응의 일종인 AEM(Adsorbate Evolution Mechanism) 반응으로 수소를 획득할 수 있다. ◇ 기존 perovskite를 기반으로 산소를 다른 anion으로 치환한 perovskite 물질도 계산하여 수소 생산 대비 에너지를 최소화 할 수 있는 촉매를 조사한다. ◇ 기존에 수소를 생산하기 위해 사용하던 화석 에너지의 사용을 줄여 장기적으로 경제적, 환경적 이익을 창출할 수 있다.
개발 과제의 배경
◇ 신에너지로서 수소 에너지의 필요성, 장점, 장래성이 대두되고 있다. ◇ 현재 수소 에너지 생산은 주로 화석연료를 통해 만들고 있기 때문에 환경오염 문제가 발생한다. ◇ 촉매를 개발하여 보다 적은 에너지로 수소 생산 극대화를 목표로 한다. ◇ 화석 에너지의 사용을 줄여 궁극적으로 경제적, 환경적 이익을 창출할 수 있다.
개발 과제의 목표 및 내용
◇ 목표 : 수소 에너지 생산에 가장 효율적인 perovskite 촉매 찾기 ◇ 물의 전기분해 반응의 일종인 OER 반응으로 수소 에너지 생산 ◇ 기존 perovskite(, )를 기반으로 산소를 다른 anion(C,N,F,Cl,S,P 등)으로 치환한 다양한 perovskite 물질에 대해서도 계산한다. ◇ DFT(Density Functional Theory)를 이용하여 컴퓨터 시뮬레이션 계산을 통해 에너지 측면에서 촉매의 OER 반응 경향성을 파악하고 효율적인 촉매를 개발한다. ◇ 각 촉매의 OER 반응에 대해 Energy diagram, Scaling relation, Volcano plot을 만들어 수소를 생산하는 데에 최소 에너지가 필요한 perovskite 촉매를 개발한다.
관련 기술의 현황
관련 기술의 현황 및 분석(State of art)
- 전 세계적인 기술현황
물의 전기분해, 화석연료를 수증기 개질, 부분산화, 바이오매스 가스화 또는 탄화, 열화학적 또는 광촉매, 생물학적기술로 제조하여 화학공업 및 전자공업 등 광범위한 분야에서 사용하고 있다. 현재 대부분의 수소 생산은 천연가스, 오일, 석탄을 주 원료로 하고 있다. 하지만 이 과정에서 이산화탄소와 같은 환경 문제를 야기할 수 있는 가스 또한 같이 생성된다. 이에 따라 보다 친환경적인 방법인 물의 전기분해 방법을 이용해서 수소를 생산하려는 연구가 진행되고 있다. 물의 전기분해를 통해 수소를 생산하는 방식은 순도가 높은 수소를 생산할 수 있는 장점이 있으나 전력 소모가 많아 가격이 높다는 치명적인 단점 또한 존재한다. 따라서 많은 전력을 소모하지 않고 수소를 전기 분해할 수 있는 방안을 마련하기 위한 연구가 진행되고 있다.
◇ 스팀 개질법(steam reforming) 천연가스 수증기 개질은 수소 생산에서 가장 저렴한 방법이며, 세계 총 수소 생산의 거의 절반을 이 방법으로 제조하고 있다. 스팀을 온도 700∼1,100℃, 메탄과 혼합하여 촉매 반응기에서 압력 3∼25bar로 반응하며 생산성을 증가시키기 위해서 계속 새로운 방법을 개발하고 있다. 연간 수소 생산 100,000톤 규모의 큰 스팀 개질기 하나로 약 100만 대의 연료전지 자동차에 공급할 수 있다. 작은 규모의 수소 생산을 위한 수증기 개질기에는 재래식 소형 개질기와 연료전지를 위해서 특별히 제작한 개질기 두 가지 종류가 있다. 현재 연료전지를 위해 개발한 개질기는 간결하면서도 종전의 소형 개질기 보다 낮은 온도와 압력에서 작동한다. 천연가스 수증기 개질법은 매우 일반적으로 사용하는 방법이다. 많은 반응들은 시스템 상에서 존재하는 산소에 기인한 반응을 수반하지만 전체적인 화학적 변환은 일반적으로 다음과 같다. CH4 + H2O -> CO + 3H2 CH4 + 2H2O -> CO2 + 4H2 위 식들의 반응은 높은 흡열반응이다. 따라서 스팀 개질에서는 높은 온도에서 촉매를 첨가하여 반응을 촉진시킨다. 이 반응에서 보는 바와 같이 수소는 메탄과 물 모두에서 분리되어 생산되기 때문에 높은 수소 생산 수율이 가능하다. 하지만 수소 생성과 동시에 환경오염의 원인이 되는 일산화탄소, 이산화탄소의 발생이 수반된다.
◇ 물 전기분해법 물 전기분해방법은 전력소모가 많아 순도가 높은 수소를 소규모로 제조하고자 할 때 주로 이용된다. 전해액은 20% 정도의 수산화나트륨(NaOH)을 사용한다. 이 방법은 국내 일부 충전소에서 아직도 사용하고 있으며, 화학반응식은 음극에서 수소가, 양극에서는 산소가 2:1의 비율로 발생하여 제품화된다. 음극 : 2H2O + 2e- -> 2OH + H2 양극 : 2OH- -> H2O + 2e- + 0.5O2 전기분해법은 가장 오래된 수소제조방법으로 실용화된 기술이며, 값싼 수력발전이 이용되는 캐나다나 노르웨이 등을 제외하면 경제성이 없어 세계적으로 널리 이용되지 않고 있다. 그러나 소량이면서 높은 순도의 수소를 얻기 위한 분야에서는 효율 높은 전기분해수소 생산기술을 개발하기 위해 노력하고 있다. 알칼리 전기분해의 효율이 70% 내외이므로 효율을 높이는 기술로 고체 고분자 전해질 전기분해나 고온수증기 전기분해법에 대한 연구가 활발히 이루어지고 있다.
- 특허조사
◇ Hydrogen production from carbonaceous material
- 미국 특허 - 특허 번호: US6,790,430B1 - 특허 날짜: Sep.14,2004 - 양수인: The Regents of the University of California, Los Alamos, NM (US) - 요약: 수소는 2단계 공정을 통해 고체 또는 액체 탄소 함유 연료에서 생성된다. 연료는 수소화 반응에서 수소로 가스화 되어 메탄이 풍부한 기체 반응 생성물을 생성한 다음, 수소 생성 및 탄산화 반응에서 물 및 산화칼슘과 반응하여 수소 및 탄산칼슘을 생성한다. 탄산칼슘은 수소 생성 및 탄산화 반응 구역으로부터 연속적으로 제거, 연소되어 산화칼슘을 재생시키고, 이는 수소 생성 및 탄산화 반응 구역으로 재도입 될 수 있다. 수소 생성 및 탄산화 반응에서 생성된 수소는 연소 반응에 필요한 에너지를 제공하고 또한 가스화 반응에서 석탄의 수소화를 유지하기에 충분하다. 이와 같이 생성된 수소는 에너지 생산 또는 다른 목적으로 이용 가능하다.
◇ Perovskite oxide catalyst for oxygen evolution reactions
- 미국 특허 - 특허 번호: US2016/0348257A1 - 특허 날짜: Dec.1,2016 - 출원인: OSAKA PREFECTURE UNIVERSITY PUBLIC CORPORATION, Sakai-shi (JP); FUJI DIE CO., LTD., Tokyo (JP) - 요약: OER(Oxygen Evolution Reaction)을 위한 촉매는 RuO2 및 IrO2와 같은 보편적이고 비싼 귀금속 산화물 촉매보다 좋은 반응성과 긴 수명을 가지고 있다. OER 촉매로서 A-site ordered perovskite 산화물 촉매 (CaCu3Fe4O12 및 CaMn3Mn4O12 등)는 경제성이 우수하다. 이 촉매는 귀금속 산화물 촉매에 비해 촉매의 활성이 높으며, 산화 반응 조건에서도 매우 안정적이므로 사용 수명이 길다. 촉매로 인해 금속-공기 전지의 전하 반응, 직사광선에 의한 직접적인 물 분해 반응에서의 anode OER 등과 같은 중요한 에너지 변환 반응이 예상된다.
◇ Hydrogen production method by multi-step copper-chlorine thermochemical cycle
- PCT (국제 특허) - 특허 번호: WO 2013/054340 A3 - 특허 날짜: 18 April 2013 - 출원인: YADAV, Ganapati Dadasaheb [IN/IN]; Chemical Engineering Department, Institute of Chemical Technology, (Deemed University), Nathalal Parekh Marg, Matunga (East), Mumbai 400 019 (IN). - 요약: 본 발명은 구리 및 염소 화합물의 반응을 수반하는 저온, multi-step, closed, cyclic 구리-염소 (Cu-CI) 공정에 의해 물로부터 수소 및 산소를 열화학적으로 제조하는 방법을 개시한다. Cu-CI 열화학 사이클을 통한 수소 생산 방법은 4 개의 열 반응, 1 개의 전기 화학 반응 그리고 1 개의 단위 작동으로 구성된다. 사이클은 6 개의 단계를 포함한다: (1) 수소 생산 단계; (2) 구리 생산 단계; (3) 건조 단계; (4) 염화수소 생산 단계; (5) 분해 단계; (6) 산소 생산 단계. 연속적인 공정의 순 반응은 물을 수소와 산소로 분해하는 것이다. 염화구리 입자를 과열 증기와 접촉시키는 것을 포함하는 산화구리의 제조 방법과 산소의 생성은 열화학 구리-염소 (Cu-CI) 사이클에 의한 수소 생산의 일부로서 산화구리와 건조 염소와의 반응을 포함한다. 반응은 고온 및 대기압에서 fixed bed 유형으로서 flow through type quartz 반응기에서 수행된다.
◇ 수증기-이산화탄소 개질에 의한 합성가스 제조용 촉매 및 이를 이용한 합성가스 제조방법
- PCT (국제 특허) - 특허 번호: WO 2014/092474 A1 - 특허 날짜: 2014년 6월 19일 - 출원인: 한국가스공사 (KOREA GAS CORPORATION) [KR/KR]; 463-754 경기도 성남시 분당구 돌마로 171, Gyeonggi-do (KR) - 요약: 본 발명은 이산화탄소를 이용한 천연가스로부터 합성가스 제조용 촉매, 특히 수증기-이산화탄소 개질에 의한 합성가스 제조에 유용한 촉매에 관한 것으로, 본 발명에 따른 촉매는 1) 건식혼합을 이용하여 세륨으로 수식된 지르코니아 및 알루미나 담체를 제조하는 단계; 2) 니켈 및 마그네슘 산화물 분말을 각각 준비하는 단계; 및 3) 단계 1)의 담체 분말과 단계 2)의 금속 분말을 혼합하여 소성하는 단계를 포함하는 방법에 의해 제조된다. 본 발명에 따른 촉매를 사용하여 제조된 합성가스의 수소/일산화탄소의 비율이 2.0±0.2로 조절될 수 있어 합성석유화학제품 (왁스, 나프타, 디젤 등)을 생산하는데 효율적인 합성가스를 용이하게 제공할 수 있다.
- 특허 전략
◇ 기존 perovskite와 비교하여 산소를 다른 anion으로 치환한 촉매는 구조적 안정성은 비슷하나 수소 생성효율은 더 좋을 것으로 기대된다. ◇ 현재 Perovskite 촉매는 태양 전지 분야에 대해서만 주로 특허가 출원되고 있다. 하지만, perovskite를 이용하여 수소를 생산하는 방법은 아직 다양한 특허가 출원되지 않고 있다. 뿐만 아니라 산소를 다른 anion으로 치환한 perovskite를 연구이기 때문에 이 연구를 주제로 특허를 출원하면 독창적인 결과를 얻을 수 있을 것이다. ◇ 이 연구를 통해 얻은 계산 결과와 추후 실험을 통해 얻은 결과를 비교했을 때 그 경향성과 결과가 동일하다면 계산결과가 타당하다고 볼 수 있다. 따라서 일반적으로 특허를 실험 결과를 이용하여 출원하지만, 이번 연구에서 얻은 DFT 계산 결과를 포함하여 특허를 출원한다면 더 근거 있는 특허를 출원할 수 있을 것이라고 생각한다.
개발과제의 기대효과
기술적 기대효과
◇ 기존 perovskite와 귀금속 촉매 대비 좋은 촉매 성능을 가질 것으로 예상한다. ◇ 기존 촉매와 구조적 안정성 차이가 거의 없이 높은 수소 생산량을 가진다. ◇ 저온에서 기존 촉매보다 높은 효율을 보일 것이다.
경제적, 사회적 기대 및 파급효과
◇ 적은 에너지가 소모되어 더 경제적으로 수소 생산이 가능할 것이다. ◇ 전기분해를 이용하여 생산하기 때문에 화석연료를 사용하지 않아 친환경적이다. ◇ 추후 수소 생산 촉매 개발 연구에서 기초적인 데이터를 제공할 것이다.
기술개발 일정 및 추진체계
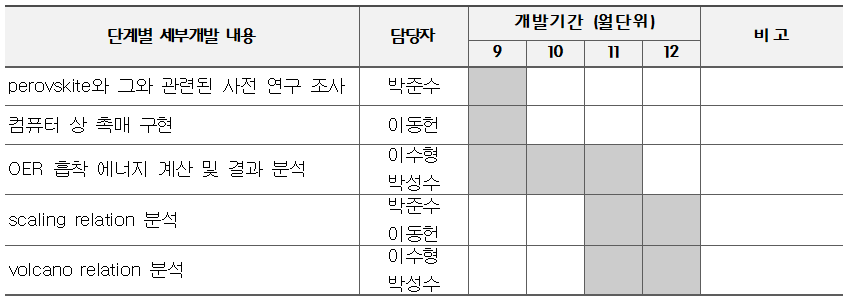
개발 일정
구성원 및 추진체계
◇ 박준수 : perovskite와 이와 관련된 사전 연구 조사 및 결과에 대한 scaling relation 분석 ◇ 이동헌 : 컴퓨터 상 촉매 구현 및 결과에 대한 scaling relation 분석 ◇ 이수형 : OER 흡착 에너지 계산과 결과 분석 및 volcano relation 분석 ◇ 박성수 : OER 흡착 에너지 계산과 결과 분석 및 volcano relation 분석
설계
설계사양
제품의 요구사항
● 물의 전기분해 반응에 있어 다양한 perovskite 촉매의 overpotential 계산하여 가장 반응에 유리한 촉매를 계산
● 반응에 유리한 촉매에 대하여 O를 제거 또는 C, N, F, Cl로 치환하여 촉매의 overpotential 변화 경향성 및 더 유리한 촉매를 개발
설계 사양
● VASP 프로그램을 이용하여 다양한 perovskite(LaNiO3, LaCoO3, LaCrO3, LaCuO3, LaMnO3, LaVO3, SrNiO3, SrCoO3, SrCrO3, SrCuO3, SrMnO3, SrVO3)에 대하여 안정한 표면의 에너지와 물의 전기 분해 반응의 각 단계의 ΔG를 계산
개념설계안
● 계산 결과를 이용하여 각 단계에 대한 ΔG 그래프를 그려 scaling relation을 확인하고, volcano plot을 통해 반응에 가장 유리한 촉매를 확인
● 반응에 가장 유리한 촉매들에 대해 1개 또는 2개의 O를 제거 또는 C, N, F, Cl로 치환하여 volcano plot 상에서의 위치 변화를 파악하며 경향성 확인하고 각 촉매가 반응이 유리해지는 방법을 조사
이론적 계산 및 시뮬레이션
● A-알칼리토금속으로 Sr, La를 사용하고 B-전이금속으로 NI, Co, Cu, Cr, Mn, V을 사용하여 기본 페로브스카이트 촉매 구현
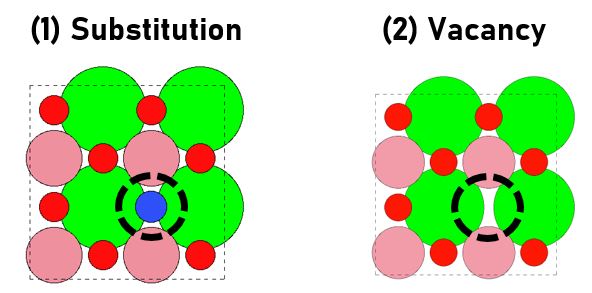
- 촉매 표면에 존재하는 산소를 C, N, Cl, F로 치환하거나 Vacancy 상태로 디자인
- 시뮬레이션 VASP 프로그램을 이용하여 디자인 한 촉매를 구현하고 흡착에너지를 계산
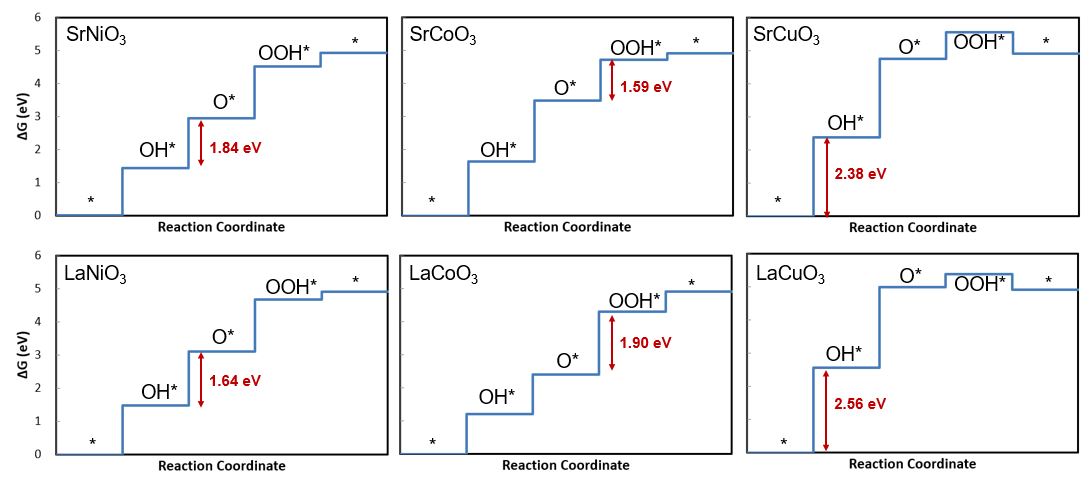
● OER 반응의 각 스텝에 대한 반응에너지를 계산하고 기본 촉매에 대한 에너지 다이어그램 도출
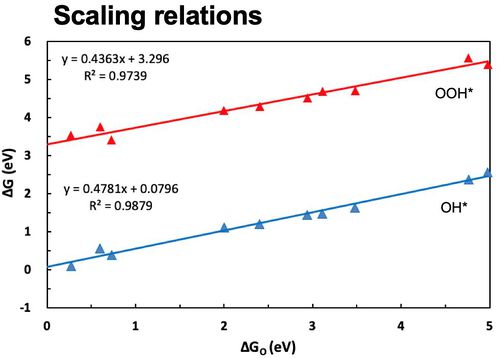
● O*vsOH*와 O*vsOOH*의 scaling relation을 확인한 결과 선형관계가 있는 것을 확인했다.
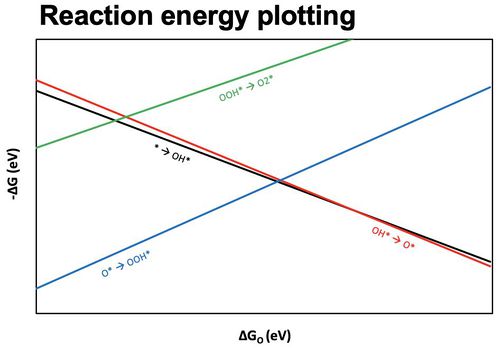
● 각 반응 과정의 반응에너지를 plotting하면 아래와 같은 그래프를 얻을 수 있다.
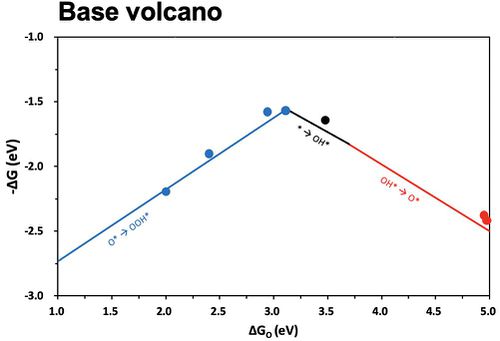
● 높은 ∆G 값을 가지는 단계가 반응 속도 결정단계이므로 이를 이용하여, volcano plot을 만들 수 있다.
● 수소 생산의 이상적인 포텐셜 값인 1.23eV와 유사한 값을 가지는 촉매 선택
상세설계 내용
● 계산한 데이터를 정리하여 volcano plot 도출하고 촉매의 경향성 파악
- 오버포텐셜이 작은 촉매들에 대해 산소를 C, N, Cl, F, Vacancy로 바꾸어 계산 - 여러 반응들 중에 가 낮은 반응 결정 단계만 모아 volcano plot을 그린 후 top으로 이동시킬 수 있는 방법에 대해 고찰
결과 및 평가
완료 작품의 소개
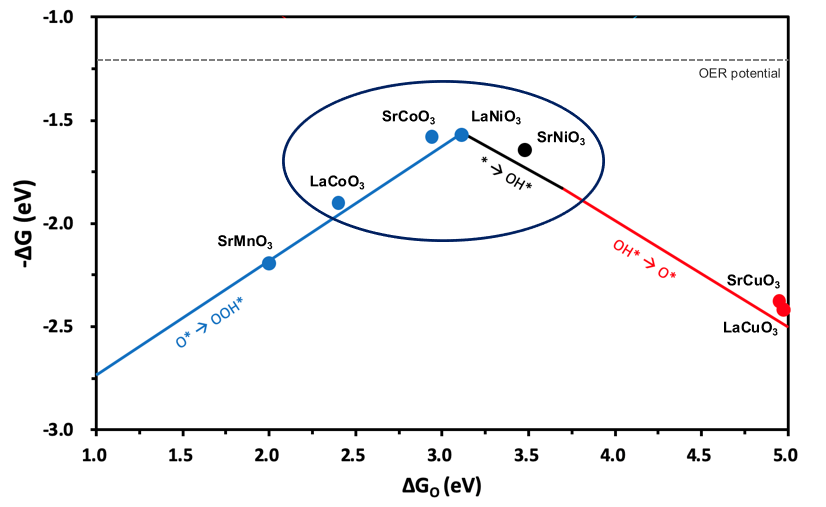
Volcano top 근처에 있는 촉매 4개에 대하여 산소 치환 및 제거 계산을 진행했고, 결과에 대한 경향성을 분석했다.
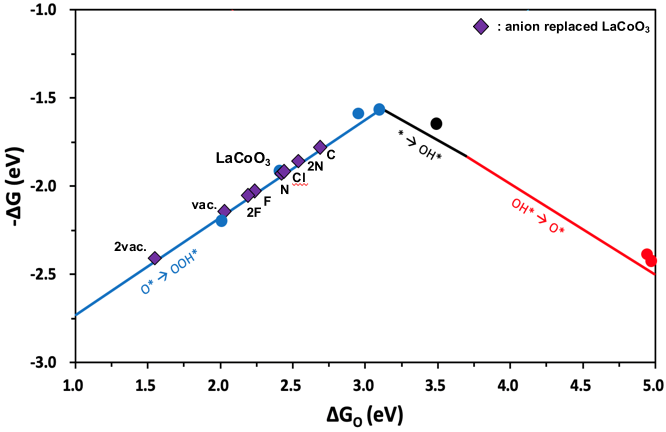
1. LaCoO3
산소를 F로 치환하거나 제거할 경우 산소 흡착에너지가 낮아져 volcano plot 상에서 왼쪽으로 이동하고, Cl, N, C로 치환할 경우 산소 흡착에너지가 높아져 오른쪽으로 이동하는 것을 확인할 수 있다. 각 원소별로 치환의 개수가 늘어날 수록 흡착에너지가 더 많이 변하는 것 또한 확인할 수 있다. LaCoO3의 경우 O를 C로 치환할 경우 volcano top에 가장 근접하므로, 이 경우가 OER 반응에 있어 가장 좋은 촉매다.
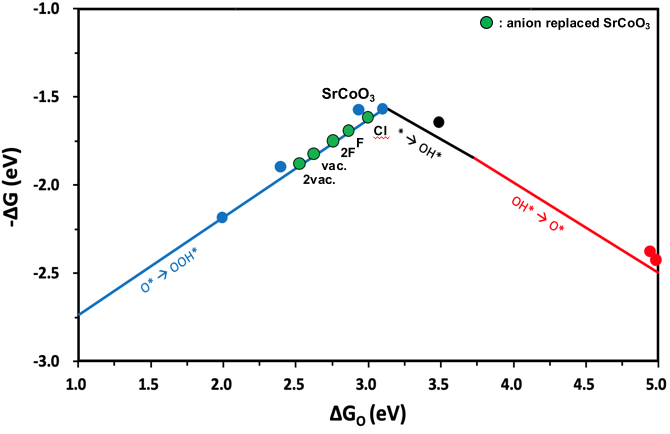
2. SrCoO3
마찬가지로 F와 vacancy는 왼쪽으로, Cl에 대해서는 오른쪽으로 이동했다. 이 경우에는 Cl로 치환한 경우가 가장 좋은 촉매임을 알 수 있으며, C, N으로 치환한 경우에는 촉매가 구조적으로 매우 불안정해져 고려 대상에서 제외했다.
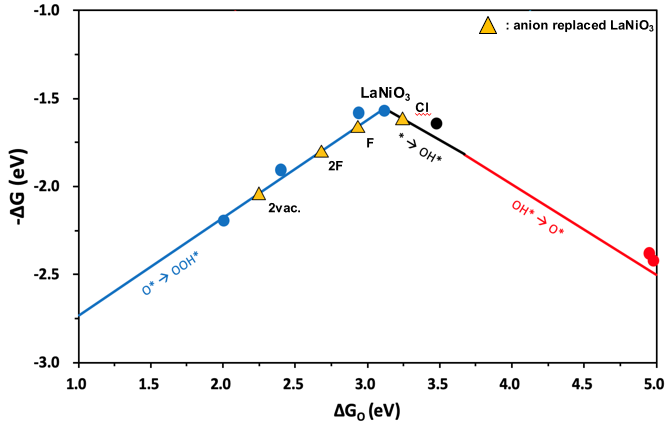
3. LaNiO3
LaNiO3의 경우, 치환을 하지 않은 경우에 이미 volcano top에 근접해있으나, 경향성을 확인하기 위해 위와 같은 방법으로 치환 계산을 진행했다. 이전 결과와 동일하게 F로 치환하거나 제거한 경우 volcano 상에서 왼쪽으로 이동하고, Cl의 경우 오른쪽으로 이동한다. 또한 LaNiO3의 경우, vacancy가 1개일 때는 구조적으로 불안정했으나, 2개일 때는 대칭 구조를 이루어 오히려 구조적으로 안정해졌으며, C, N의 경우는 이전 촉매와 같은 이유로 고려 대상에서 제외했다.
4. SrNiO3
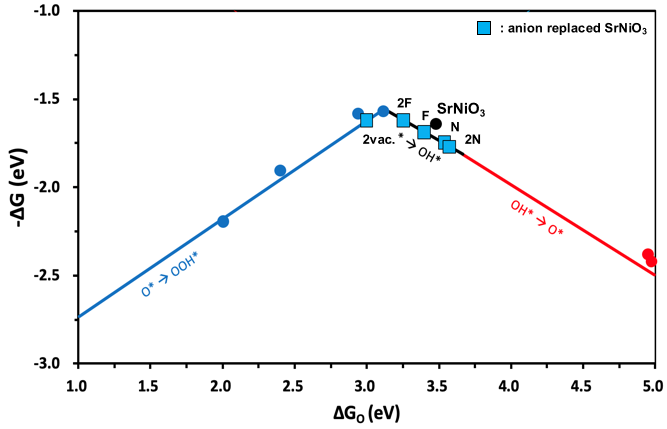
SrNiO3는 이전의 촉매들과는 다르게 volcano top 기준 오른쪽에 위치한다. 변화 경향성은 똑같이 F, vacancy에 대해서는 왼쪽으로, N으로 치환한 경우에는 오른쪽으로 이동했다. 따라서 이 촉매는 O를 F로 치환하거나 제외하는 방법이 OER 반응에 더 유리하게 작용한다.
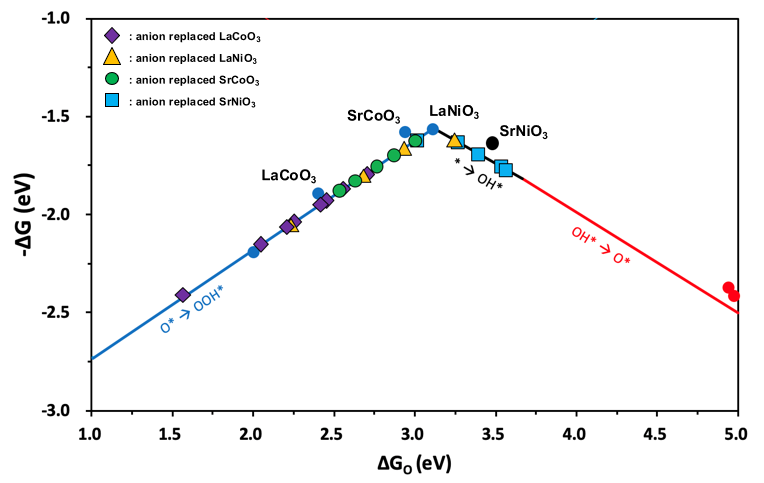
위 4가지 그래프를 하나의 그래프에 나타내면 다음과 같다.
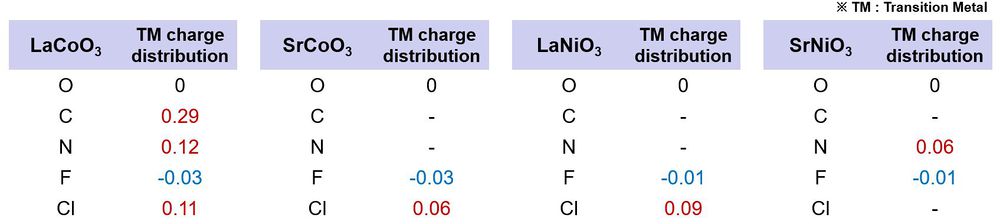
Charge distribution
Bader charge analysis를 통해 활성사이트의 전자 변화를 계산했다. 계산결과 F로 치환한 촉매는 활성사이트의 전자 밀도가 감소하였고, C, N, Cl로 치환한 촉매의 경우 활성사이트의 전자 밀도가 증가하였다. F의 경우, 전기음성도가 산소보다 크기 때문에 활성사이트의 전자 밀도가 감소한 것이고, C, N, Cl의 경우 전기음성도가 산소보다 작기 때문에 활성사이트의 전자 밀도가 증가했다. 따라서, 활성사이트의 전자 밀도 변화에 따라, 흡착에너지 변화 경향성을 파악할 수 있는데, 전자 밀도 감소 시 흡착에너지가 감소했고, 전자 밀도 증가 시 흡착에너지가 증가했다.
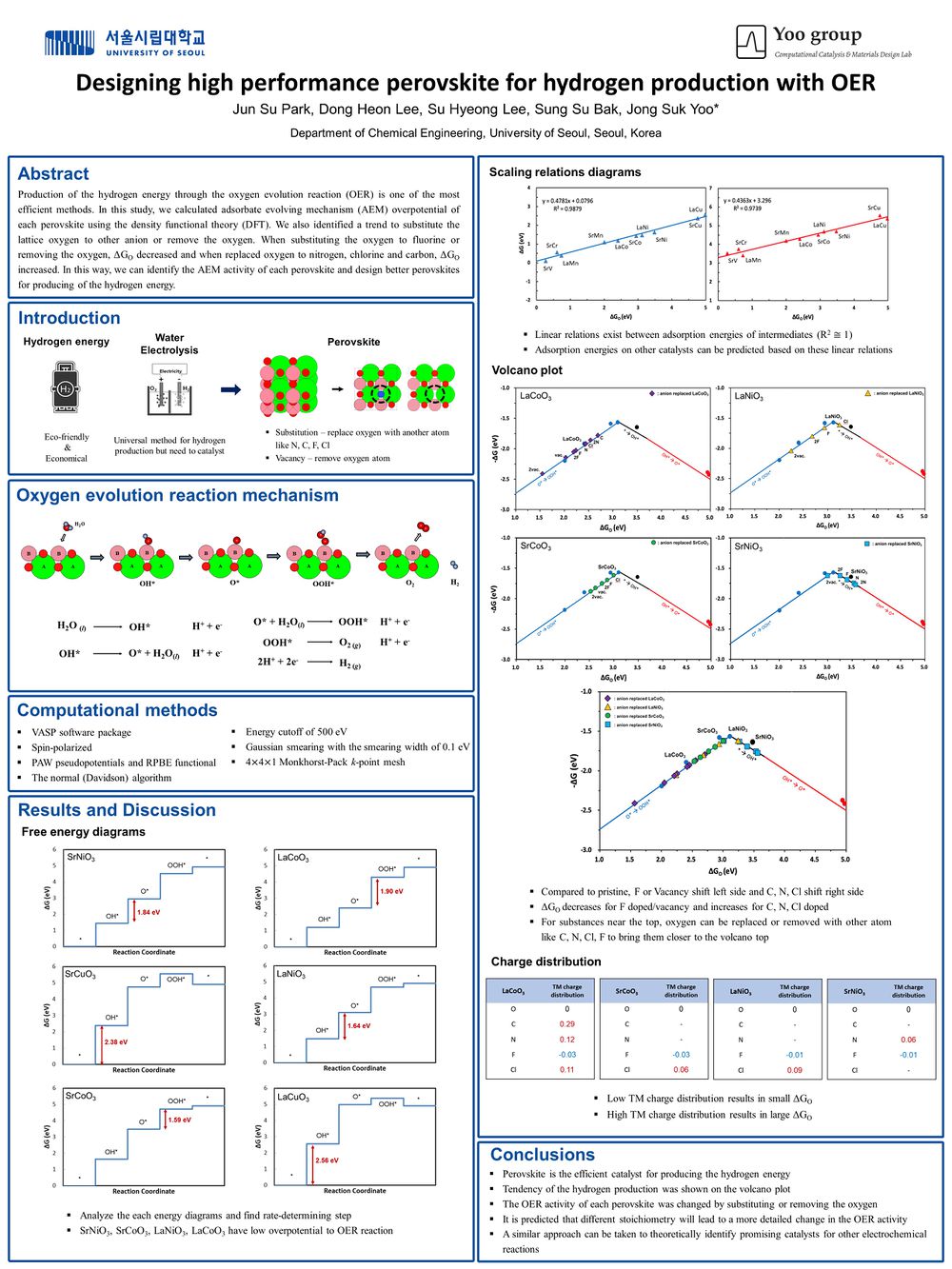
포스터
완료작품의 평가
Perovskite 촉매의 산소 치환으로 인해 촉매 수소 생산 성능을 향상시킬 수 있었다.
1. LaCoO3의 경우 C로 치환한 것이 가장 좋은 성능을 가진다.
2. SrCoO3의 경우 Cl로 치환한 것이 가장 좋은 성능을 가진다.
3. LaNiO3의 경우 치환하지 않은 것이 가장 좋은 성능을 가진다.
4. SrNiO3의 경우 F나 vacancy에서 좋은 성능을 가진다.
F로 치환하거나 vacancy를 만들었을때는, 활성사이트의 전자 감소로 인해 O* 흡착에너지가 감소하였고, C, N ,Cl으로 치환했을때는 활성사이트의 전자가 증가하여 O* 흡착에너지가 증가하였다.
따라서, volcano peak 왼쪽에 촉매가 위치해 있을 때는 흡착에너지를 증가시키는 C, N, Cl로 치환을 하고, volcano peak 오른쪽에 존재할 때는 F로 치환하거나, 산소 vacancy를 만들면 수소 생산에 더 효율이 좋은 촉매를 만들 수 있다.
향후계획
1. 치환한 anion의 종류를 다양화하여 연구를 진행해야 한다.
2. 실제 실험연구를 통해 촉매의 성능을 확인해봐야한다.