"윤진환 교수님 1팀"의 두 판 사이의 차이
Uosche25211 (토론 | 기여) (→H-ZSM5 제조) |
Uosche25211 (토론 | 기여) (→실험 방법) |
||
| 244번째 줄: | 244번째 줄: | ||
''' ''' ii. 자연 냉각, 공기 소성 | ''' ''' ii. 자연 냉각, 공기 소성 | ||
| + | |||
| + | *이온교환법 | ||
| + | 지지체: ZSM-5 H형 10 g | ||
| + | 용액: 금속 질산염 HNO₃ (69–70% ACS reagent ≥98%), 초순수 18.2 MΩ·cm | ||
| + | 장비: 항온교반(70°C), 부흐너여과, 전도도계, 110°C 오븐, 머플퍼니스(공기), H₂/N₂ 환원로 | ||
| + | L/S: 15–20 mL·g⁻¹ → 10 g당 150–200 mL/회 | ||
| + | pH: 3.8–4.5 유지(0.1 M HNO₃로 미세 조절) | ||
| + | 세척 기준: 여액 전도도 ≤ 20 µS·cm⁻¹ | ||
| + | |||
| + | |||
| + | |||
| + | --- stock 용액 --- | ||
| + | Fe–ZSM-5: 0.10 M Fe(NO₃)₃·9H₂O 250 mL, 필요 염 0.10×0.25×404.00 = 10.10 g | ||
| + | Ni–ZSM-5: 0.10 M Ni(NO₃)₂·6H₂O 250 mL, 필요 염 0.10×0.25×290.79 = 7.27 g | ||
| + | Co–ZSM-5: 0.10 M Co(NO₃)₂·6H₂O 250 mL 필요 염 0.10×0.25×291.03 = 7.28 g` | ||
| + | 1. 교환용 stock 용액 제조 | ||
| + | ①. 메스플라스크(250 mL)에 초순수 ~150mL → 해당 염 완전 용해 → 초순수로 250 mL 정용 pH 확인 후 필요 시 0.1 M HNO₃ 로 3.8–4.5로 맞춤 | ||
| + | (탁해지면 pH↓) | ||
| + | ②. pH 확인 후 필요 시 0.1 M HNO₃ 로 3.8–4.5로 맞춤 | ||
| + | (탁해지면 pH↓). | ||
| + | * Fe(NO₃)₃·9H₂O: ~0.72 g, Ni(NO₃)₂·6H₂O: ~0.50 g, Co(NO₃)₂·6H₂O: ~0.49 g | ||
| + | 수준이지만, 교환 평형을 밀기 위해 용액은 과량 제공해야함. | ||
| + | --- 이온 교환법 실험 --- | ||
| + | 1. 1차 이온교환 | ||
| + | ①. 500 mL 비커에 stock 용액 150–200 mL + ZSM-5 10 g . | ||
| + | ②. 70 °C, 600 rpm, 5h 교반. 증발 시 초순수로 부피 유지. | ||
| + | pH 3.8–4.5 유지. | ||
| + | ③. 부흐너 여과 → 초순수 200–300mL로 세척 반복(여액 전도도 ≤ 20 µS·cm⁻¹). | ||
| + | |||
| + | 2. 2차 이온교환 | ||
| + | ①. 동일 조건으로 stock 용액 150–200 mL 재사용 → 70 °C,5h→ 여과·세척. | ||
| + | ②. 목표 로딩이 낮게 나오면 3차까지 반복 가능. | ||
| + | |||
| + | 3. 건조 | ||
| + | ①. 110 °C, 12h 건조. | ||
| + | 4. 소성(질산염 분해, 산점 안정화) | ||
| + | ①. 2°C·min⁻¹ 승온 → 500–550°C, 4–6 h, 공기(NOₓ 배출, 후드 필수) | ||
| + | 5. 활성화(필요 시) | ||
| + | ①. 금속 환원상 필요하면: | ||
| + | N₂ 퍼지 30 min → 5–10% H₂/N₂, 1–2 °C·min⁻¹ → 400°C, 2h → N₂ 냉각 | ||
==결과 및 평가== | ==결과 및 평가== | ||
2025년 12월 2일 (화) 20:31 판
프로젝트 개요
기술개발 과제
국문 : 제올라이트 기반 전이금속 촉매를 이용한 폐플라스틱 열분해 및 방향족 자원 회수 연구
영문 : Catalytic Pyrolysis of Waste Plastics Using Zeolite-Based Transition Metal Catalysts for Aromatic Resource Recovery
과제 팀명
윤진환 교수님 1팀
지도교수
윤진환 교수님
개발기간
2025년 9월 ~ 2025년 12월 (총 4개월)
구성원 소개
서울시립대학교 화학공학과 2019340033 유인혁(팀장)
서울시립대학교 화학공학과 2019340006 김도완
서울시립대학교 화학공학과 2019340015 김태정
서론
개발 과제의 개요
개발 과제 요약
◇ 제올라이트 금속 도핑 및 열분해 매커니즘을 이해하고 폐플라스틱 재활용 공정을 재현한다.
◇ 제올라이트에 금속을 도핑시켜 열분해에 최적화된 촉매를 제작 및 분석한다.
◇ 전이금속 제올라이트를 이용한 폐플라스틱 열분해 과정을 재현하고 방향족 화합물의 수득률을 계산한다.
◇ 이전 학기에서 진행했던 선행연구에서의 수득률을 비교 및 타당성을 검증한다.
개발 과제의 배경
현대 사회에서는 편리함과 위생을 이유로 일회용 플라스틱 제품의 사용이 폭발적으로 증가하고 있으며 그로 인해 폐플라스틱의 배출량 또한 지속적으로 급증하고 있다. 이러한 추세는 도시 및 산업 폐기물 관리 체계에 과도한 부담을 주고 있으며 기존의 소각 또는 매립 방식으로 처리되는 폐플라스틱은 환경에 심각한 악영향을 끼치고 있다.
폐플라스틱의 소각 과정에서 일산화탄소(CO), 이산화황(SO₂), 이산화탄소(CO₂ ) 및 온실가스 등과 같은 유독 가스가 대량으로 방출되어 대기오염은 물론 기후변화에까지 부정적인 영향을 미치며 매립된 플라스틱은 수십 년 이상 분해되지 않고 토양 및 지하수 오염을 유발시키고 있다.
금속 도핑 제올라이트 기반 촉매 시스템은 폐플라스틱의 효율적 자원화와 환경 부하 저감이라는 두 가지 과제를 동시에 해결할 수 있는 유망한 기술적 해법으로 지속가능한 폐기물 처리 및 순환 경제 구축에 기여할 수 있을 것으로 기대된다.
촉매 설계를 통해 유해가스 발생 최소화 및 자원 회수율 증대가 가능하므로, 탄소중립 및 폐기물 관리와 관련된 정책적 의사결정의 과학적 근거로 활용될 수 있다.
개발 과제의 목표 및 내용
◇ 폐플라스틱 재활용 공정시 필요한 제올라이트의 금속 도핑 방법과 열분해 매커니즘을 이해하고 실험을 설계 및 진행한다.
◇ 제올라이트에 금속을 도핑시키고 XRD, XPS 분석기기를 이용해 도핑 농도를 파악한다.
◇ 도핑시킨 제올라이트를 이용해 열분해 실험을 진행하고 GC-FID와 FT-IR을 이용해 방향족 화학물질의 수득률을 파악한다.
◇ 이전학기에 진행했던 선행연구에 대한 실험적 비교를 통해 방향족 화학물질 수득률의 경향성을 파악한다.
관련 기술의 현황
관련 기술의 현황 및 분석(State of art)
- 전 세계적인 기술현황
◇ 최근 연구를 폐플라스틱 열분해 시에 사용되는 촉매의 성능을 평가하는 연구가 진행되고 있다. 최근 연구를 보면 함침법을 통하여 전이 금속을 도핑시킨 후 실제 플라스틱 폐기물을 열분해하는 실험을 통해 촉매의 성능을 판단하는 지표를 설정하였다. 위 선행연구에서는 Acidity/SBET 비율이 제올라이트계 촉매의 성능을 평가하는 핵심 기술 지표로 주목하고 있다. (촉매의 산점 밀도(Acidity)와 비표면적(Specific Surface Area, SBET))
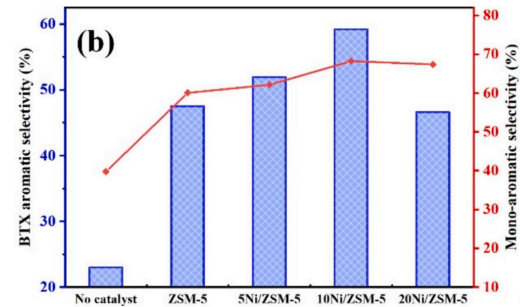
◇ Zhang et al. Fuel, 2024는 고체 열 운반체를 갖춘 회전식 반응기 내 Ni/ZSM-5 촉매 기반 폴리에틸렌(PE) 현장 촉매 열분해를 제시하며 금속 니켈 담지량 및 촉매-대-PE 질량비가 열분해 오일의 BTX 방향족 선택도와 수소 분율에 미치는 영향을 분석했다. 이 연구는 금속 니켈 담지량이 10 wt%일 때 열분해 오일 내 BTX 방향족 농도가 향상되었고, 20Ni/ZSM-5 촉매 사용 시 수소 가스 분율이 증가했다. 또한 그 원인이 니켈 금속이 C–C 및 C–H 결합을 분해하는 데 탁월한 능력을 가지기 때문임을 입증했다. 또한 촉매-대-PE 질량비를 0.5에서 2로 변화시켰을 때 열분해 오일 내 단일고리 방향족 화합물의 농도가 증가했음을 확인했다. 그러나 촉매 비활성화의 주요 원인인 코크 침적(coke deposition)의 양이 니켈 담지량 증가에 따라 증가했음을 보고하면서도, 코크 침적의 발생을 정량적으로 제어하고 촉매 재생 후 장기적인 내구성을 확보하기 위한 구체적인 운용 전략에 대해서는 구체적으로 다루지 않았다.
◇ Koti et al. ACS Omega, 2025는 매립지 폐플라스틱의 촉매 열분해를 제시하며 응답 표면 방법론(RSM-CCD)을 통해 온도와 촉매 담지량의 최적 조건을 조사했다. 이 연구는 세척 과정을 거친 폐플라스틱이 오일 수율을 높이는 데 효과적임을 확인하고, 최적 조건에서 세척된 폐기물이 가장 높은 오일 수율과 높은 HHV를 달성했음을 분석했다. 특히, 5 wt% Co/HZSM-5 촉매가 높은 가솔린 수율을 보이는 등 고품질 탄화수소 화합물 분포를 보였음을 확인했다. 그러나 최적 조건에서 생산된 산성의 열분해 오일을 상업적 연료로 직접 활용하기 위해 필요한 후처리 또는 산성도 저감 방안에 대해서는 구체적으로 다루지 않았다.
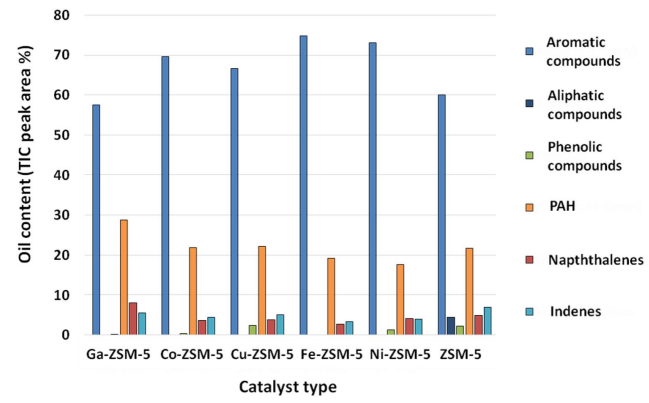
◇ Dyer et al. Journal of Material Cycles and Waste Management, 2022는 폐 바이오매스와 폴리스티렌의 동시 열분해을 제시하며 Ga, Co, Cu, Fe, Ni 변형 ZSM-5 촉매를 사용하여 액체 연료 및 방향족 화학물질 생산에 미치는 영향을 분석했다. 이 연구는 Ni–ZSM-5와 Co–ZSM-5가 탈카르복실화 및 탈카르보닐화를 통해 산소를 주로 제거하는 반면 ZSM-5, Ga–ZSM-5, Cu–ZSM-5, Fe–ZSM-5 촉매는 수소화 탈산소화를 통해 산소를 제거한다는 메커니즘의 차이를 규명했다. 또한 Co–ZSM-5, Cu–ZSM-5, Fe–ZSM-5, Ni–ZSM-5 촉매는 미변성 ZSM-5에 비해 단일고리 방향족 화합물의 수율을 증가시켰다. 그러나 금속 담지 후 촉매의 표면적 및 기공 부피가 감소했음을 보고하면서도, 이것이 촉매 활성점 접근성 및 촉매 수명에 미치는 구체적인 영향이나 사용된 촉매의 코크 침적량 정량 분석에 대해서는 구체적으로 다루지 않았다.
◇ Waziri et al. Applied Petrochemical Research, 2019는 저밀도 폴리에틸렌(LDPE) 열분해 기체 생성물의 촉매 개질(reforming)을 제시하며 Fe-ZSM-5 촉매의 온도 및 담지량이 액체 연료 품질에 미치는 영향을 분석했다. 이 연구는 촉매 개질이 액체 분획의 방향족 함량을 크게 증가시키고 지방족 함량을 감소시킴을 FTIR 결과로 확인했으며, 최적 조건에서 응축액의 방향족 탄화수소 조성이 상대적으로 약 70%까지 증가하고 주 생성물이 p-자일렌임을 GC/MS 분석을 통해 입증했다. 그러나 촉매의 고온 적용은 비응축성 가스 수율을 높이는 결과를 가져왔으며, 촉매 비활성화의 주요 원인이 되는 사용된 촉매의 코크 침적 및 비활성화 정도에 대한 특성화 결과나 촉매 재생 후 재사용 가능성에 대해서는 구체적으로 다루지 않았다.
- 특허조사
◇ 고급 경질유 생산을 위한 제올라이트 촉매: 한국 에너지 기술 연구원에서 폐플라스틱 열분해로 생성된 왁스 오일을 제올라이트계 촉매 존재 하에서 열분해하여 나프타나 경질 올레핀과 같은 고급 탄화수소로 전환하는 방법에 대한 특허를 출원하였다.
◇ 특정 Si/Al 비율의 제올라이트: 한국화학연구원에서 폐플라스틱 열분해유로부터 경질 올레핀 수율을 높이기 위해 Si/Al 몰 비율이 50~1000을 만족하는 제올라이트 촉매를 이용하는 방법이 특허로 제시되었다.
◇ 금속이 함침된 제올라이트 촉매: Johnson Matthey Plc 사에서 금속이 함침된 제올라이트 촉매를 이용한 폐플라스틱 분해 특성에 대한 연구 및 관련 특허로 제시하였다.
◇ 순환 유동층 반응기 및 제올라이트 촉매 시스템: 한국화학연구원에서는 제올라이트 성형체 촉매와 순환 유동층 반응기를 결합하여, 기존 나프타 분해 공정보다 낮은 온도에서 폐플라스틱을 효율적으로 분해하고 촉매를 연속적으로 재생할 수 있는 파일럿 규모의 기술을 개발하였다.
◇ 개질 제올라이트 촉매를 이용한 혼합 폐플라스틱 처리 기술: 한국 폐기물 자원 순환 학회에서 할로겐화 폴리비닐(PVC 등)이나 또는 산성 플라스틱이 포함되어 있는 혼합 폐플라스틱을 처리하기 위하여, 개질된 제올라이트 촉매를 사용하여 고부가의 탄화수소 유체 연료로 전환하는 기술을 개발하였다.
- 특허전략
◇ 기존에 연구한 머신러닝 기반의 예측 모델을 실험을 통해 실증한다.
◇ 기존에 연구한 머신러닝 모델의 예측값과 실제 수율을 정량적으로 비교한다. 이를 통해 촉매 수명, 실험 규모 등을 학습시켜 지속가능성, 경제성에 대한 이점을 가져갈 수 있다.
개발과제의 기대효과
기술적 기대효과
◇ 금속 도핑 제올라이트 기반 촉매 시스템은 폐플라스틱의 효율적 자원화와 환경 부하 저감이라는 두 가지 과제를 동시에 해결할 수 있는 유망한 기술적 해법으 로 지속가능한 폐기물 처리 및 순환 경제 구축에 기여할 수 있을 것으로 기대된다.
◇ 다양한 촉매 조합 및 반응 조건에서의 방향족 생산성을 사전에 예측할 수 있어 반응 최적화 실험을 최소화하고 개발 시간을 단축시킬 수 있다. 이 과정에서 화학적 재활용 공정의 고도화 기반을 마련할 수 있다.
경제적, 사회적 기대 및 파급효과
◇ 촉매 설계를 통해 유해가스 발생 최소화 및 자원 회수율 증대가 가능하므로, 탄소중립 및 폐기물 관리와 관련된 정책적 의사결정의 과학적 근거로 활용될 수 있다.
◇ 여러 금속 종류, 흡착위치, 활성도 등 여러 조건에 대한 변수들을 분석하고 정량화하였기 때문에 다양한 플라스틱 종류 및 열분해 조건에 맞는 최적화된 촉매를 설계하는 것이 가능하다. 이를 통하여 각 상황에 맞는 촉매를 설계하는 플랫폼을 구축할 수 있다.
기술개발 일정 및 추진체계
구성원 및 추진체계
◇ 김도완, 김태정, 유인혁 : 도핑 및 열분해 실험 설계
◇ 김도완, 김태정, 유인혁 : 도핑 실험 및 분석
◇ 김도완, 김태정, 유인혁 : 열분해 실험 및 분석
◇ 김도완, 김태정, 유인혁 : 선행연구와 비교
이론 및 실험 설계
이론
열분해 메커니즘
- Radical mechanism
1. 고분자 사슬 끊기 (열분해 시작) : 플라스틱은 긴 탄소 사슬(고분자)로 이루어져 있다. 산소 없이 300~500도 정도로 가열하면, 이 긴 탄소 사슬 중간중간에 있는 결합이 뜨거운 열 때문에 끊어지기 시작하는데 이것을 열분해라고 한다.
2. 자유 라디칼 생성 : 결합이 끊어질 때, 전자를 하나씩 나눠 가지면서 '자유 라디칼'이라는 불안정한 조각들이 생긴다. 이 라디칼들은 다른 분자와 반응하려는 경향이 있어 활발하게 움직인다.
3. 사슬 반응 (성장 및 끊김) : 생성된 라디칼들이 다른 플라스틱 사슬을 공격해서 또 다른 라디칼을 만들고, 자신은 안정화되거나 더 작은 조각으로 변함. 이러한 과정이 계속 반복되면서 원래의 긴 고분자 사슬이 점점 더 짧은 조각들로 변화한다. 이것을 라디칼 연쇄 반응이라고 한다.
4. 왁스 생성 : 열분해 과정에서 온도가 너무 높지 않거나, 특정 촉매를 사용하지 않으면 사슬이 완전히 짧게 끊어지지 않고 적당히 긴 상태로 남는다. 적당히 긴 탄화수소 사슬들 (보통 탄소 원자가 20개 이상 연결된 것들) 이 상온에서 고체나 반고체 형태로 뭉쳐지는 것을 왁스라고 한다.
- Carbenium ion mechanism
촉매를 쓰면 길이가 짧은 탄화수소 사슬이 나오게 되는데 그 이유는 촉매가 열분해과정을 다르게 이끌기 때문이다.
1.촉매의 산성자리: X(촉매의 산성 자리)가 플라스틱 고분자 사슬에 있는 단일 결합(C-C)을 공격해서 끊는 역할을 한다.
2. 카르베늄 이온 생성: 촉매 표면에서 C-C 결합이 끊어질 때, '카르베늄 이온'이라는 불안정한 중간체가 생기기 쉽다. (자유 라디칼 메커니즘도 있지만, 산성 촉매에서는 이온 메커니즘이 중요하다.)
(카르베늄 이온 : 탄소 원자가 양전하(+)를 띠고 있는 불안정한 이온)
3. 베타-깨짐 (Beta-scission): 카르베늄 이온은 안정화되기 위해 자기로부터 2개 탄소 떨어진 곳의 C-C 결합을 또 끊어버리는 반응을 잘 발생시키는데 이것을 '베타-깨짐'이라고 한다. 이 과정에서 이중 결합(C=C)을 가진 올레핀이 만들어져 나오게 되고 동시에 새로운 카르베늄 이온이 또 생겨서 반응이 계속 이어진다.
4. 짧은 사슬 선호: 촉매의 구조적인 특성(특히 제올라이트의 미세한 구멍 구조)과 산성 자리의 성질 때문에, 촉매는 긴 사슬보다는 짧은 탄소 사슬, 특히 에틸렌이나 프로필렌 같은 '가벼운' 올레핀을 만드는 데 더 유리하게 반응을 유도하는 경향을 가진다.
촉매는 플라스틱 고분자 사슬을 효과적으로 쪼개는데 이 쪼개는 과정이 그냥 열만 가했을 때랑 달라서 이중 결합을 포함하는 짧은 탄소 사슬들이 많이 생기게 만든다.
- Carbenium ion 생성 과정
1. 산성 촉매의 도움: 산성 촉매의 산성 자리가 플라스틱 사슬의 C-C 결합을 공격해서, 한쪽 탄소가 전자를 덜 가져가면서 양전하를 띠고 떨어져 나오는 경우에 카르베늄 이온이 생길 수 있음
2. 다른 분자로부터 수소 이온(H+)을 떼어내면서: 탄화수소 분자에서 수소 이온(H+)이 떨어져 나가면서 옆에 있던 탄소가 양전하를 띠게 되어도 카르베늄 이온이 만들어질 수 있음
- Carbenium ion 특징
1. 매우 불안정함: 전자가 부족해서 주변의 전자나 음전하를 띤 물질과 바로 반응하는 경향.
2. 재배열 (Rearrangement): 더 안정적인 형태의 카르베늄 이온으로 스스로 구조를 바꾸는 '재배열' 반응을 잘 일으킴. 이 재배열 때문에 최종 생성물이 다양하게 나올 수 있음.
3. 반응성이 높음: 다른 분자들과 빠르게 반응해서 새로운 결합을 만들거나 기존 결합을 끊는 역할
제올라이트 ZSM5
- 촉매 사용 이유
만약 온도를 더 높이거나 특정 촉매를 쓰면, 이 적당히 긴 사슬들이 더 짧게 끊어져서 가벼운 기름(연료유)이나 가스 형태로 변화한다. 어떤 조건을 쓰냐에 따라 최종적으로 나오는 물질(가스, 기름, 왁스, 숯)의 비율이 바뀐다.
결국 폐플라스틱 왁스 열분해 메커니즘은 플라스틱 고분자 사슬이 열에 의해 끊어지고, 이 과정에서 생성된 다양한 길이의 탄화수소 조각들 중에서 적당히 긴 조각들이 뭉쳐 왁스 형태가 되는 과정이다. 여기서 만들어진 왁스는 접착제, 코팅제, 광택제, 잉크, 양초, 윤활제 등으로 사용된다.
열분해 시 촉매를 이용하면 더 짧은 탄화수소 사슬을 얻을 수 있으며 기름 형태의 물질(디젤, 가솔린), 가스형태의 물질(메탄, 에탄) 및 방향족 물질의 수율이 높아진다. 특히 불포화 탄화수소인 올레핀 이 많이 생성되는데 이때 촉매가 열분해로 생긴 올레핀이나 파라핀 계열의 고리화 혹은 탈수소화를 진행하여 방향족으로 전환시킨다. (탄소 원자들 사이에 적어도 하나 이상의 이중 결합(C=C)을 가지고 있는 것들로 왁스나 일반적인 기름처럼 탄소-탄소 사이에 단일 결합(C-C)만 있는 것들(포화 탄화수소)과는 구조가 좀 다르다.)
- 제올라이트(Zeolite)
제올라이트는 결정성 알루미노실리케이트로, 내부에 균일한 크기의 기공을 가진 산성촉매이다. 제올라이트 촉매는 산 촉매로 작용하여 시작단계의 C-C 결합 분해에 효과적이고, 결합에너지가 높다는 점 때문에 높은 열적 안정성을 가지고, 또 ZSM-5, Y형 등 다양한 형태를 가진다. 미세한 기공이 존재하는 특유의 구조와 그 구조가 단단하기 때문에 원하는 분자만 반응시킬 수 있는 형태 선택성이 우수하고, 목적에 맞춰 조성을 변화시켜 물성과 활성을 정밀하게 조절할 수 있는 조절 가능성 또한 우수하다. 이러한 장점들은 제올라이트를 촉매로 사용하게 하는 중요한 요소이다.
하지만 단점 또한 가지고 있다. 고온의 수증기 환경에서 제올라이트의 골격이 손상되거나 알루미늄이 dealumination 되는 문제를 가져 수열 안정성이 낮다. 또한 촉매작용 중 생성된 코크가 기공이나 표면에 흡착되는 코킹 문제가 있다. 그리고 기공 크기가 작고 정형화되어 큰 분자의 접근이 힘들다. 고온, 수분, 반응물 등의 이유로 활성성분이 유실되는 경우가 있다는 점 또한 단점으로 지적된다.
- 전이금속 종류의 선정 이유
열분해 진행 시 최종목표를 생각하면 탄화수소의 회수율을 높이는 것이라고 할 수 있다. 그 중에서도 BTX 방향족을 메인 타겟으로 가져가는데 그 이유는 경제적이고 산업적으로 재활용 가능한 고부가가치 화학 원료이기 때문이다. 이러한 배경속에서 방향족의 수율을 높이기 위해 다음과 같은 사항들을 고려할 수 있다.
- 제올라이트의 종류
여러 제올라이트 중 ZSM-5 구조에서의 기공크기가 방향족 생성에 최적의 크기이기 때문에 ZSM-5 구조를 사용한다.
- 흡착 site
다음, 산점의 농도를 높여 C-C 분해를 촉진 시키는 방법이다. 이는 흡착 site를 설계하는 방법으로 이루어진다. 흡착 site는 반응물(예: PE, PP 사슬)이 촉매 표면에 효율적으로 고정되어 활성화되도록 하는 역할을 한다. 일반적으로 Brønsted 산점 (H⁺)이 작용해 고분자 사슬을 프로톤화 → 카르베늄 이온 생성을 유도한다.
금속 도핑 시, 금속 산화물 표면은 Lewis acid site 역할을 하여 π-전자 또는 lone pair를 흡인해 반응 활성화를 이끌어 낸다.
Brønsted 산점 → C-C 결합 분해 유도 Lewis 산점(도핑된 금속) → 탈수소화/고리화 반응 촉진
- 탈수소화& 고리화
방향족 생성은 탈수소화와 고리화로 진행된다. 대부분의 방향족 생성은 올레핀 → 방향족 전환을 포함하며, 이때 H₂가 빠져나가는 것을 탈수소화 반응이라고 하며 이 과정은 필수라고 볼 수 있다. 전이금속(Fe, Ga, Zn 등)은 이 탈수소화 반응의 활성화 에너지를 낮춰주고 d-전자 구조가 적당하여 π-결합을 안정화 시키고 수소를 제거하는데에 유리하다.
다음은 고리화 반응이다. ZSM-5의 Brønsted 산점에서 형성되는 카르베늄 이온은 불안정하다. 도핑된 금속이 전자 밀도 조절 + 안정화 역할을 하여, 올바른 경로로의 분해를 유도한다. 그 결과, 불안정한 중간체가 고리화 → 방향족 경로로 쉽게 전환되며 왁스, 올레핀 등 다른 부산물로 전환되는 비율이 낮아진다.
- 정리
탈수소화 반응을 촉진 시키는 Redox능력, 카르베늄 이온을 안정시키고 활성화 에너지를 결정하는 d-전자 구조, 전자 밀도를 조절하며 안정화 역할을 하는 전기 음성도 및 구조를 가지기 때문에 전이금속을 제올라이트 촉매의 도핑원소로 사용한다.
실험 설계
실험 기구 및 시약
내용
실험 방법
- H-ZSM5 제조 실험
①. 1M NH₄NO₃ 용액 제조 ( 1 L 만들기: NH₄NO₃ 80.0 g + 물 → 1 L 정용 )
②. Na-ZSM-5 → NH₄-ZSM-5 (암모늄 이온교환)
i. 500 mL 비커에 1 M NH₄NO₃ 150–200 mL를 담고 80 °C로 예열.
ii. Na-ZSM-5 10 g 투입, 교반 600 rpm, 80 °C, 2 h 유지. (증발 시 물 보충)
iii. 부흐너 여과 → 초순수로 세척(여액 전도도 ≤ 50 µS/cm).
iv. 다음 회차 동일 조건으로 새로운 1 M NH₄NO₃ 용액 사용.
v. 마지막 세척은 여액 전도도 ≤ 20 µS/cm.
③. NH₄-ZSM-5 → H-ZSM-5 (탈암모니아 소성)
i. 승온: 2 °C·min⁻¹로 500–550 °C (온도 올린 뒤 4-6시간 안정화 시키기)
ii. 자연 냉각, 공기 소성
- 이온교환법
지지체: ZSM-5 H형 10 g 용액: 금속 질산염 HNO₃ (69–70% ACS reagent ≥98%), 초순수 18.2 MΩ·cm 장비: 항온교반(70°C), 부흐너여과, 전도도계, 110°C 오븐, 머플퍼니스(공기), H₂/N₂ 환원로 L/S: 15–20 mL·g⁻¹ → 10 g당 150–200 mL/회 pH: 3.8–4.5 유지(0.1 M HNO₃로 미세 조절) 세척 기준: 여액 전도도 ≤ 20 µS·cm⁻¹
--- stock 용액 --- Fe–ZSM-5: 0.10 M Fe(NO₃)₃·9H₂O 250 mL, 필요 염 0.10×0.25×404.00 = 10.10 g Ni–ZSM-5: 0.10 M Ni(NO₃)₂·6H₂O 250 mL, 필요 염 0.10×0.25×290.79 = 7.27 g Co–ZSM-5: 0.10 M Co(NO₃)₂·6H₂O 250 mL 필요 염 0.10×0.25×291.03 = 7.28 g` 1. 교환용 stock 용액 제조 ①. 메스플라스크(250 mL)에 초순수 ~150mL → 해당 염 완전 용해 → 초순수로 250 mL 정용 pH 확인 후 필요 시 0.1 M HNO₃ 로 3.8–4.5로 맞춤 (탁해지면 pH↓) ②. pH 확인 후 필요 시 0.1 M HNO₃ 로 3.8–4.5로 맞춤 (탁해지면 pH↓).
- Fe(NO₃)₃·9H₂O: ~0.72 g, Ni(NO₃)₂·6H₂O: ~0.50 g, Co(NO₃)₂·6H₂O: ~0.49 g
수준이지만, 교환 평형을 밀기 위해 용액은 과량 제공해야함. --- 이온 교환법 실험 --- 1. 1차 이온교환 ①. 500 mL 비커에 stock 용액 150–200 mL + ZSM-5 10 g . ②. 70 °C, 600 rpm, 5h 교반. 증발 시 초순수로 부피 유지. pH 3.8–4.5 유지. ③. 부흐너 여과 → 초순수 200–300mL로 세척 반복(여액 전도도 ≤ 20 µS·cm⁻¹).
2. 2차 이온교환 ①. 동일 조건으로 stock 용액 150–200 mL 재사용 → 70 °C,5h→ 여과·세척. ②. 목표 로딩이 낮게 나오면 3차까지 반복 가능.
3. 건조 ①. 110 °C, 12h 건조. 4. 소성(질산염 분해, 산점 안정화) ①. 2°C·min⁻¹ 승온 → 500–550°C, 4–6 h, 공기(NOₓ 배출, 후드 필수) 5. 활성화(필요 시) ①. 금속 환원상 필요하면: N₂ 퍼지 30 min → 5–10% H₂/N₂, 1–2 °C·min⁻¹ → 400°C, 2h → N₂ 냉각
결과 및 평가
실험결과 및 분석
H-ZSM5 제조
우선 ZSM5에 각각의 금속을 도핑하기 위해서는 Na-ZSM5를 H-ZSM5로 바꾸는 작업을 진행하여야 한다. 이 과정을 진행하지 않고 바로 도핑을 진행하게 되면, 우선 Co, Fe, Ni가 들어갈 자리에 이미 Na가 자리를 잡고 있기 때문에 위의 금속들이 들어갈 공간이 없어서 도핑이 제대로 되지 않는다.
또한 Na^+자체는 산점이 거의 존재하지 않기 때문에 촉매로서의 성능이 좋지 않다. 따라서 본 연구에서는 NH_4 NO_3와 Na-ZSM5와의 이온 교환을 통해서 우선 Na^+ 를 NH_4^+로 치환해서 금속이온이 들어갈 자리를 우선적으로 만들었고, 그 후 소성과정을 거쳐 NH_4^+가 탈리되며, ( 〖NH_4〗^+ →H++NH_3 (g) )강한 Brønsted 산점을 가지는 H-ZSM5를 제조하였다.
이렇게 제조된 H-ZSM5는 H^+가 proton 형태로 존재해서 금속 이온과 쉽게 교환이 가능하고, 산점도 역시 이전의 Na-ZSM5 대비 굉장히 크다. 또한 폐플라스틱과 열분해시 탈수소, 고리화 반응을 유도해서 방향족의 수득률을 올리는데 큰 역할을 하게 된다.
위의 실험이 잘 진행 되었는지를 FT-IR을 통해서 확인할 수 있다. 먼저 아래의 그림은 Na-ZSM5의 FT-IR 그래프이다.
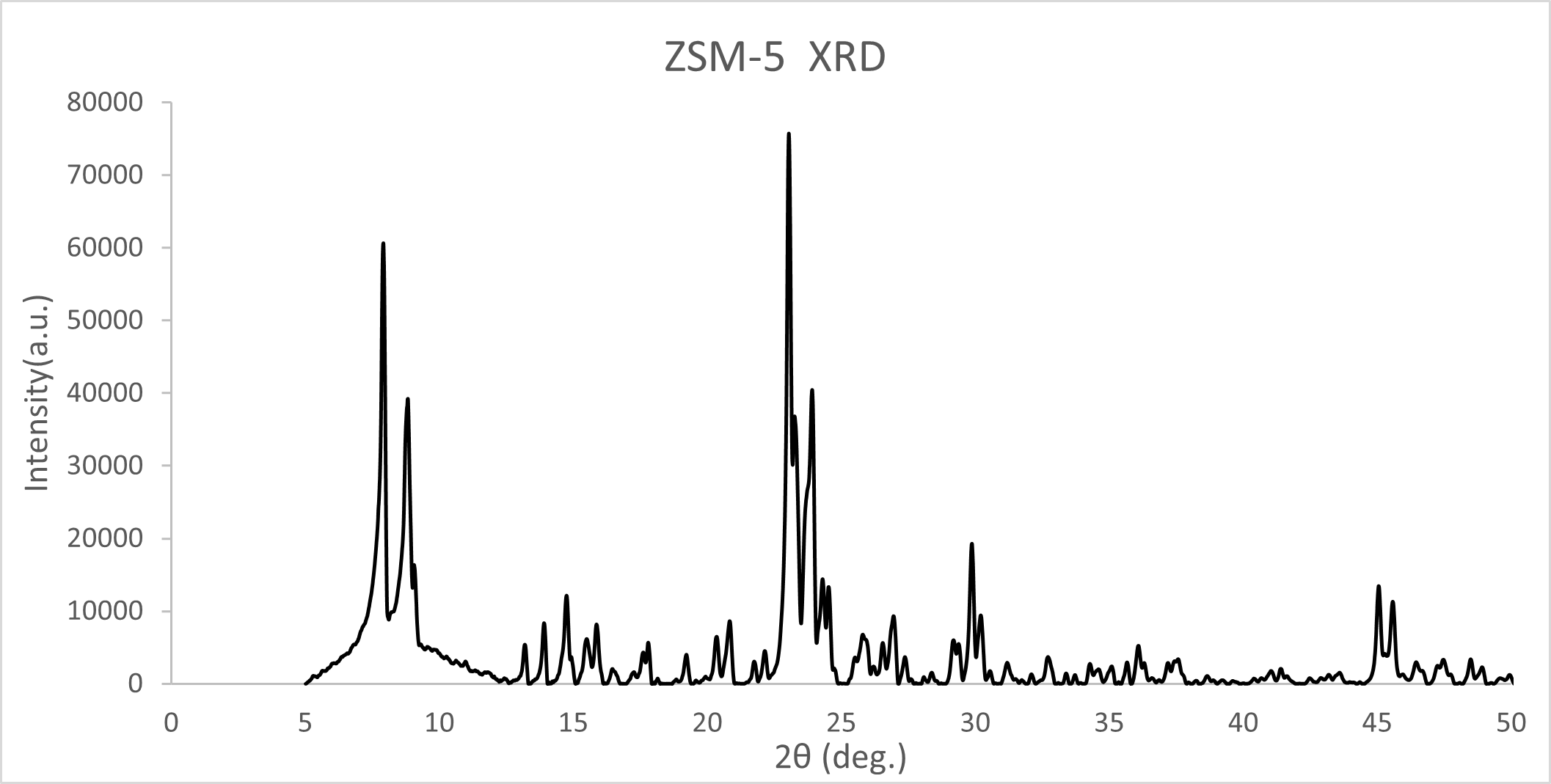
위의 그림은 Na-ZSM5의 FT-IR이다. 위 그림에 표시한 1250-1000부근에 존재하는 peak가 ZSM5 결정 구조의 핵심 peak이며, ZSM5 외부 골격에 존재하는 Si-O-Si 결합의 존재를 알 수 있다. ZSM5 구조에 대해 조금 더 자세히 알아보기 위해서 XRD 분석 결과를 살펴보자. 아래는 XRD 분석 결과 그래프이다.
이제 각 peak에 대해서 알아보자. 먼저 7-10º영역에 존재하는 peak는 ZSM5에 존재하는 10원자 고리기공으로 인해 발생한 peak이고, 22-25º영역에 존재하는 peak는 ZSM5 구조 해석에 가장 핵심이 되는 peak로, ZSM5 구조 특유의 3차원 10원자 고리 기공이 규칙적으로 잘 짜여 있다는 것을 위의 그래프로 확인 할 수 있다. 또한 7-10º영역, 22-25º영역에 있는 두개의 peak가 굉장히 강하게 찍혀 있는 것을 통해 이번 실험에 사용하는 ZSM5의 품질이 매우 우수함을 알 수 있다.
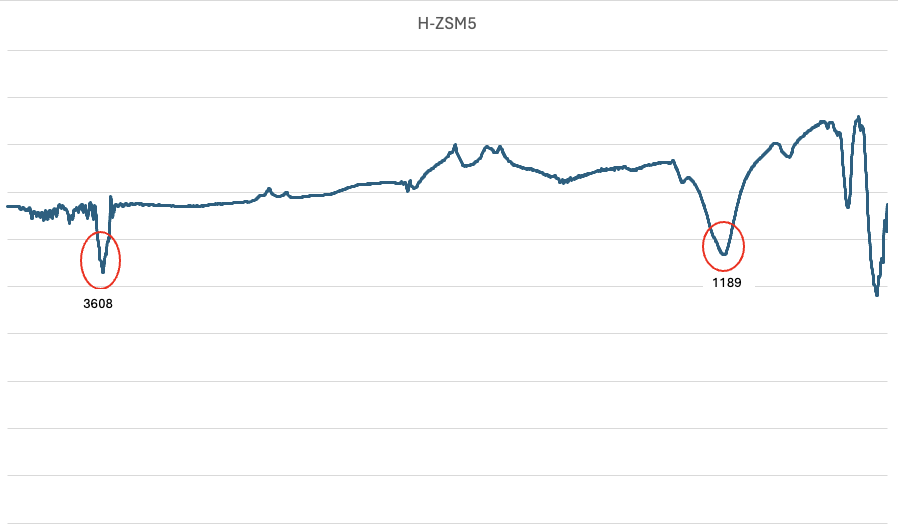
그 다음, 위의 실험을 통해 제조한 H-ZSM5의 FT-IR의 그래프를 살펴보자.
위의 FT-IR의 그래프를 보면 Na-ZSM5와 마찬가지로, 1250-1000cm^(-1)부근에 ZSM5의 핵심 peak가 존재함을 확인할 수 있다. 하지만, 이전과는 다르게 3610〖cm〗^(-1)부근에 좁고 뾰족한 peak가 보이는데 이는 Brønsted 산점으로 인해 존재하는 peak로, Na-ZSM5와 H-ZSM5의 가장 큰 차이점이다. 따라서 위의 그래프를 통해 제작한 물질이 H-ZSM5임을 확인할 수 있다.
전이금속 도핑
이번에는 위에서 제조한 H-ZSM-5에 Co, Fe, Ni를 도핑하여 열분해 촉매 성능을 향상시키는 작업을 진행하였다. 각각의 전이금속을 선택한 이유는 다음과 같다.
Fe : 우수한 탈수소화 능력과 Redox능력으로 방향족화 촉진에 기여한다.
Co : 중간수준의 d-전자구조와 적절한 전기음성도를 가지고 있어서 탈수소화 고리화. 반응을 촉진시키는데에 적합하다.
Ni : 고리화 반응 촉진 및 카르베늄 이온 안정화
이를 바탕으로 이번 실험에서는 Fe, Co, Ni 도핑을 통해 H-ZSM-5의 촉매 성능을 효과적으로 향상시키고, 폐플라스틱 열분해 과정에서 BTX 방향족 생성 효율을 크게 높일 수 있을 것으로 예상할 수 있다. 실험이 성공적으로 진행되었는지 확인하기 위해 X-ray Photoelectron Spectroscopy (XPS) 를 이용하여 분석하였다. XPS란, 표면에 X-선을 쏘고, 튀어나오는 광전자의 에너지를 측정하여 표면에 존재하는 원소를 분석하는 장비로, ZSM5 표면에 금속이 잘 도핑 되었는지 확인하기에 적합한 장비이다. 분석 결과는 다음과 같다.
가장 먼저 Co-ZSM5의 분석 결과를 살펴보자.
위의 그림은 Co-ZSM5의 XPS의 분석 결과이다. XPS 분석의 이유가 전이 금속의 도핑 유무 확인이므로, 전이금속의 Binding Energy 부근을 위주로 살펴보자. 그래프에 800-795eV부근, 783-780eV부근에 확실한 peak를 확인할 수 있다. 두개의 peak는 각각 Co 2P_(1/2), Co 2P_(3/2) 을 나타내며, 이를 통해 표면에 Co가 확실히 존재함을 알 수 있다. 하지만, 금속 Co 특유의 peak (약 778eV 부근)에는 뚜렷한 peak가 보이지 않는데, 이는 금속이 주로 산화된 형태로 존재함을 알 수 있다. 이를 통해서 H-ZSM5 표면에 Co^(2+) 또는 CoOx가 잘 도핑 되어 있음을 확인할 수 있다.
다음은 Ni-ZSM5의 분석 결과를 살펴보자.
위의 그림은 Ni-ZSM5의 XPS 분석 결과이다. 위의 그림에서 역시 855eV 부근, 873eV 부근에서 peak를 확인할 수 있다. 이는 각각 Ni 2P_(3/2), Ni 2P_(1/2)이 시료 표면에 존재함을 의미하므로 이 시료 역시 표면에 Ni이 확실히 존재함을 알 수 있다. 또한 Co와 마찬가지로, 851-853eV 부근에서 관찰할 수 있는 금속 Ni의 peak는 뚜렷하게 관찰되지 않으므로, 이는 표면에 존재하는 Ni이 산화된 상태로 존재함을 확인할 수 있다.
마지막으로 Fe-ZSM5의 분석 결과를 살펴보자.
위의 그래프 역시 725eV 부근에 Fe 2P_(1/2), 711eV 부근에 Fe 2P_(3/2)을 나타내는 peak를 확인할 수 있으며, 이번 시료 역시 표면에 Fe가 확실히 존재함을 확인할 수 있다. 또한 707eV 부근에서 확인할 수 있는 금속 Fe의 peak는 눈에 띄지 않으므로, 이번 시료 역시 Fe가 산화된 상태로 존재함을 알 수 있다.
따라서 위의 결과를 보았을 때, 표면에 도핑한 금속들이 적합한 상태로 존재함을 알 수 있으며, 실험이 성공적으로 진행되었음을 확인할 수 있다.
폐플라스틱 열분해
내용
관련사업비 내역서
내용
완료작품의 평가
향후계획
내용
포스터
내용 NH₄NO₃
H⁺
NH₄⁺
NH₃
Co 2p₁/₂
Co 2p₃/₂
Na⁺
Co²⁺
Ni 2p₃/₂
Ni 2p₁/₂
Fe 2p₃/₂
Fe 2p₁/₂
참고 문헌
1. Zhang, Y., et al. (2024). In-situ catalytic pyrolysis of polyethylene to co-produce BTX aromatics and H₂ by Ni/ZSM-5 in the rotary reactor with solid heat carriers. Fuel, 371, 131950. https://doi.org/10.1016/j.fuel.2024.131950
2. Koti, A., Khongprom, P., & Ratanawilai, S. (2025). Catalytic pyrolysis oil from landfilled plastics through Ni/HZSM-5 and Co/HZSM-5 catalysts. ACS Omega, 10, 5744–5755.
3. Dyer, A. C., Nahil, M. A., & Williams, P. T. (2022). Biomass:Polystyrene co-pyrolysis coupled with metal-modified zeolite catalysis for liquid fuel and chemical production. Journal of Material Cycles and Waste Management, 24, 477–490. https://doi.org/10.1007/s10163-021-01334-0
4. Waziri, A. Y., et al. (2019). Catalytic reforming of gaseous products from pyrolysis of low-density polyethylene over iron-modified ZSM-5 catalysts. Applied Petrochemical Research, 9, 101–112. https://doi.org/10.1007/s13203-019-0230-4