"515"의 두 판 사이의 차이
(→조사 내용) |
(→공정 개선 및 LNP 구성 및 조성) |
||
| 153번째 줄: | 153번째 줄: | ||
====공정 개선 및 LNP 구성 및 조성==== | ====공정 개선 및 LNP 구성 및 조성==== | ||
| − | + | 3.4 LNP manufaturing | |
| + | 3.4.1 microfluidics | ||
| + | [[파일:Example.jpg]] | ||
| + | Microfluidics는 유체의 미세한 조절과 변형이 요구되는 실험, 산업에서 쓰이는 학문이다. mRNA-LNP 공정에서 mRNA 용액과 지질이 용해된 에탄올 용액을 혼합하여 mRNA-LNP를 제조할 때, Microfluidics를 이용한 Staggered herringbone micromixer를 사용한다. 이 공정에서 Total Flow Rate(TFR, 유체의 흐름속도), Flow Rate Ratio(FRR, 수용상과 유기상의 흐름비), Lipid 용액의 Composition, Material이 mRNA-LNP 특성을 결정한다. | ||
| + | |||
| + | 3.4.2 manufacturing parameter | ||
| + | 3.4.2.1 TFR | ||
| + | |||
| + | 수용상과 유기상의 혼합속도 또는 전체 유체의 속도이다. 거시적으로는 생산속도로 볼 수 있다. 보통 5 mL/min ~ 20 mL/min 수준으로 사용된다. | ||
| + | |||
| + | 3.4.2.2 FRR | ||
| + | |||
| + | 수용상(mRNA와 buffer)과 유기상(지질)의 흐름비, 유량비 또는 각 수용상과 유기상의 syringe pump의 세기비로도 볼 수 있다.1:1 ~ 5:1 수준으로 사용된다. | ||
| + | |||
| + | 3.4.4 각 Parameter가 LNP 크기와 균일성에 미치는 영향 | ||
| + | 3,4.4.1 TFR의 영향 | ||
| + | |||
| + | |||
| + | 표 1 TFR 변화에 따른 LNP크기와 PDI 변화 | ||
| + | |||
| + | mRNA-LNP 제조 공정시 Total Flow rate가 LNP 크기에 미치는 영향을 알아보기 위하여 TFR을 5~20 mL/min 으로 변화시킨다. 이 때 FRR은 3:1 (수용상:유기상)로 고정하며 Lipid composition은 DSPC:Chol:X:PEG-2000=10:40:48:2 (X는 Cationic 또는 ionisable로 바꾸면서 관찰)로 고정시킨다. 최종적으로 얻은 혼합물의 밀도는 2 mg/mL가 되도록 정제한다. 결과는 다음 그래프와 같았다. | ||
| + | |||
| + | |||
| + | LNP의 크기는 DOTAP을 사용하였을 때 가장 작게 관측되었으며 MC3, DDAB 순으로 그 크기가 커짐을 알 수 있다. 또한 TFR이 5 mL/min 일 때 LNP의 크기가 커졌으며, TFR이 10 mL/min 일 때와 20 mL/min 일 때 크기는 거의 비슷하게 관측되었다. PDI값은 Lipid마다 달랐지만 모든 TFR에서 변화가 없었고 모두 0.2 이하로 안정적인 것을 관측할 수 있었다. | ||
| + | 결론적으로 LNP는 빠른 TFR에서 작은 크기로 형성되며 TFR은 균질성에 미치는 영향이 미미하다고 사료된다.[3] | ||
| + | |||
| + | 3.4.4.2 FRR의 영향 | ||
| + | |||
| + | |||
| + | 표 2 FRR 변화에 따른 LNP크기와 PDI 변화 | ||
| + | |||
| + | 작은 크기의 mRNA-LNP가 세포질로 침투해야 하는 mRNA백신에 유리하다고 판단되어 TFR은 20 mL/min 으로 고정하고 Lipid composition은 DSPC:Chol:X:PEG-2000=10:40:48:2 (X는 Cationic 또는 ion-isable로 바꾸면서 관찰)로 고정시킨다. FRR은 (➀1:1, ➁3:1, ➂5:1, 수용상:유기상) 세 경우를 관측하여 LNP의 크기와 PDI값을 측정하였다. | ||
| + | |||
| + | FRR이 1:1 일 때 LNP의 크기가 다른 FRR의 비율에 비해 매우 크게 나타난 것을 관측할 수 있었으며 PDI값 역시 MC3와 DDAP Lipid에서 0.2를 초과하며 매우 불안정한 모습을 관찰할 수 있었다. FRR이 3:1인 경우와 5:1인 경우 LNP의 크기와 PDI 값의 변화가 미미하였음을 알 수 있었으며 mRNA-LNP 백신 제조시 FRR의 비율이 1:1 인 경우는 소거하며 3:1 ~ 5:1 이 가장 적합함을 시사하였다. [4] | ||
| + | |||
| + | |||
| + | 3.4.4.3 Lipid composition의 영향 | ||
| + | |||
| + | 표 3 Lipid composition의 영향에 따른 LNP크기, PDI변화 | ||
| + | 위 두 실험에서 얻은 결론으로 TFR은 20 mL/min으로 FRR은 3:1로 고정하며 Lipid의 비율을 변화시키며 LNP의 크기와 PDI 값을 측정한다. Lipid composition의 변화는 Structural Lipid인 DSCP와 PEG-2000은 100중 10과 2인 상태로 고정하며 choles-terol과 ionisable lipid 또는 cationic lipid 조성을 변경하며 LNP의 크기와 PDI를 관측한다. | ||
| + | DSCP:Cholesterol:X:PEG2000=(10:10:78:2 ~ 10:70:18:2) | ||
| + | DOTAP의 경우 LNP크기의 변화는 cho-lesterol의 비율이 증가할수록 그 크기가 감소하였으며 PDI값이 작아지는 것으로 관측된다. Cholesterol의 함량이 증가할수록 제조공정에서는 유리할 것으로 판단된다. 그러나 MC3의 경우 Cholesterol 함량의 변화에도 LNP의 크기, PDI 값의 변화가 미미하게 관측된다. DDAB같은 경우 낮은 Cholesterol 함량에는 커다란 크기의 LNP, 높은 PDI값이 관측되면서 매우 불안정한 모습을 보였으며 cholesterol 함량이 100중 30 이후에는 함량이 증가할수록 LNP 크기는 작아졌으며 PDI값은 대개 비슷한 값을 가지는 것으로 관측되었다. [5] | ||
| + | |||
| + | 3.4.4.4 Parmater 선택 | ||
| + | |||
| + | mRNA-LNP를 이용한 백신은 세포질 내로 침투하여 엔도솜 탈출과정을 거쳐 단백질 합성을 하는 것이 최종 목적이다. 이에 타겟 세포질 침투에 용이하도록 작은 크기의 LNP를 채택해야 한다. 또한 공정과정에서 낮은 PDI값을 갖도록 설계해야 할 것이다. 이와 같은 이유로 herringbone micromixer를 이용한 mRNA-LNP 공정에서는 높은 FTR값을 가져야 하며 FRR값은 수용상의 흐름속도가 더 빠르도록 설계해야하며, 콜레스테롤의 함량을 높이하되 타겟 조직과의 상호작용을 고려하여 Ionisable lipid 또는 Cationic lipid의 비율을 조절해야 한다. | ||
==결과 및 평가== | ==결과 및 평가== | ||
2021년 12월 16일 (목) 23:33 판
프로젝트 개요
기술개발 과제
국문 : 핵산 물질의 효과적인 체내 전달을 위한 지질 나노 입자의 개선(개량) 연구
영문 : Improvement of Lipid Nanoparticles for Efficient Nucleic Acid Delivery in Vivo
과제 팀명
515
지도교수
이종범 교수님
개발기간
2021년 9월 ~ 2021년 12월 (총 4개월)
구성원 소개
서울시립대학교 화학공학과 20153400** 신*빈(팀장)
서울시립대학교 화학공학과 20153400** 김*찬
서울시립대학교 화학공학과 20153400** 김*준
서울시립대학교 화학공학과 20153400** 정*희
서울시립대학교 화학공학과 20153400** 최*종
서론
개발 과제의 개요
개발 과제 요약
- 핵산물질을 이용한 치료에 이용되는 Lipid nanoparticle(LNP)에 사용되는 지질들의 역할 파악
- LNP를 구성하는 각 지질들의 구조 변형, 개선 합성 을 위한 연구들에 대해 조사
- 지질 구조의 변경이 가져올 효과에 대한 조사
- LNP 구성 및 조성의 변경이 가져오는 효과에 대하여 조사
개발 과제의 배경
RNAi, 항체 생성, 특정 체내 부족 단백질 생성 등을 이용하는 핵산 물질을 이용한 치료가 활발히 연구되고 있으며, 코로나19 백신, 암 치료제 등으로 상용화되기까지 이르렀다. 그러나 이러한 핵산 물질들은 불안정한 상태의 물질로 분해되기 쉽기 때문에 목표 표적까지 핵산 물질을 안전하게 전달시킬 수 있는 효율적인 전달체가 필요하다. 또한 이같은 핵산 물질의 보호 뿐만 아니라 체내에서 이루어지는 면역반응의 회피, 세포독성, 안정성, 체내 분포, 전달 효율 등 고려해야 할 요소들이 추가적으로 존재하며 이들을 조절하기 위한 연구가 필요하다. 특히 주요 전달체로 이용되고 있는 지질나노입자(LNP)는 여러 방면에서 활발한 연구가 이뤄지고 있는 바, LNP를 구성하는 다양한 지질을 조사하고, 최신 LNP 연구 동향에 대해 알아본다.
개발 과제의 목표 및 내용
- LNP 제작에는 여러 지질이 사용된다. 이때 사용되는 지질에 따라 만들어지는 LNP의 구조에 안정성을 추가해 주거나 LNP의 크기 등에 영향을 주는 특정 지질의 특성에 대하여 조사한다.
- 조사한 지질의 특성이 지질의 어떤 구조, 작용기에 의해 정해지는지, 그리고 이를 이용하여 지질의 특성을 바꾸기 위한 비슷한 구조의 지질들을 연구한 논문들을 찾아본다.
- 약물이 몸 속에 전달되는 능력을 향상시키기 위한 어떤 시도들이 있었는지 찾아본다.
- 의도한 시간 이상으로 몸에 존재하는 약물은 부작용을 일으킬 수 있어 적절한 분해성이 요구되는 바 몸 속으로 들어온 LNP가 효과적으로 분해되기 위해 영향을 미치는 요소에 대해 찾아보고 실제 체내에서 분해되는 메커니즘을 살펴본다.
- 약물이 투여되는 방식에 따라서 달라지는 지질 성능에 대하여 살펴본다.
- LNP의 구성을 변경하였을 때 달라지는 성능에 대하여 조사한다.
관련 기술의 현황
관련 기술의 현황 및 분석(State of art)
전 세계적인 기술현황
- RNA interference 치료제인 Onpattro가 최초로 FDA승인을 얻어 상용 제품으로 출시되었다.
- Pfizer, moderna 사의 백신이 LNP에 바이러스 단백질 mRNA를 담아 백신으로 이용하고 있다.
- 다발성 골수종, 난소암 치료제인 DOXIL이 개발되었다.
- 수용성 아밀로이드증 치료제이며 siRNA 기반 LNP 약물인 Patisiran이 개발되었다.
특허조사 및 특허 전략 분석
향상된 지질 조성물 - 특허번호 : PCT/US2010/038224 - 출원일 : 2010.6.10. - 등록일 : 2010.12.16. - 특허권자 : 알닐람 파마슈티칼스 인코포레이티드 본 발명은 화학식 (I)의 양이온성 지질, 화학식 I의 양이온성 지질을 포함하는 향상된 지질 제제 및 상응하는 이용 방법을 특징으로 한다. 또한, 표적화 지질, 그리고 이런 표적화 지질을 포함하는 특정한 지질 제제가 개시된다.
폴리에틸렌글리콜과 트리페닐포스포늄이 컨쥬게이트된 물질 및 이를 적용한 미토콘드리아 표적 자기조립형 나노약물 전달체 - 특허번호 : KR1017433990000 - 출원일 : 2016.05.31. - 등록일 : 2017.05.29. - 특허권자 : 충남대학교산학협력단 폴리에틸렌글리콜(PEG)의 말단에 트리페닐포스포늄(TPP)이 화학적으로 결합된 하기 화학식 1의 PEGTPP (Polyethylene gylcol-Triphenylphosphonium) 컨쥬게이트.
약물전달체 - 특허번호 : KR1010783020000 - 출원일 : 2008.05.29. - 등록일 : 2011.10.25. - 특허권자 : (주)제테마 (a) 생체 적합성 중합체; 및 (b) 상기 중합체에 컨쥬게이션된 소수성기를 포함하는 약물전달체.
생체활성 친유성 화합물을 갖는 PEG화된 지질 나노입자 특허번호 : KR1020187006989 출원일 : 2016.08.11. 등록일 : 2018.03.30. 발명자 : 가이야르,피테르얍,립,야콥 본 발명은 친유성 진단 또는 치료 제제를 이를 필요로 하는 대상에게 전신 또는 국소 전달하기 위한 나노입자에 관한 것이다. 본 발명의 나노입자는 수용성 중합체 및 생체 적합성 지질 및 친유성 제제 중 적어도 하나를 포함한다. 나아가,본 발명은 본 발명의 나노입자를 사용한 안과 치료에 관한 것이다. 또한, 본 발명은 본 발명의 나노입자를 포함하는 조성물 및 포뮬레이션에 관한 것이다.
산화된 콜레스테롤을 함유하는 약물 전달 시스템 - 특허번호 : PCT/US2020/013639 - 출원일 : 2020.01.15. - 등록일 : 2020.07.23. - 특허권자 : 조지아 테크 리서치 코포레이션 나노입자 조성물은 이온화가능한 지질, 인지질, PEG-지질, 및 D-스테롤 고리 근처에서 히드록실 기로 변형된 콜레스테롤을 포함하는 것으로 개시된 나노입자 조성물은 간세포(hepatocyte)보다는 간 쿠퍼 세포(Kupffer cell) 및 내피 세포(endothelial cell)를 더욱 우선적으로 표적화할 수 있다. 이는 치료 mRNA를 신체의 특정 조직에 효과적으로 전달하기 위한 조성물 및 방법을 제공하고 이로써 기능장애 쿠퍼 세포 및 내피 세포가 질환 발병기전에 관여하는 간 질환을 치료하는 데 유익할 수 있다.
선행기술인 Ionizable lipid (MC3) 및 PEG lipid, 콜레스트롤 등을 상위개념으로 일부 하위개념들을 선택적으로 포함하는 구성인 지질나노전달체를 청구범위로 하여 기존 LNP에 비해 이질적이거나 동일하더라도 현저한 효과를 가진 LNP를 개발할 수 있다면, 선택발명의 특허요건을 만족함과 동시에 구성요건 완비 원칙을 회피할 수 있을 것이다.
개발과제의 기대효과
기술적 기대효과
- LNP를 구성하는 각 지질들의 개선방안들과 그에 따른 효과들을 이용한다면 개발자가 원하는 방향의 고성능 LNP 약물을 제조하는 데 도움이 될 수 있다.
- LNP 표면 형태(morphology)에 따른 유전자 전달 효율에의 영향을 알고 적절한 지질상 및 형태를 설계할 수 있다.
경제적, 사회적 기대 및 파급효과
- 백신을 개발할 때 중요한 것은 신속하게 개발을 진행하는 것과 개발 비용을 절감하는 것이다. mRNA백신의 특징이 핵산물질의 개발이 빠르게 이루어질 수 있는 점을 감안하면, 이 때 이미 연구가 진행된 LNP나 구성 지질 성분을 이용한다면 개발 목표를 더욱 빠르게 이루어낼 수 있을 것이다.
- 효율적일 수 있는 지질을 테스트 전에 평가하는 기준을 제시해 동물 실험, 임상 실험에 들어갈 비용을 절감하는 데 도움을 줄 수 있을 것이다.
기술개발 일정 및 추진체계
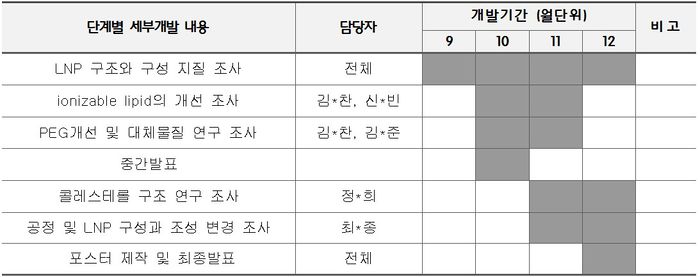
개발 일정
5인 각각이 조사를 진행하였으며, 주 1회 이상 모임을 가져 조사 내용을 공유하며 설명,발표하는 시간을 가졌음.
주 1회 조사한 내용을 종합하여 조교님께 제출하여 피드백을 받음.
본론
이론적 배경
약물 전달 경로
핵산이라는 약물을 전달하기 위한 LNP의 성능을 향상시키기 위해서는 이 약물이 전달되는 경로에 대하여 이해하는 것이 가장 중요하다.
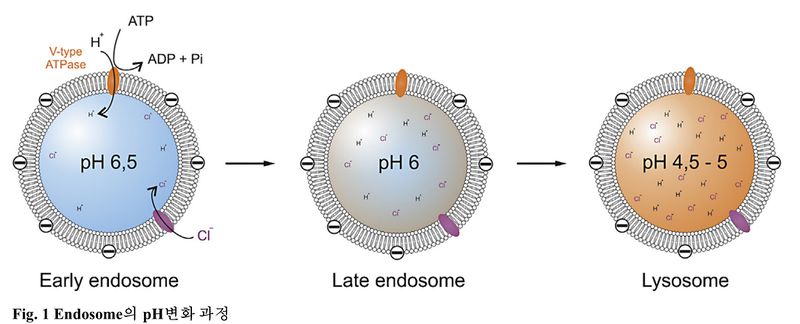
이 LNP는 Intravenous injection(IV) 혹은 Intramuscular injec-tion(IM) 경로로 체내에 주입되는 것이 일반적이며, 체내로 들어온 약물은 세포 내로 이입되게 되고(endocytosis), 이후 핵산물질이 세포질로 이동해서 작용하게 된다. 이 때 endocytosis의 가장 일반적인 경로는 clathrin-mediated endocytosis이다. 그리고 이 clathrin-mediated endocytosis는 세포 내로 유입된 소포가 초기 엔도솜을 거쳐 리소좀에서 분해되어 소멸되는 경로를 거치게 된다. 이 과정은 V-type ATPase가 엔도솜에 proton을 제공하여 엔도솜 내부를 산성화시키는데, 초기 엔도솜(pH 6.0-6.5)과 후기 엔도솜(pH 4.5-5.5)을 거쳐 리소좀(pH 4-5)으로 향하면서 산성화되고 리소좀에서 가수분해되는 순서로 세포 내로의 유입을 원하지 않는 물질의 제거가 이루어진다. 따라서 이 엔도솜을 탈출하여 세포질로 약물을 전달시키는 과정이 매우 중요하다. 특히 LNP를 전달 매체로 하여 siRNA를 전달하는 경우에 대한 연구에서 endosomal escape rate는 1~3%에 불과하였다는 결과를 보인 사례도 존재하는 등 이 endosomal escape가 약물 전달에 있어 rate limiting step이라고 볼 수 있다. 즉, 이 부분에 대한 개선이 결과적으로 약물 투여량을 줄이는 효과를 낼 수 있고 나아가 핵산 물질을 활용한 약물의 상용화에 중요한 장벽이라는 것을 시사한다.
하지만 이 endosomal escape가 일어나는 메커니즘은 정확하게 밝혀지지 않았다. 그에 따라 정확히 어떠한 방식으로 구조 개선을 해야 엔도솜 탈출을 개선할 수 있을지에 대한 방향은 확실하지 않다. 아직까지 이 메커니즘을 조사하거나 정량적으로 측정하기 위한 분석방법이 여럿 제시되었지만, 공통된 합의를 이루어내지는 못했다. 그에 따라 현재 개발되는 LNP에 사용된 지질들은 지금껏 제시된 여러 가설들에 기반하여 개발이 이루어졌다.
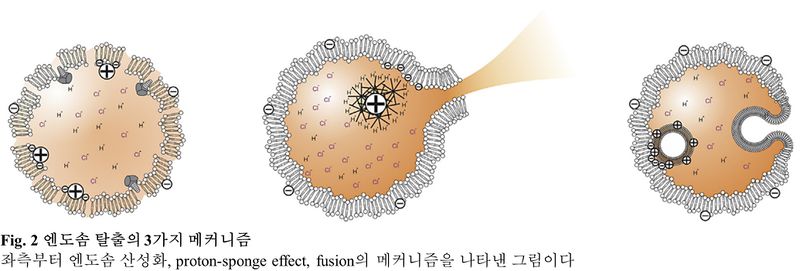
첫 번째 가설은 엔도솜의 산성화가 엔도솜막과 지질의 상호작용을 촉진시키고 이는 엔도솜막을 계속 불안정하게 만들어 작은 구멍을 형성하고 나노물질의 누출을 일어나도록 한다는 것이다. 이 메커니즘은 이후 제시되는 것과는 막과의 상호작용이 직접적으로 막에 구멍을 나게 한다는 점에서 다르다.
다른 가설은 proton-sponge effect이다. 이 가설은 엔도솜 내부가 보다 상대적으로 낮은 pH를 가진다는 점에서 만약 완충효과를 띌 수 있는 물질이 들어간다면 V-type ATPase의 작용을 더욱 많이 일어나게 할 것이라는 주장을 한다. 이 결과로 pro-tonated된 LNP가 막과의 상호작용으로 막을 더 불안정하게 만들 것이고, 또한 LNP 내부 지질 간의 정전기적 반발력이 부피적 팽창을 유도하여 막의 불안정에 기여한다. 또한 지속적인 이온의 유입은 삼투효과를 일으켜 물의 유입을 촉진하게 되고 그 결과 엔도솜이 파괴(rupture)되는 결과를 가져와 내부의 핵산물질이 세포질로 옮겨질 수 있게 한다고 설명한다. 이는 일반적으로 가장 주된 메커니즘으로 받아들여졌다. 이 과정을 잘 일으킬 수 있을 것으로 제시된 지질들은 head group에 아민기를 포함한 지질들이었으며, 그에 따라 연구되는 많은 지질들이 아민기를 포함하거나 또 다른 완충 효과를 할 수 있는 지질들을 기반으로 개발되었다.
또 다른 가설은 막의 융합(fusion)에 의한 메커니즘이다. 이 가설은 마찬가지로 불안정해진 엔도솜막이 나노입자막과 융합하여 내부 물질을 세포질로 방출하게 되는 메커니즘으로 여러 helper lipid들이 이 효과를 위해 LNP에 추가되었다. 그 중 하나인 콜레스테롤 또한 여러 다른 기능도 있지만 이 막과의 융합성(fusogenicity)를 향상시키기 위한 목적으로 LNP에 포함되었다고 한다. 지금까지 약물의 전달능력을 향상시키기 위해서 약물 전달 메커니즘에 대하여 살펴보았다. 이를 정확히 분석할 수 있는 방법이 나와준다면 LNP를 통한 핵산물질 전달은 더욱 발전할 수 있을 것이다. 하지만 그 메커니즘이 확실하게 밝혀지지 않은 지금, 약물의 상용화 및 개선을 위해서 이루어지는 연구들은 전달 능력의 개선에 대한 수치적 비교 뿐 아니라 targetting, cytotoxicity 등 또 다른 측면에서의 연구 등을 통해 활발하게 이루어지고 있다.
지질의 정량적 평가법
여기서는 본 리뷰에서 리뷰한 연구들의 보편적인 실험 과정에 대해 설명한다. 합성된 지질들은 실제 사용 환경과 비슷하게 LNP를 형성한 뒤 in vitro screening, in vivo screening(mice, rat, Non-human Pri-mates)을 거쳐 검증을 진행한다.
먼저 in vitro screening의 경우는 HeLa세포주와 luciferase를 이용하여 screening을 거치게 된다. siRNA 전달을 목표로 하는 경우 HeLa 세포주에 firefly luciferase와 Renilla luciferase를 발현시키도록 만든 뒤 LNP에 antifirefly luciferase RNA를 집어넣어 전달시켜 얼마나 firefly 발현이 억제되는지, 그와 동시에 Renilla에는 변화가 없는지를 확인하여 전달능력과 세포독성(cytotoxicity)을 평가하는 것이 일반적이다. mRNA의 경우에는 firefly를 생산할 수 있는 mRNA를 전달하여 측정을 하는 방식이 일반적이다. 물론 in vitro screening은 체내와 환경이 달라 체내 전달과 상당히 다른 결과를 내는 경우가 자주 있어 이것으로 최적의 지질을 판단하기에는 무리가 있다. 다만 번거로운 절차, 시간, 비용이 들어가는 in vivo screening에 앞서 적절하지 않은 것으로 판단되는(낮은 전달, 세포독성) 지질을 선상에서 제외하기에 적절하다고 할 수 있다.
다음으로 in vivo screening의 경우에는 흔히 혈액 응고에 기여하는 제7인자 (Factor VII)에 대한 억제를 측정하는 것이 siRNA 측정에는 일반적이다. 7인자는 간조직에서만 생성되며 혈액으로 분비되어 정량화가 쉽다는 특징을 가진다. 이 때부터는 필요에 따라 다양한 여러 핵산물질이 사용되기도 한다(주로 정량적 측정이 용이함이 주된 선택의 기준이다). 면역 반응이나 항체 생성 확인을 위해 인플루엔자 바이러스 mRNA를 넣는 등이 그 예이다.
조사 내용
내용
Ionizable lipids
내용
PEGs
내용
Alternatives for PEGs - POEGMA
Cholesterols
내용
공정 개선 및 LNP 구성 및 조성
3.4 LNP manufaturing
3.4.1 microfluidics
 Microfluidics는 유체의 미세한 조절과 변형이 요구되는 실험, 산업에서 쓰이는 학문이다. mRNA-LNP 공정에서 mRNA 용액과 지질이 용해된 에탄올 용액을 혼합하여 mRNA-LNP를 제조할 때, Microfluidics를 이용한 Staggered herringbone micromixer를 사용한다. 이 공정에서 Total Flow Rate(TFR, 유체의 흐름속도), Flow Rate Ratio(FRR, 수용상과 유기상의 흐름비), Lipid 용액의 Composition, Material이 mRNA-LNP 특성을 결정한다.
Microfluidics는 유체의 미세한 조절과 변형이 요구되는 실험, 산업에서 쓰이는 학문이다. mRNA-LNP 공정에서 mRNA 용액과 지질이 용해된 에탄올 용액을 혼합하여 mRNA-LNP를 제조할 때, Microfluidics를 이용한 Staggered herringbone micromixer를 사용한다. 이 공정에서 Total Flow Rate(TFR, 유체의 흐름속도), Flow Rate Ratio(FRR, 수용상과 유기상의 흐름비), Lipid 용액의 Composition, Material이 mRNA-LNP 특성을 결정한다.
3.4.2 manufacturing parameter 3.4.2.1 TFR
수용상과 유기상의 혼합속도 또는 전체 유체의 속도이다. 거시적으로는 생산속도로 볼 수 있다. 보통 5 mL/min ~ 20 mL/min 수준으로 사용된다.
3.4.2.2 FRR
수용상(mRNA와 buffer)과 유기상(지질)의 흐름비, 유량비 또는 각 수용상과 유기상의 syringe pump의 세기비로도 볼 수 있다.1:1 ~ 5:1 수준으로 사용된다.
3.4.4 각 Parameter가 LNP 크기와 균일성에 미치는 영향 3,4.4.1 TFR의 영향
표 1 TFR 변화에 따른 LNP크기와 PDI 변화
mRNA-LNP 제조 공정시 Total Flow rate가 LNP 크기에 미치는 영향을 알아보기 위하여 TFR을 5~20 mL/min 으로 변화시킨다. 이 때 FRR은 3:1 (수용상:유기상)로 고정하며 Lipid composition은 DSPC:Chol:X:PEG-2000=10:40:48:2 (X는 Cationic 또는 ionisable로 바꾸면서 관찰)로 고정시킨다. 최종적으로 얻은 혼합물의 밀도는 2 mg/mL가 되도록 정제한다. 결과는 다음 그래프와 같았다.
LNP의 크기는 DOTAP을 사용하였을 때 가장 작게 관측되었으며 MC3, DDAB 순으로 그 크기가 커짐을 알 수 있다. 또한 TFR이 5 mL/min 일 때 LNP의 크기가 커졌으며, TFR이 10 mL/min 일 때와 20 mL/min 일 때 크기는 거의 비슷하게 관측되었다. PDI값은 Lipid마다 달랐지만 모든 TFR에서 변화가 없었고 모두 0.2 이하로 안정적인 것을 관측할 수 있었다.
결론적으로 LNP는 빠른 TFR에서 작은 크기로 형성되며 TFR은 균질성에 미치는 영향이 미미하다고 사료된다.[3]
3.4.4.2 FRR의 영향
표 2 FRR 변화에 따른 LNP크기와 PDI 변화
작은 크기의 mRNA-LNP가 세포질로 침투해야 하는 mRNA백신에 유리하다고 판단되어 TFR은 20 mL/min 으로 고정하고 Lipid composition은 DSPC:Chol:X:PEG-2000=10:40:48:2 (X는 Cationic 또는 ion-isable로 바꾸면서 관찰)로 고정시킨다. FRR은 (➀1:1, ➁3:1, ➂5:1, 수용상:유기상) 세 경우를 관측하여 LNP의 크기와 PDI값을 측정하였다.
FRR이 1:1 일 때 LNP의 크기가 다른 FRR의 비율에 비해 매우 크게 나타난 것을 관측할 수 있었으며 PDI값 역시 MC3와 DDAP Lipid에서 0.2를 초과하며 매우 불안정한 모습을 관찰할 수 있었다. FRR이 3:1인 경우와 5:1인 경우 LNP의 크기와 PDI 값의 변화가 미미하였음을 알 수 있었으며 mRNA-LNP 백신 제조시 FRR의 비율이 1:1 인 경우는 소거하며 3:1 ~ 5:1 이 가장 적합함을 시사하였다. [4]
3.4.4.3 Lipid composition의 영향
표 3 Lipid composition의 영향에 따른 LNP크기, PDI변화 위 두 실험에서 얻은 결론으로 TFR은 20 mL/min으로 FRR은 3:1로 고정하며 Lipid의 비율을 변화시키며 LNP의 크기와 PDI 값을 측정한다. Lipid composition의 변화는 Structural Lipid인 DSCP와 PEG-2000은 100중 10과 2인 상태로 고정하며 choles-terol과 ionisable lipid 또는 cationic lipid 조성을 변경하며 LNP의 크기와 PDI를 관측한다. DSCP:Cholesterol:X:PEG2000=(10:10:78:2 ~ 10:70:18:2) DOTAP의 경우 LNP크기의 변화는 cho-lesterol의 비율이 증가할수록 그 크기가 감소하였으며 PDI값이 작아지는 것으로 관측된다. Cholesterol의 함량이 증가할수록 제조공정에서는 유리할 것으로 판단된다. 그러나 MC3의 경우 Cholesterol 함량의 변화에도 LNP의 크기, PDI 값의 변화가 미미하게 관측된다. DDAB같은 경우 낮은 Cholesterol 함량에는 커다란 크기의 LNP, 높은 PDI값이 관측되면서 매우 불안정한 모습을 보였으며 cholesterol 함량이 100중 30 이후에는 함량이 증가할수록 LNP 크기는 작아졌으며 PDI값은 대개 비슷한 값을 가지는 것으로 관측되었다. [5]
3.4.4.4 Parmater 선택
mRNA-LNP를 이용한 백신은 세포질 내로 침투하여 엔도솜 탈출과정을 거쳐 단백질 합성을 하는 것이 최종 목적이다. 이에 타겟 세포질 침투에 용이하도록 작은 크기의 LNP를 채택해야 한다. 또한 공정과정에서 낮은 PDI값을 갖도록 설계해야 할 것이다. 이와 같은 이유로 herringbone micromixer를 이용한 mRNA-LNP 공정에서는 높은 FTR값을 가져야 하며 FRR값은 수용상의 흐름속도가 더 빠르도록 설계해야하며, 콜레스테롤의 함량을 높이하되 타겟 조직과의 상호작용을 고려하여 Ionisable lipid 또는 Cationic lipid의 비율을 조절해야 한다.
결과 및 평가
완료 작품의 소개
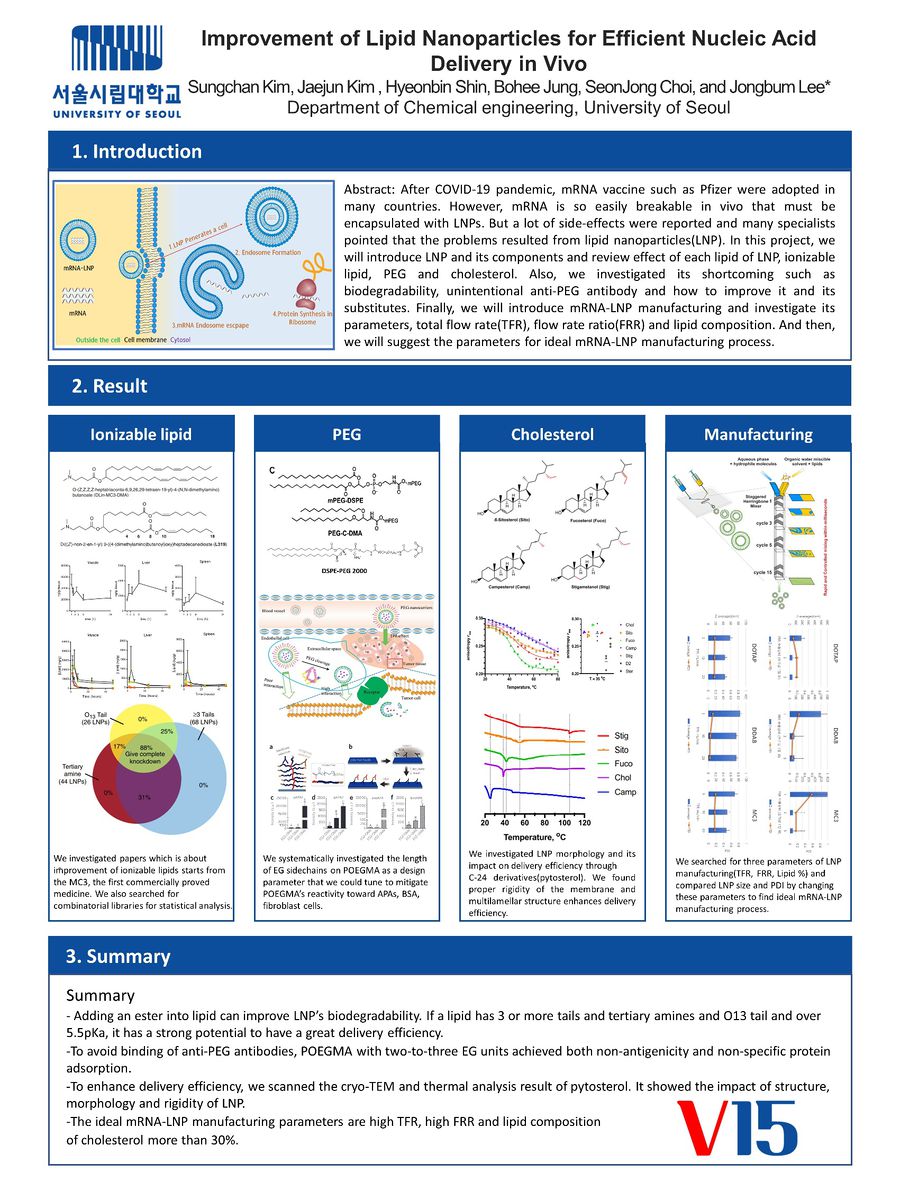
조사 내용을 정리하여 리뷰 논문의 형식으로 작성하였다.
[그림넣을꺼임 리뷰논문 전체샷으로 한걸로]
포스터
완료작품의 평가
내용
향후계획
향후 좀 더 최신의 지질 합성에 대한 조사를 좀 더 하여야 하며, 추후 이루어질 엔도솜 탈출 메커니즘에 대한 분석이 정확하게 이루어지는지에 대하여 지속하여 정보를 탐색할 것이다