유준재 교수님 1팀
프로젝트 개요
기술개발 과제
국문 : Coke Oven Gas를 이용한 알데하이드 생산 공정 모델링
영문 : Modeling an Aldehyde Production Process Using Coke Oven Gas
과제 팀명
유준재교수님 1팀
지도교수
유준재 교수님
개발기간
2025년 9월 ~ 2025년 12월 (총 4개월)
구성원 소개
서울시립대학교 화학공학과 20223400** 전*진(팀장)
서울시립대학교 화학공학과 20193400** 최*현
서울시립대학교 화학공학과 20203400** 남*현
서울시립대학교 화학공학과 20223400** 김*영
서울시립대학교 화학공학과 20223400** 이*민
서론
개발 과제의 개요
개발 과제 요약
◇ 인구의 기하급수적인 증가와 이에 따른 산업 발전으로 인해 에너지 수요가 급격히 증가함에 따라 과거에는 주로 화석연료를 통해 에너지가 공급되어 왔다. 현재의 탄소 기반 에너지 시스템은 글로벌 연료자원의 고갈과 기후변화에 대응해야 하며, 이에 따라 새로운 재생 가능 에너지원의 탐색과 화석연료의 지속가능한 활용이 에너지 공급망의 핵심 과제로 부상하고 있다. 산업 부문 중 철강산업은 가장 많은 에너지를 소비하는 분야로, 전 세계 CO₂ 배출량의 약 9%를 차지한다. 이 산업에서 생성되는 COG(Coke Oven Gas)는 연료이자 환원제로 사용되며, 석탄을 Coke Oven Battery에서 고온으로 산소 없이 가열해 생산된다. COG는 높은 함량의 수소와 유용한 화합물을 포함하고 있어, 여러 산업 폐가스 중에서도 특히 주목받는 자원이다.
◇ Formaldehyde는 전 세계적으로 연간 약 2,500만~3,000만 톤 이상이 생산되어 소비되는 대표적인 기초 화학물질로, 산업적 가치가 매우 큰 물질이다. 높은 반응성과 저렴한 원가 덕분에 다양한 부가가치 화학제품의 전구체로 활용되며, 특히 Melamine - Phenol 수지·요소 수지 등 고부가가치 수지 생산에 핵심적으로 사용된다. 이러한 수지는 접착제, 합판, 파티클보드, MDF, 단열재 제조에 필수적인 성분으로, 건축·가구 산업 전반에서 막대한 수요를 차지한다. 경제적 측면에서도 Formaldehyde는 매우 중요한데, 특히 COG와 같은 철강 산업 부생가스를 원료로 활용할 경우 저부가가치 가스를 고부가가치 화학물질로 전환할 수 있어, 자원 활용 효율을 높이는 동시에 온실가스 저감 효과까지 달성할 수 있다.
◇ 본 연구는 화석연료의 지속가능한 활용을 목표로, Coke Oven Battery에서 생산된 raw COG를 기반으로 Syngas를 생산하여, 최종적으로 고부가가치 물질인 Aldehyde를 얻는 것을 목표로 한다.
◇ 먼저, raw COG는 냉각 공정을 거쳐 온도를 낮춘 후, H₂S/NH₃/BTX scrubber를 통해 해당 물질들을 제거한다. 이후, desorption 공정을 통해 흡수된 성분을 탈착시켜 용매를 재순환한다. 이 일련의 purification 과정을 통해 clean COG를 생산하게 된다. 정제된 clean COG에는 합성연료 (Syngas)와 Olefin을 포함하고 있다. 본 연구는 크게 두 경로로 Formaldehyde를 생산하고자 한다. 먼저, Syngas를 Methanol로 합성하여 Formaldehyde를 생산하고자 한다. 두 번째로는, 대표적 Olefin 물질인 Ethylene을 합성하여 Formaldehyde를 생산하고자 한다. 이처럼 COG를 활용하여 Formaldehyde를 생산해내는 공정을 통합하여 구성하고자 한다.
◇ 마지막으로, 구축된 Aspen Plus 시뮬레이션 모델을 바탕으로 TEA를 수행하여 경제성을 평가하고, 이를 통해 공정의 실현 가능성을 검토한다. 더 나아가, 해당 공정이 관련 산업 전반에 미칠 수 있는 경제적 파급 효과를 분석한다.
개발 과제의 배경
◇ 그림 1을 보면 20세기 이후 인구의 빠른 증가와 산업화의 가속으로 글로벌 에너지 수요는 빠르게 증가하는 추세이다. 이러한 수요는 주로 화석연료의 연소 및 활용으로 충당되었으나, 지구온난화와 환경오염 문제의 발생으로 친환경 에너지 공급원의 개발, 기존 화석 연료의 개질을 통한 탄소 배출 저감 및 환경오염 감축이 요구되고 있다.
그림 1. Global direct primary energy consumption (Energy Institute - Statistical Review of World Energy (2024))
◇ Coke Oven Gas (COG)는 철강 산업의 주요 열원인 코크스의 주 부산물로, 석탄을 무/저산소 조건에서 고온 가열하는 공정에서 생성된다. 과거 COG는 다량의 수소, CH4 등의 가연 성분에 집중하여 단순히 연료로 사용하였다 (그림 2). 그러나 기술의 개발로 CH4를 활용한 SMR (Steam Methane Reforming), WGS (Water-Gas Shift) 등의 공정이 도입되어 Syngas와 수소 생산의 가능성이 입증되었고, COG 내 성분을 다양하게 활용한 고부가가치 생산 공정 연구가 관심을 모으기 시작하였다.
그림 2. Composition of COG (이전 연구에서 발췌)
◇ Syngas는 COG를 통해 얻을 수 있는 대표적인 핵심 원료로, 수소와 CO의 혼합 가스이다. Fisher-Tropsch 합성, Methanol 합성 등 다양한 공정의 원료로 활용되며 꾸준한 산업적 수요를 보이고 있다. 대표적인 Syngas의 생산 원리는 상술한 SMR (Steam Methane Reforming)과 부분 산화 (Partial oxidation)이다. SMR은 CH4를 수증기와 함께 개질하여 Syngas를 얻는 방식이고, 부분 산화는 제한된 산소량에서 CH4를 반응시켜 Syngas를 얻는 방식이다. 본 연구에서는 일차적으로 가치 있는 Olefin 성분을 분리한 후, 남은 COG를 Syngas로 변환하는 공정을 제시할 것이다.
◇ Formaldehyde는 1859년 발견되어 1868년 생산법이 확립된 이래, 가장 중요한 화학적 중간체의 일종으로 간주되어 왔다. 접착제, 고분자 화합물, 페인트, 코팅제 등 산업적으로 광범위하게 활용되는 Formaldehyde의 수요를 충족하기 위해 다양한 생산 공정이 고안되었고, 최초 생산법이었던 Methanol-공기 혼합 증기의 백금 촉매 반응을 시작점으로 수율 제고를 위한 촉매 개발과 공정 개발이 지속되어 왔다.
◇ 다양한 연구에도 불구하고, formaldehyde의 주 생산 방법은 여전히 Methanol을 원료로 한다. 현재 주로 활용되는 BASF 공정 (Water Ballast Process)는 Methanol-물의 혼합물을 사용하며, ICI/Degussa 공정은 Methanol-공기 혼합물을 사용한다. 하지만 두 공정 모두 700K 이상의 고온을 필요로 하기에 대량의 에너지를 요구하는 문제가 있다. 이를 극복하기 위해 최근 주목받는 Formox Process는 Methanol-공기 혼합물을 기존 silver 촉매가 아닌 철-몰리브덴 촉매에 통과시키는 방식으로 550~600 K의 상대적 저온의 반응 조건을 확보하며 에너지 효율을 제고하였다. 하지만 선행 연구에서는 단일 반응기에 대한 반응 조건을 위주로 연구하였기에, 공정 전반에 대한 경제성 및 에너지 분석이 부족한 상태이다.
◇ 따라서 본 연구는 COG – Syngas – Methanol – Formaldehyde까지의 전 생산 공정을 Aspen Plus를 통해 모사 및 연결하고, Formaldehyde 생산 효율을 분석한다. 또한 Syngas 생산 공정 이전에 Olefin을 선제적 분리하여 이를 활용한 고부가가치 부산물 공정을 모사한다. 그림 2에서 활용되는 Olefin인 Ethylene (C2H4)와 Propylene (C3H6)를 각각 분리하여, 가치 있는 물질을 생산하는 Oxidation 공정을 설계한다.
◇ 이를 통해 COG로부터 고부가가치 생산물을 만드는 다양한 공정의 흐름 포트폴리오를 완성한다. 또한 각 공정의 효율 및 경제성 평가를 통해 공정의 현실성과 기술적 타당성을 평가한다. 본 연구로 COG 통합 활용 공정 구조를 완성함으로써 COG를 보다 가치 있게 활용하는 방법론을 제시하고 지구온난화 예방, 탄소 배출 저감에 기여할 수 있을 것이다. 또한 고부가가치 화학제품 전환의 방향 제시로 순환경제 구현과 지속가능한 화학 산업의 패러다임 구축을 돕는다. 궁극적으로 온실가스 배출 저감과 경제적 효율성을 달성하고 탄소 중립 사회로의 전환 가속에 힘을 싣고자 한다.
개발 과제의 목표 및 내용
◇ 따라서 본 연구는 2가지의 큰 갈래로 진행된다. 먼저 첫 번째로 COG – Syngas – Methanol – Formaldehyde까지의 전 생산 공정을 Aspen Plus를 통해 모사 및 연결하고, Formaldehyde 생산 효율을 분석한다. Methanol – Formaldehyde 공정에 기존 연구된 반응기를 도입하여 세부 모사하면서, 차세대 반응기가 도입된 신공정의 운용 효율 검증을 통해 공정의 현실성을 보인다. 위 공정을 구현하는 과정에서, 정제하지 않은 COG에는 NH₃, H₂S, 고체 불순물이 포함되어 있으므로 이를 H₂S 0.01 ppmv 이하, NH₃ 0.1 ppmv 이하, BTX 5 ppmv 이하로 제거하는 것을 목표로 한다. 또한 Methanol 합성 비율에 맞는 Syngas를 제조하기 위하여 CH4를 chemical looping 공정을 통해 H2, CO 비율을 조절한다. Methanol로부터 Formaldehyde를 메탄올 잔존 0.5 wt% 이하, 금속 불순물 1 ppmv 이하로 생산하는 것을 목표로 한다.
◇ 또한 두 번째로 COG 내 Olefin 성분을 활용한 고부가가치 부산물 공정을 모사하고 그 효용을 확인한다. 이를 위해 COG에서 Syngas 생산 공정으로 진행하기 이전 Olefin 성분을 선제적 분리한다. Figure 2에서 확인되는 Olefin인 Ethylene (C2H4)와 Propylene (C3H6)를 각각 활용, Ethylene으로는 Formaldehyde 생산 공정을, Propylene으로는 Propylene oxide, Acrylic acid 등의 생산 공정을 선택하여 연구한다.
◇ 앞선 두 갈래의 공정 모사로 COG를 원료로 하는 고부가가치 물질 생산 공정을 구현한 후, 기술-경제성 평가 (Techno-Economic Analysis, TEA)를 통해 설계한 공정의 현실적, 경제적 타당성을 검토하여 공정 완성도를 종합적으로 판단한다.
관련 기술의 현황
관련 기술의 현황 및 분석(State of art)
◇ COG off-gas에 존재하는 다량의 CH₄를 Reforming하여, Syngas를 제조하는 연구가 활발히 진행되어 왔다. 이 공정은 Steam Reforming, Autothermal Reforming, Dry Reforming으로 구분된다. 가장 상업적으로 사용되는 공정은 Steam Reforming(SMR)이다. 주된 반응은 아래와 같다.
CH₄ + H2O → CO + 3H2 (1)
이 반응은 Ni/Al₂O₃ 촉매 상에서 수행되며, 일반적으로 800–900 °C의 고온과 20–30 bar의 고압 조건에서 운전된다. 흡열반응으로, 외부 열원을 필요로 하며, 반응 평형은 온도가 높을수록 Syngas 생성량이 늘어나지만 과도한 온도에서는 촉매 열화 및 탐소침적이 촉진된다.
◇ COG off-gas에 존재하는 다량의 Syngas(H2, CO2)로부터 Methanol을 생성하는 연구는 활발히 진행되어 왔다. Methanol의 경우 H2와 마찬가지로 차세대 연료로 주목받고 있으며, 최근에는 단순 화학원료의 범위를 넘어 탄소중립 시대의 핵심 에너지 캐리어 및 전환 플랫폼으로서 그 중요성이 재조명되고 있다. Syngas로부터 Methanol을 합성하는 주된 반응은 아래와 같다.
CO + 2H2 → CH3OH (2)
CO2 +3H2 → CH3OH + H2O (3)
CO2 +3H2 ↔ CO + H2O (RWGS) (4)
이 반응들은 모두 Cu/ZnO/Al₂O₃ 촉매 상에서 수행되며, 일반적으로 200–300 °C의 중온과 40–100 bar의 고압 조건에서 운전된다. 온도가 지나치게 높으면 Methanol이 열분해되거나 CO₂ 전환율이 저하되고, 온도가 낮으면 반응속도가 급격히 떨어지므로 이 범위가 최적 영역으로 평가된다. 반응물의 몰비는 통상적으로 H₂/(CO + CO₂) 의 비율을 수율과 운전 조건에 따라 2-3 정도로 조정하며, 미반응 가스는 재순환(recycle)하여 원료 활용 효율을 높인다. 상업적 Methanol 생산 공정은 Lurgi 및 ICI(Imperial Chemical Industries) 공정이 대표적이다. 초기의 고압(250 bar 이상) 공정은 높은 장치비를 요구했으나, Cu계 촉매의 도입 이후 저압 공정(50–100 bar) 으로 전환되며 에너지 효율이 크게 개선되었다. 일반적으로 다관형 고정층(multitubular fixed-bed) 반응기를 이용하며, 반응 후 생성된 Methanol·물 혼합물은 응축 및 저압 증류를 통해 순수 Methanol로 분리된다.
그림 3. Reaction mechanism of methanol production from Syngas
◇ Ethylene(C2H4)으로부터 Ethanol(CH3OH)을 생산하는 대표공정은 Ethylene direct hydration이다. 산업적으로는 고체 담지형 인산(Phosphoric Acid) 촉매를 실리카/규조토 등에 담지한 SPA(H₃PO₄/SiO₂) 를 고정층 반응기에 충전하여, Ethylene과 수증기 혼합물을 고압·중온에서 통과시키는 방식이 표준이다. 생성물은 주로 Ethanol이며, 부반응으로 디에틸 에테르(di-ethyl-ether)가 소량 형성될 수 있다. SPA는 강한 브뢴스테드 산성점과 안정한 담지 구조 덕분에 상업 공정에서 오랫동안 주력으로 쓰여 왔다. 공정은 250–300 °C, 70–80 bar 범위에서 운전되며, Ethylene:Steam 몰비는 촉매 탈활성(인산 용출)과 에테르 형성 억제를 동시에 고려하여 수증기를 과량이 되지 않게 설정한다. 논문에 따르면, 몰 기준 수증기/Ethylene = 0.6 조건에서 단일 패스의 전환율은 4–25%로 보고되며, Ethanol selectivity가 98%라고 보고된다. 단일 패스의 전환율이 낮으므로 미반응 가스를 Recycling하여 전체 수율을 높인다. Indirect hydration 라고 불리는 황산 흡수–가수분해 2단계 공정(Ethyl hydrogen sulfate/Diethyl sulfate 중간체 경유)이 먼저 상업화되었지만, 부식·폐산 처리·에너지 비용 등의 한계로 현재는 직접 수화 공정이 주류로 자리 잡았다.
◇ Formaldehyde 생산의 주요 경로는 Formox 공정과 은 촉매 공정으로 구분된다. Formox 공정은 Methanol을 산화철–몰리브덴(Fe–Mo) 복합 산화물 촉매 위에서 부분 산화시켜 Formaldehyde를 생성하는 방식이다. 해당 반응은 세 단계로 구분된다. 먼저 Methanol이 촉매 표면에서 해리 흡착되어 메톡시–몰리브덴(Mo–OCH₃) 종을 형성하고, 다음으로 이 메톡시 리간드가 산화되어 Formaldehyde로 탈리되며 촉매가 환원된다. 마지막으로 산소에 의해 촉매가 재산화되어 순환이 완결된다. Waters은 이러한 3단계 메커니즘이 실제 Formox 고체 촉매에서 일어나는 반응과 본질적으로 동일함을 기상 질량분석 기반 촉매 주기 실험으로 검증하였다. 특히 Mo₂O₆(OH)⁻ 이온 쌍이 Methanol을 Formaldehyde로 산화하는 과정에서 이원자 몰리브데이트 중심이 핵심적으로 작용함을 규명하였으며, 단핵체 시스템에 비해 훨씬 높은 반응성을 보인다고 보고하였다. 이는 Fe–Mo 산화물계 촉매의 이중 금속 산화 중심이 공정의 선택도와 활성 향상에 기여함을 뒷받침한다.
그림 4. Gas-phase catalytic cycles for the oxidation of methanol to formaldehyde
◇ Ethanol로부터 Acetaldehyde를 생산하는 주요 경로는 비산화 탈수소화(dehydrogenation) 공정이다. 이 공정은 일반적으로 Cu 기반 촉매를 사용하며, 500 K 이상에서 높은 전환율과 선택도를 확보할 수 있다. 탈수소화 반응은 흡열성이며, 부생성 수소를 동시에 얻을 수 있기 때문에 COG 기반 통합 공정과의 연계성이 높다. Pang은 계층적 구조의 Cu-MFI Zeolite catalyst를 설계하여, 523 K에서 97%의 에탄올 전환율과 93%의 아세트알데하이드 선택도를 500시간 이상 유지함을 보고하였다.이는 촉매 표면의 Cu⁺와 Cu⁰ 간의 전자 이동이 탈수소화 반응 주기를 안정적으로 유지함을 의미한다. 연구진은 Cu⁺가 에탄올의 O–H 결합을 활성화하여 에톡시 중간체를 형성하고, 이후 β-C–H 절단을 통해 Acetaldehyde를 생성하며, 생성된 H 원자가 Cu⁰로 이동해 H₂로 탈리되는 Cu⁺/Cu⁰ 이원 활성 메커니즘을 제시하였다. 이러한 Cu 기반 비산화 탈수소화 공정은 귀금속 촉매를 대체할 수 있는 경제적이고 지속 가능한 경로로 평가된다. Pang의 연구에 따르면, Cu-MFI의 높은 안정성은 제올라이트 내 미세공극이 Cu 종의 소결을 억제하기 때문이며, 이는 기존 Cu/SiO₂ 촉매보다 장기 운전 성능이 우수함을 보여준다. 또한 동일 논문은 ZnO, Al₂O₃, 탄소 지지체 등과의 복합 구조 설계를 통해 Cu⁺의 전자밀도 조절 및 선택도 향상 가능성을 제시하였다. 이러한 연구는 향후 COG-기반 Ethanol 탈수소화를 통한 Acetaldehyde 생산 공정의 상용화에 필요한 촉매 수명 및 공정 통합 설계 방향성을 제공한다.
그림 5. Typical reaction networks for Ethanol dehydrogenation
◇ COG off-gas에 포함된 C2계 Olefin 중 Ethylene을 활용하고자 하는 연구는 꾸준히 진행되어 왔다. 특히 Ethylene을 Acetaldehyde로 반응시키는 산업적 process인 Wacker process(Hoechst-Wacker process)는 1960년 첫 공정 설립 이래 꾸준히 Acetaldehyde 생산의 주요 path로 여겨져 왔으며, PdCl2 수용액과 CuCl2 촉매를 기반으로 한다. 더 높은 수율의 반응 조건을 찾고 공정 성능 향상을 위해 Lambert et al. 은 Wacker process에 대한 C2-C4까지의 Olefin-Aldehyde 반응의 PdCl2 촉매에서의 kinetics을 연구하였다. 연구에서는 Pd과 O2의 농도 변화에 따른 C2-C4의 전화율을 확인하고 반응 속도 및 활성화 에너지 값을 제안하였다. 실험 결과에 따르면 올레핀/O2 비율은 화학양론적인 2:1의 비율이 유지되어야 하며, Pd 이온의 재생 반응이 병목이 될 가능성을 제시하였다.특허 에 의하면 현재 산업적으로 가장 활발히 사용되는 촉매는 PdCl2 – CuCl2 – HCl 액상 Wacker process이며, 본 연구의 Ethylene-Acetaldehyde 공정 모사에서도 동일한 촉매 조건을 사용한다.
그림 6. Catalytic Cycle of Wacker Process
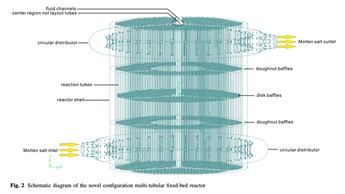
◇ COG의 off-gas 내 Olefin 중 C3H6 (Propylene)을 활용하고자 하는 연구 또한 진행되고 있다. C3H6를 Acrolein (C3H4O) 으로 선택적 부분 산화 (Selective Partial Oxidation) 하는 반응은 Acrylic Acid 생산의 첫 번째 단계로서 산업적으로 매우 중요한 경로이다. 이 반응은 높은 발열성을 가지므로 이 공정 구현의 핵심 과제는 반응기 내에서의 효율적인 열 관리와 촉매 비활성화 및 부산물 생성 방지라고 할 수 있다. 그림 7에 나와 있는 Multitubular Fixed-bed Reactor을 사용하며, 최적의 열 제거를 위해 최대 30,000개의 튜브로 구성될 수 있다.
그림 7. Multitubular Fixed-bed Reactor의 diagram
촉매로는 우수한 selectivity를 보이는 Bismuth Molybdate (Bi(MoO4)3) 기반 촉매가 사용된다. C3H6 전환율 95% 이상, 튜브 압력 강하 10% 미만, 반응 온도 633-703 K 유지 등의 설계 제약 조건을 충족하도록 공정을 구현해야 한다. 반응열을 제거하기 위해 냉각재로 높은 열용량과 우수한 열전달 계수를 가진 Molten Salt를 이용한다. 이 반응은 Redox Mechanism, 즉 Mars-van Krevelen Mechanism을 따르는 것으로 확인되었으며, 이는 lattice oxygen을 산소원으로 사용하여 분자 산소보다 선택적 산화에 유리하다. 목표 물질인 Acrolein 외에도 연속적인 산화 반응을 통해 Acrylic acid가 생성되거나, Acetaldehyde, CO2, CO 등의 부산물이 생성된다. 복잡한 반응 관계를 담은 반응 네트워크 모델이 개발되었고 31개의 운동 매개변수를 통해 공정의 동적 거동과 제어 전략 수립에 이용된다.
그림 8. Reaction networks for Propylene selective partial oxidation
나. 특허조사
◇ US 9102532 B2 (“Method for producing synthesis gas for methanol production”) 이 특허는 천연가스를 원료로 하여 Syngas를 생산하는 방법에 관한 것이다. 기존의 Steam Reforming 공정은 800–950 °C의 고온과 Ni 촉매가 필요한 흡열반응이지만, 생성가스 내 수소가 과잉되고 CO/CO₂ 비가 낮아 메탄올 합성 공정 효율이 떨어지는 한계가 있었다. 본 발명은 이러한 문제를 개선하기 위해, 원료 가스의 일부를 촉매 부분산화(Catalytic Partial Oxidation, CPO)로, 나머지를 수증기 개질과 Water-Gas Shift (WGS) 반응으로 각각 처리한 뒤, 두 스트림을 재결합하는 이중 경로 개질 방식을 제안한다. 이 공정에서는 첫 번째 스트림이 CPO 반응을 거쳐 H₂, CO, CO₂ 등을 포함하는 혼합가스를 형성하고, 두 번째 스트림은 SR과 WGS를 통해 추가적인 CO와 H₂를 생성한다. 이후 두 혼합가스를 혼합하여 최종 Syngas의 (H₂ − CO₂)/(CO + CO₂) 비율(R ratio)을 약 1.95 ~ 2.05로 조정한다. 이는 메탄올 합성 반응에 가장 적합한 조성 범위로 알려져 있으며, 공정 전체의 수소 과잉 문제를 완화하고 열효율을 높일 수 있다.
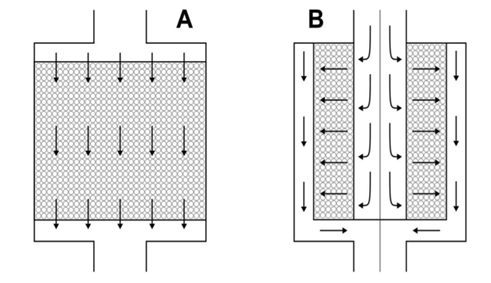
◇ Johnson Matthey Davy Technologies: “Process and plant for the production of methanol” (EP 1262228 A1) 이 특허는 Syngas의 대용량 처리에서 반응기 내 열 제거(핫스폿)와 압력강하 문제를 줄이기 위해, 촉매층을 수평 방향으로 얕게(“shallow bed”) 배치하고, 기체 유동을 수직 방향으로 통과시키는 독특한 촉매 볼륨 레이아웃을 제안한다. 얕은 층은 같은 촉매량에서 단면적을 넓혀 열전도·복사에 의한 온도 평탄화를 돕고, 하부의 상대적으로 뜨거운 영역에서 상부의 차가운 영역으로 열을 빠르게 전달하여 온도 구배를 완화한다. 이 배치는 대형기에서의 열관리 안정성과 장치 내 압력강하 저감을 동시에 노려, 기존 수직 용기·깊은층 설계 대비 운전 윈도우를 넓히는 것이 포인트다. 대규모 루프에서 고압 분리기–재순환과 결합하면, 고부하에서도 촉매 수명과 선택도 유지에 유리하다.
◇ Luyben, William L. "Design and control of a methanol reactor/column process." Industrial & engineering chemistry research 49.13 (2010): 6150-6163. Luyben (2010)의 “Design and Control of a Methanol Reactor/Column Process” 논문은 Syngas로부터 메탄올을 생산하는 공정의 설계·운전 통합을 체계적으로 분석한 대표적인 선행연구이다. 이 연구는 고정된 Syngas 유량에서 경제성을 극대화하기 위해 반응기 압력·온도, 플래시탱크 압력, 리사이클 비율, 증류단수 등을 변수로 설정하고 Aspen Plus 시뮬레이션을 통해 최적 조건을 도출하였다. 반응기는 Cu/ZnO/Al₂O₃ 촉매를 적용한 다관식 튜브형 구조로, LHHW( Langmuir–Hinshelwood–Hougen–Watson ) 형태의 Vanden Bussche–Froment 속도식을 사용하였다. 반응은 264 °C 의 중온 조건에서 고압 증기를 발생시키며, 약 110 bar 에서 운전되어 에너지 회수와 생산효율의 균형을 이룬다. 이때 전체 탄소전환율은 약 96%에 달하며, gas recycle ratio는 3.36, purge ratio은 2.2%로 설정되었다. 또한 2 bar 저압 플래시 드럼과 42단 증류 컬럼을 통해 MeOH/물 분리를 단순화하였다. 경제성 분석 결과 에너지 및 자본 비용보다 제품 수율이 수익성에 지배적임을 보였고, 반응기 압력 상승은 전환율 증가 효과와 압축 비용 증가 효과 사이의 절충점에 의해 결정됨을 밝혔다. Luyben은 또한 플랜트 전체의 조작성 향상을 위해 공정 압력을 직접 제어하지 않고 부동시켜 상호보완적 루프제어를 적용하는 새로운 Plant-wide Control 전략을 제시하였다. 이는 공정 교란이나 Syngas 조성 변동에도 제품 규격을 유지하는 제어 구조로 검증되었다. 따라서 이 논문은 반응기–증류–재순환 시스템을 하나의 통합 체계로 접근한 첫 사례로서, 이후 메탄올 공정의 에너지 통합, 재순환 최적화, 제어 전략 수립 연구들의 기반이 되었다.
◇ US 4181629A (“Catalyst for the oxidation of methanol to formaldehyde …”) 미국 특허, 발행일 1980-01-01 이 특허는 Methanol을 Formaldehyde로 전환하기 위한 산화촉매 조성 및 그 제조방법을 제안한다. 구체적으로는 알루미나 또는 실리카 지지체 위에 철산화물(Fe-oxide) 및 몰리브덴산화물(Mo-oxide)를 조합해 코팅한 촉매를 사용하며, 지지체의 비표면적과 공극 부피를 낮게 유지함으로써 과산화(완전산화)로의 진행을 억제하고 높은 선택도 확보가 가능하다고 기술되어 있다. 핵심 포인트는 (i) 지지체의 특성(비표면적 ≤ 1 m²/g, 공극부피 ≤ 0.2 mL/g) 제어, (ii) Mo:Fe 원자비 ≈ 1.5-2.5:1 설계, (iii) 기상 반응 온도 약 300 °C 조건에서 메탄올 전환율 ≈ 95% 및 선택도 ≈ 80%를 보고한 점이다. 이로써 Formox형 산화철–몰리브덴 산화물 촉매 적용 가능성과 고유한 설계 변수 제시가 특허의 의의이다.
◇ 유연식, 신현종, 최병렬, 최영현, 조영진, 김덕기, 박주연, 박광호, "불포화 알데히드 및/또는 불포화 산의 제조방법," 대한민국 특허 KR10-0714606B1, 출원일 2006년 2월 20일, 공고일 2007년 5월 7일, 특허권자: 주식회사 엘지화학.
본 특허는 Propylene으로부터 불포화 Aldehyde (Acrolein) 및 불포화 Acrylic Acid를 제조하는 Shell-and-Tube 반응기에 관한 것으로, 촉매 유효성분 내부의 세공 밀도 및 크기 조절을 통해 촉매 활성을 단계적으로 제어함으로써 Hot spot 문제를 해결하고 고수율의 생성물 제조를 가능하게 하는 기술이다. 전통적인 Mo-Bi계 촉매를 사용하되, 반응기 입구에서 출구로 갈수록 촉매 비표면적이 증가하도록 다층 충진하여 발열 반응을 효과적으로 제어하는 것이 핵심이다. Propylene을 Acrolein 및 Acrylic Acid로 전환하는 공정은 일반적으로 두 단계로 구성된다. 제1단계에서는 Mo-Bi계 촉매를 사용하여 Olefin을 불포화 Aldehyde로 전환하고, 제2단계에서는 Mo-V계 촉매를 이용해 불포화 Aldehyde를 불포화산으로 산화시킨다. 이 반응은 매우 강한 발열 반응(–347 kJ/mol)으로 반응기 입구에서 Hot spot이 발생하여 COx 부산물이 증가하고, 고온에 노출된 촉매의 비활성화가 가속화되어 촉매 수명이 단축되는 문제가 발생한다. 본 특허는 촉매 제조 시 요소, 나프탈렌 등 승화성 또는 열분해 물질을 첨가하여 건조·소성 과정에서 이들이 제거되며 세공을 형성하도록 함으로써 촉매 비표면적을 5-100 m²/g 범위에서 정밀 조절한다. 반응기 입구에는 저활성 촉매, 중간에는 중활성 촉매, 출구에는 고활성 촉매를 다층 충진하여 반응물 농도 분포에 따라 촉매 활성을 최적화한다. 실험 결과 다층 충진 시 프로필렌 전환율 98.9%, 선택도 97.3%, 수율 96.2%를 달성하였으며, 최대 발열부 온도도 340 ℃로 단일 촉매 대비 19 ℃ 낮았다. 4,000시간 장기 운전 후에도 수율 96.1%를 유지하여 안정성과 내구성이 입증되었다. 본 기술은 촉매 크기를 균일하게 유지하면서 세공 조절만으로 활성을 정밀 제어하여 반응관 막힘 없이 높은 전환율과 선택도를 동시에 달성하며, 상업적으로는 2-3단 촉매층으로 충분한 효과를 얻을 수 있다.
◇ US 4220803A (“Catalytic dehydrogenation of ethanol …”) 미국 특허, 발행일 1980-12-30 이 특허는 Ethanol을 Acetaldehyde 및 Acetic acid로 전환하는 기상 산화적 탈수소화(Oxidative Dehydrogenation, ODH) 공정을 제안한다. 여기서는 산소와 Ethanol 혼합가스를 Cu-크롬 산화물 지지 촉매(바륨 제외) 위에서 접촉시키며, 산소:Ethanol 몰비를 약 0.1 ~ 0.5 범위로 제시하고 있다. 주요 기술 포인트는 (i) 고농도 Ethanol 투입 가능성 확보, (ii) 바륨이 없는 촉매 조성으로 수명 및 선택도 개선, (iii) Acetaldehyde와 Acetic acid을 높은 선택도로 동시에 생산하는 공정 구조이다. 본 특허는 특히 Ethanol→Acetaldehyde 경로에서 촉매 설계 및 반응조건(산소/Ethanol 비율, 온도) 조정에 관한 산업 적용 가능성 높은 기술을 담고 있다.
◇ Hoechst AG. Verfahren zur Oxydation von Olefinen zu Aldehyden, Ketonen oder den Aldehyden entsprechenden Säuren. German Patent DE 1190451 B, issued April 8, 1965. 해당 특허는 Olefin을 Aldehyde/Ketone/Carboxylic acid로 산화하는 공정을 제안하며, 현대적 Wacker process의 핵심 아이디어를 제시하고 있다. Ethylene 등 Olefin을 air 등 산소 함유 가스로 산화시키는 흐름으로, 수용액 하에 Pd계 촉매와 구리 산화물 등 산화/환원 보조계를 촉매로서 포함한다. Pd계 촉매 외 주기율표 8족 귀금속이 사용될 수 있으며, 이러한 촉매 조성은 수용액 내 8족 귀금속과 그 염이 올레핀과 착물을 형성하고 산화/환원 보조계와 함께 촉매로 작동하는 Wacker-Hoeschst형 수(水)계 Pd/Cu/HCl 시스템의 토대이다. 즉 Pd계(주기율표 8족계) 촉매와 산화/환원 보조계를 결합한 연속 운전이 가능한 균일계(Homogeneous) 촉매 공정을 제시하는 데에 의의가 있다. 촉매-레독스(산화/환원) 조합 반응 조건을 기-액 접촉이 보장되는 흡수탑/버블탑/충전탑류 장치에 적용 가능함을 시사하며, 2단 운전 등 전화율 제고를 위한 방향성을 제시한다. 뿐만 아니라 공기 사용, 재순환, 분무/비말 회수, 부식/촉매 손실 억제 등 개량 특허의 출발점으로 위치하고 있다. 해당 촉매 구조는 현재 Wacker process에 적용되어 Aldehyde 생산에 사용되고 있으나 경우에 따라 케톤, 탄소 개수에 상응하는 Carboxylic acid 제조까지 가능함을 시사하고 있다.
다. 특허전략 ◇ 본 연구는 COG로부터 Aldehyde군 고부가가치 생산물을 제조하는 통합 공정을 설계한다는 점에서 기존 연구와 명확한 차별성을 갖는다. 기존 연구들이 COG를 단순 연료로 활용하거나 수소 생산에 집중한 반면, 본 연구는 COG 내 다양한 성분(Syngas, olenfin)을 체계적으로 분리·활용하여 Formaldehyde를 포함한 Aldehyde군 화합물을 생산하는 전체 공정 포트폴리오를 구축한다는 점에서 독창적이다.
◇ 특히, COG에서 Aldehyde군 고부가가치 화합물을 생산하는 연구는 선행 사례가 거의 없으며, 본 연구가 이 분야의 선구적 연구가 될 것으로 예상된다. 기존 Formaldehyde 생산 연구들이 단일 반응기 수준의 촉매 개발이나 반응 조건 최적화에 집중한 것과 달리, 본 연구는 촉매 개발이 아닌 공정 전체의 설계, 통합, 경제성 및 환경성 평가에 초점을 맞춘다.
◇ 본 연구는 크게 두 가지 전략적 접근으로 진행된다. 첫 번째 전략은 COG 정제 후 Syngas 기반 Formaldehyde 생산 경로이고, 두 번째 전략은 Olefin 선제적 분리 및 Aldehyde군 생산 경로이다.
◇ 첫 번째 전략은 COG를 정제하여 Syngas를 생산하고, 이를 기반으로 Methanol을 거쳐 최종적으로 Formaldehyde를 생산하는 경로이다. 먼저 coke oven에서 생성된 raw COG를 정제하여 clean COG를 생산한다. 정제된 clean COG에는 H2와 CO를 포함한 Syngas 성분과 Olefin이 함유되어 있다. 본 연구에서는 clean COG로부터 Syngas를 제조하기 위해 다양한 개질 기술을 검토하고, Methanol 합성에 최적화된 H2/CO 비율을 달성할 수 있는 공정을 선정하여 적용한다. 생산된 Syngas는 Methanol 합성 반응기로 공급되며, 여기서 생성된 Methanol은 산화 반응을 통해 최종 목표 생산물인 Formaldehyde로 전환된다.
◇ 두 번째 전략은 clean COG에서 Olefin 성분을 선제적으로 분리하여 고부가가치 화합물을 생산하는 경로이다. Clean COG에 포함된 Ethylene, Propylene 등 Olefin과 기타 탄화수소를 먼저 분리하고, Ethylene은 Wacker process를 통해 Aldehyde를 생성하고 Propylene은 산화 반응을 통해 Acrolein (Aldehyde의 한 종류)을 생성한다. 이러한 접근은 Syngas 전환 경로로 진행하기 전에 보다 직접적이고 효율적인 방법으로 Aldehyde군 화합물을 생산할 수 있다는 장점이 있다.
◇ 이러한 이중 경로 전략은 COG의 모든 가치 있는 성분을 최대한 활용하여 경제성을 극대화하는 동시에, 다양한 시장 수요에 대응할 수 있는 유연한 생산 체계를 구축한다.
◇ 본 연구는 Aspen Plus 소프트웨어를 활용한 전체 공정의 모델링 및 최적화를 핵심 방법론으로 채택한다. 촉매 개발이나 실험실 규모의 반응 연구가 아닌, 산업 현장에 적용 가능한 실제 플랜트 규모의 공정 설계를 목표로 한다.
◇ 공정 설계의 현실적 타당성을 검증하기 위해 TEA(Techno-Economic Analysis)를 수행할 예정이다. TEA를 통해서 투자비, 운전비, 생산원가, 순현재가치(NPV), 내부수익률(IRR), 투자 회수 기간 등의 재무 지표를 산출하고 주요 변수에 따른 민감도 분석을 수행한다. 이를 통해 COG 활용 Aldehyde군 생산 분야의 선구적 연구를 수행하여 저부가가치 산업 폐가스를 고부가가치 화합물로 전환하는 공정 모델을 제시할 수 있고, 단순한 공정 설계를 넘어 실제 산업 현장 적용 가능성을 종합적으로 입증할 수 있다.
개발과제의 기대효과
기술적 기대효과
◇ COG는 H2, CH4, Olefin 등 가치 있는 물질을 다량 함유하고 있기에 여러 방면으로의 활용이 주목되는 물질이다. 특히 최근 가장 주목받는 물질인 수소를 비교적 고농도로 포함하고 있으므로 고부가 화학 원료의 전환이 가능한 자원이다. 또한 Aldehyde는 다양한 화학 물질의 중간체(intermediate)로 사용되며, 후속 공정에 의해 산(Acid), 에스터(Ester), 플라스틱, 수지, 용제 등으로 전환될 수 있는 고부가가치 전구체이다. 본 연구에서는 COG에서 알데하이드까지의 전환 공정을 Aspen Plus로 모사하고, COG 내 물질의 선택적 분리와 Aldehyde까지의 다양한 루트를 제안하여 COG와 Aldehyde 간의 기술적-산업적 연결성을 보이고자 한다.
◇ COG의 처리 및 활용 공정에 관한 연구는 많이 선행됐으나, 이는 공정 내 Scrubbing, Stripping 등 부분 공정에 국한되어 왔다. 본 연구는 raw COG로부터 purification 과정을 거친 off-gas를, PSA(Pressure-Swing Adsorption)와 증류(distillation) 등의 방식으로 분리 후 분리된 물질군(Group) 별로 Aldehyde 생산 공정까지 연결하여 COG-to-Aldehyde 공정 네트워크의 기술적 가능성을 시험한다. 뿐만 아니라 Raw COG부터 생산물(Aldehyde)까지의 전 공정을 통합적으로 모사하여 성능 및 경제성을 평가함으로써 공정 전체에 대한 동시 성능 연구를 진행한다.
◇ 특히 Ethane(C2H6)과 Ethylene(C2H4)의 분리는 두 물질의 비교적 비슷한 끓는점과 물성 등의 이유로 기존에는 membrane, 극저온 증류 등의 까다로운 방식으로 진행되었고, 주기적인 막 교체 비용이나 극저온 상태 유지 비용 등의 단점이 존재했다. 본 연구에서는 Ethane-Ethylene 혼합 기체에서 Ethylene의 선택적 반응을 통해 Ethanol, Acetaldehyde를 생산하여 기체-액체 flash 분리하는 공정을 도입하여, Ethane-Ethylene 분리의 새로운 방식을 제안한다.
경제적, 사회적 기대 및 파급효과
◇ 본 연구에서 제안하는 COG-to-Aldehyde 전환 공정은 철강산업의 부산물인 COG를 부가가치가 낮은 연료용 가스가 아닌 고부가 화학원료 생산 자원으로 재활용함으로써, 산업 내 자원 순환형 가치사슬(Resource Circular Economy) 구축에 기여한다. COG는 기존에 단순 연소 또는 부분산화(SMR, ATR) 등의 용도로 활용되어 왔으나, 본 연구의 공정은 이를 직접 고부가 화합물인 Aldehyde로 전환하므로 원료 단가 대비 부가가치를 약 3~5배 이상 향상시킬 잠재력을 가진다.
◇ 철강 공정과 화학 공정을 통합(Integration) 하는 “철강-화학 융합 공정”을 실현함으로써, 기존 석유계 원료로부터 생산되던 Aldehyde류의 생산비를 절감하고 화석자원 의존도를 완화할 수 있다. 국내 주요 제철소에서 연간 배출되는 COG는 약 8~10 billion Nm³ 수준으로, 이를 활용한 공정이 상업화될 경우 연간 수천억 원 규모의 원료 절감 및 신시장 창출 효과가 기대된다.
◇ 본 공정은 극저온 분리나 고비용의 membrane 시스템을 대체할 수 있는 반응-분리 결합형(reactive separation) 공정 구조를 도입함으로써, 설비 투자비(CAPEX) 및 운영비(OPEX)를 모두 절감할 수 있다. 이로써 산업 전반의 에너지 효율성 향상 및 온실가스 감축에 따른 경제적 보상(ETS credits, LCA benefits) 도 동시에 확보할 수 있다.
◇ 국내 최초로 COG의 정제부터 고부가 화합물 생산까지를 하나의 통합 공정으로 설계 및 모사한 사례로서, COG의 전주기(End-to-End) 활용 가능성을 제시함으로써 산업 구조의 패러다임 전환을 촉진하는 효과를 기대할 수 있다. 지금까지 COG 관련 연구는 탈황, 탈암모니아, PSA 등 “정제 단계”에 머물러 있었으나, 본 연구는 정제 이후 분리·반응·생산까지를 모두 하나의 시스템으로 통합 설계하였다. 이러한 접근은 COG를 단순한 부생가스가 아닌 ‘신규 화학원료 플랫폼(Alternative Feedstock Platform)’으로 인식하게 하는 사회적 전환점을 마련하며, 향후 철강·정유·화학 산업 간의 연계 확대를 촉진한다.
◇ 본 연구는 COG를 고부가 화학제품으로 전환할 수 있는 실질적 공정 설계 로드맵을 제시했다는 점에서 사회적 실현 가능성이 높다. 현재 상용화된 COG 활용 기술이 거의 없는 상황에서, 본 연구의 모사 결과는 향후 실증 프로젝트나 산업 기술이전의 기반이 될 수 있으며, 이는 국내 철강산업의 탈탄소화와 부가가치화 전략을 동시에 달성하는 국가적 모델로 확장될 잠재력을 가진다.
기술개발 일정 및 추진체계
개발 일정
내용
구성원 및 추진체계
내용
설계
설계사양
제품의 요구사항
내용
설계 사양
내용
개념설계안
내용
이론적 계산 및 시뮬레이션
내용
상세설계 내용
내용
결과 및 평가
완료 작품의 소개
프로토타입 사진 혹은 작동 장면
내용
포스터
내용
관련사업비 내역서
내용
완료작품의 평가
내용
향후계획
내용
특허 출원 내용
내용